Содержание
- 2. Расчет фактора эквивалентности
- 3. Эквивалент одного и того же вещества может меняться в зависимости от того, в какую реакцию оно
- 4. Закон эквивалентов Закон эквивалентов был открыт в 1792 г. И. Рихтером. Современная формулировка закона: Вещества взаимодействуют
- 5. Жидкое состояние. Растворы.
- 6. Жидкое состояние. 1. В жидкостях наблюдается ближний порядок – упорядоченное расположение частиц на расстояниях нескольких нанометров.
- 7. Жидкое состояние. 2. Жидкое состояние по свойствам ближе к твердому. Эти состояния называются конденсированными. Сходство подтверждается
- 8. Жидкое состояние 3. Жидкости изотропны, тогда как кристаллы анизотропны. 4. Жидкость существует в температурном интервале, ограниченном
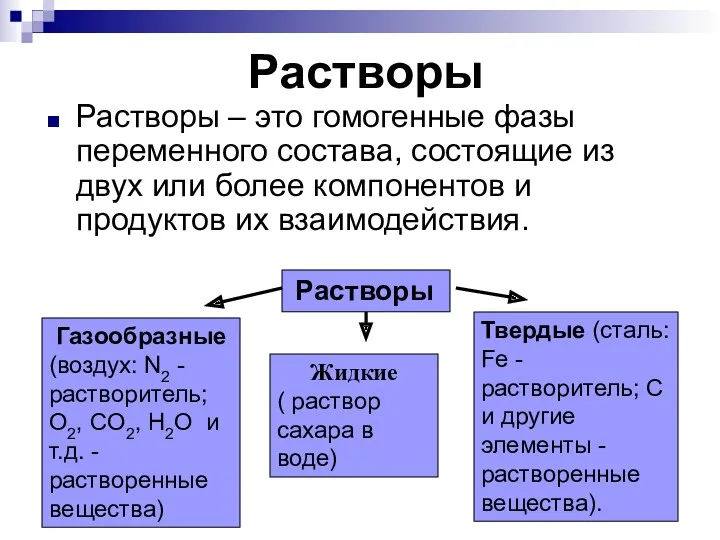
- 9. Растворы Растворы – это гомогенные фазы переменного состава, состоящие из двух или более компонентов и продуктов
- 10. Раствор состоит из одного или нескольких растворенных веществ и растворителя. Растворителем считают компонент, агрегатное состояние которого
- 11. Насыщенный раствор – это раствор, содержащий максимально возможное (для данных условий) количество растворенного вещества. Насыщенный раствор
- 12. Концентрированный раствор —раствор с высоким содержанием растворённого вещества. Концентрированные растворы могут образовывать только хорошо растворимые вещества.
- 13. Способы выражения концентрации Массовая доля - это отношение массы растворенного вещества Х к общей массе раствора:
- 14. Способы выражения концентрации Молярная концентрация (молярность) c(Х) - отношение количества вещества к объему раствора. c(Х) =
- 15. Способы выражения концентрации Моляльность (b) - отношение количества вещества Х к массе растворителя b(X) = Титр
- 16. Коллигативные свойства растворов Некоторые физико-химические свойства разбавленных растворов определяются только количеством частиц этого вещества в растворе
- 17. Коллигативные свойства растворов В случае электролитов в эти формулы вводится поправочный коэффициент, который называется изотоническим коэффициентом
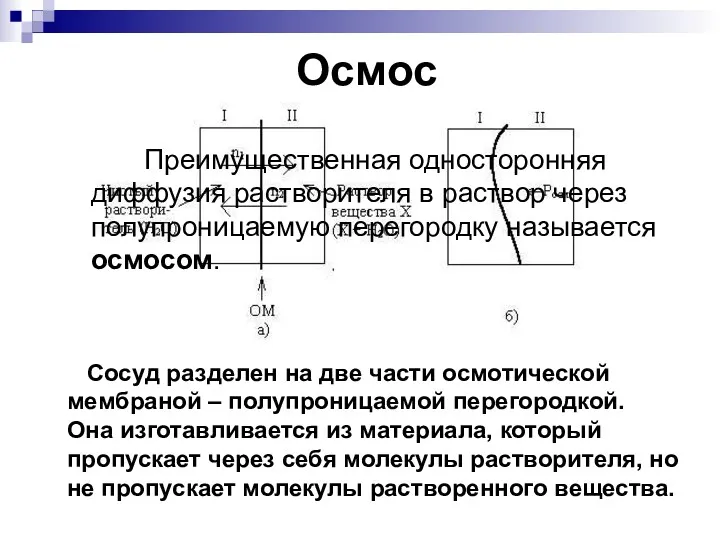
- 18. Осмос Сосуд разделен на две части осмотической мембраной – полупроницаемой перегородкой. Она изготавливается из материала, который
- 19. n1>n2 Объем I будет уменьшаться, а объем II увеличиваться. Эластичная осмотическая мембрана выгнется влево. Получается, что
- 20. Закон осмотического давления Осмотическое давление равно тому давлению, которое производило бы растворенное вещество, если бы оно
- 21. Закон Рауля Если жидкий летучий растворитель (например, воду) поместить в замкнутый объем, то Н2О(ж) Н2О(г) Равновесное
- 22. Величина называется относительным понижением давления пара над раствором. Относительное понижение давления насыщенного пара растворителя над раствором
- 23. Первое следствие из закона Рауля Раствор нелетучего вещества имеет температуру кипения выше, чем у чистого растворителя.
- 24. Второе следствие из закона Рауля Раствор нелетучего вещества имеет температуру замерзания ниже, чем у чистого растворителя:
- 26. Скачать презентацию





















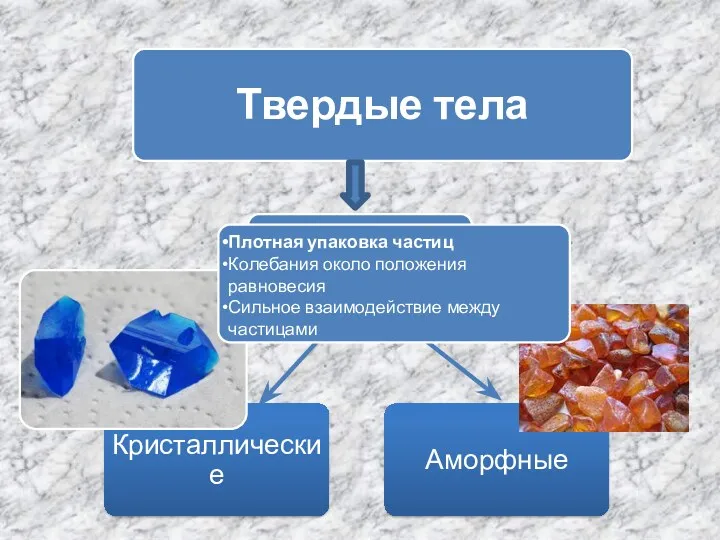 Твердые тела - кристаллические и аморфные
Твердые тела - кристаллические и аморфные Галогенопроизводные. Растворимость, общие закономерности
Галогенопроизводные. Растворимость, общие закономерности Відносна молекулярна маса
Відносна молекулярна маса Переработка угля
Переработка угля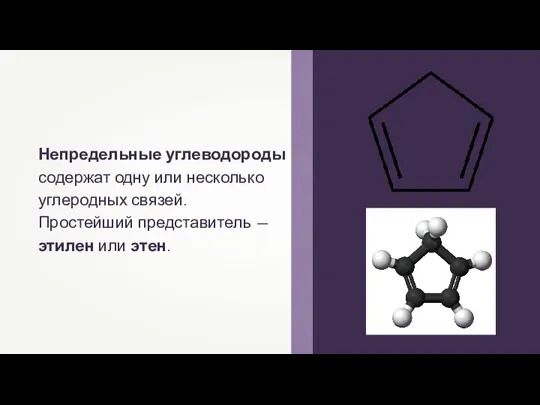 Физические и химические свойства алкенов
Физические и химические свойства алкенов Химические профессии на стройках Олимпиады
Химические профессии на стройках Олимпиады Щелочные металлы
Щелочные металлы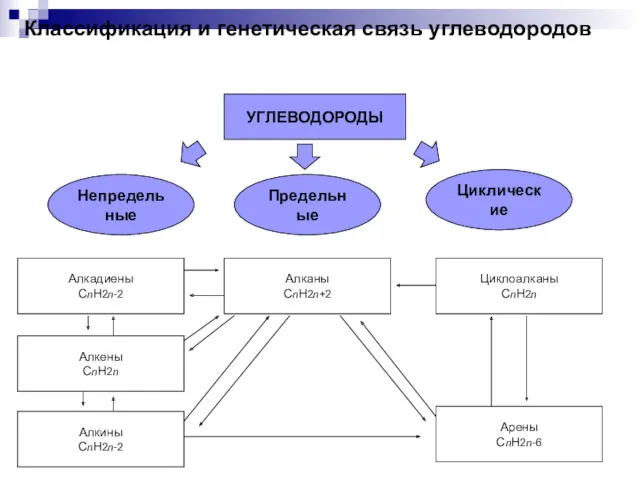 Классификация и генетическая связь углеводородов
Классификация и генетическая связь углеводородов Электрохимические накопители энергии
Электрохимические накопители энергии Таблицы. Определение характера оксидов
Таблицы. Определение характера оксидов Строение атома
Строение атома Магматические породы и постмагматические процессы
Магматические породы и постмагматические процессы Распространение водорода в природе. Получение в лаболатории
Распространение водорода в природе. Получение в лаболатории Кислородсодержащие соединения серы
Кислородсодержащие соединения серы Бытовые химические товары. Особенности упаковки, маркировки товаров бытовой химии
Бытовые химические товары. Особенности упаковки, маркировки товаров бытовой химии Узагальнення й систематизація знань з теми Початкові хімічні поняття
Узагальнення й систематизація знань з теми Початкові хімічні поняття Химиялық элемент алюминий
Химиялық элемент алюминий Полимеры, бумага
Полимеры, бумага Химическая кинетика. Тема 2.2
Химическая кинетика. Тема 2.2 Алкадиены
Алкадиены Метод электронного баланса для уравнивания окислительно-восстановительных реакций
Метод электронного баланса для уравнивания окислительно-восстановительных реакций Молекулярно-массовые характеристики высокомолекулярных соединений
Молекулярно-массовые характеристики высокомолекулярных соединений Правила ДСС
Правила ДСС Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Электронный помощник по химии 8 класс
Электронный помощник по химии 8 класс Дисперсные системы. (Лекция 6)
Дисперсные системы. (Лекция 6) Химия. D-элементтер
Химия. D-элементтер Аминокилоты. Свойства
Аминокилоты. Свойства