Содержание
- 2. ОБЩИЕ ПОНЯТИЯ ЭЛЕКТРОННЫЕ СЛОИ СТРОЕНИЕ АТОМА порядок заполнения ПЕРИОДИЧЕСКИЙ ЗАКОН Д.И. Менделеева провал электрона РАДИУС АТОМА
- 4. периодическая система элементов Д.И. Менделеева (длиннопериодная форма)
- 5. периодическая система элементов Д.И. Менделеева (полностью развернутая форма)
- 6. Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их свойствах, строении и
- 7. СТРОЕНИЕ АТОМА Атом состоит из ядра и находящихся около ядра электронов. Таким образом, можно сделать следующие
- 8. Атом Li Li находится во 2-м периоде IА группе, имеет № п/п = 3 и Ar
- 9. металлы – всегда отдают электроны неметаллам неметаллы – всегда берут электроны у металлов правило октета каждый
- 10. ЭЛЕКТРОННЫЕ СЛОИ Электроны в атоме расположены в строго определенном порядке, на электронных слоях (энергетических уровнях). Число
- 11. 4 3 2 1 4 3 2 1 электронно-графическая форма записи ПОРЯДОК ЗАПОЛНЕНИЯ
- 12. 4 3 2 1 7 6 5 Е ОБЩИЙ ПОРЯДОК ЗАПОЛНЕНИЯ СОГЛАСНО ЭНЕРГИИ ЭЛЕКТРОНА 1s2 2s2
- 13. 4 3 2 1 4 3 2 1 ПРОВАЛ (ПРОСКОК) ЭЛЕКТРОНА
- 14. 2 1 2 1 Валентность – число связей, которые образует атом хим. элемента с др. атомами.
- 15. 1 2 2 1 ОБМЕННЫЙ МЕХАНИЗМ ОБРАЗОВАНИЯ КОВАЛЕНТНОЙ СВЯЗИ – ОБОБЩЕСТВЛЕНИЕ НЕСПАРЕННЫХ ЭЛЕКТРОНОВ ОТДЕЛЬНЫХ АТОМОВ В
- 16. ЗАДАНИЕ Укажите заряд ядра, число протонов, нейтронов и электронов, число электронных слоёв и электронов на них.
- 17. Электроотрицательность (эо) – способность атома хим. элемента «стягивать» на себя общие с другими элементами электронные пары.
- 18. ХИМИЧЕСКАЯ СВЯЗЬ внутримолекулярная химическая связь – электростатическое взаимодействие между электро- нами и ядрами, приводящее к образованию
- 19. – тип ковалентной связи, где один из атомов является донором электронной пары, а другой атом является
- 20. также донорно-акцепторная связь реализуется в следующих соединениях: NH3 + H+ = NH4+ HCl Cl– H+ =
- 21. H + ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ ОБРАЗОВАНИЯ КОВАЛЕНТНОЙ СВЯЗИ – ОБЪЕДИНЕНИЕ СВОБОДНОЙ ОРБИТАЛИ ОДНОГО АТОМА С ОРБИТАЛЬЮ ДРУГОГО
- 22. H2O NH3 водородная – хим. связь, которая образуется между полярными молекулами в результате притяжения разноименных зарядов,
- 23. СТЕПЕНЬ ОКИСЛЕНИЯ (со) – условный заряд на атоме элемента при допущении, что все связи в молекуле
- 24. СОСТОЯНИЕ ВЕЩЕСТВА – имеют четкую упорядоченную структуру – не имеют четкой упорядоченной структуры кристаллическая решетка атомная
- 25. АЛЛОТРОПИЯ Аллотро́пия (от др.-греч. ἄλλος — «другой», τρόπος — «поворот, свойство») — существование двух и более
- 26. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ УГЛЕРОДА
- 27. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ФОСФОРА
- 28. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ АЛЛОТРОПНЫЕ МОДИФИКАЦИИ СЕРЫ
- 29. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ОЛОВА Олово существует в трех аллотропных формах: серое олово (α-олово), белое олово (β-олово) и
- 30. ЗАДАНИЯ НА ДОМ а) P и Br б) Fe и Cl ответьте на вопрос: почему молекулярный
- 31. УСПЕХОВ В ОБУЧЕНИИ !!! следите за новостями, акциями и обновлениями в нашей группе вконтакте: #_химия_на_сто https://vk.com/chem_na_100
- 32. ДОПОЛНИТЕЛЬНЫЕ СЛАЙДЫ
- 33. ОТНОСИТЕЛЬНАЯ ЭО АТОМОВ ПО ПОЛИНГУ
- 34. СТЕПЕНЬ ПОЛЯРНОСТИ СВЯЗИ
- 35. СВОЙСТВА КОВАЛЕНТНОЙ СВЯЗИ 1. направленность – определяет валентный угол между связями и характеризует химическое строение веществ.
- 36. ХАРАКТЕРИСТИКИ КОВАЛЕНТНОЙ СВЯЗИ 1. кратность – число общих электронных пар между двумя атомами. 2. длина –
- 37. ГАЛОГЕНЫ элементы VII группы главной подгруппы
- 38. ПНИКТОГЕНЫ элементы V группы главной подгруппы
- 40. Скачать презентацию
 Инструментальные методы исследования органических веществ
Инструментальные методы исследования органических веществ Алканы. Общая характеристика, гомологический ряд, номенклатура, изомерия. Методы синтеза
Алканы. Общая характеристика, гомологический ряд, номенклатура, изомерия. Методы синтеза Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів
Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів Электролитическая диссоциация
Электролитическая диссоциация Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Фенолы
Фенолы Массовая доля компонента вещества в смеси
Массовая доля компонента вещества в смеси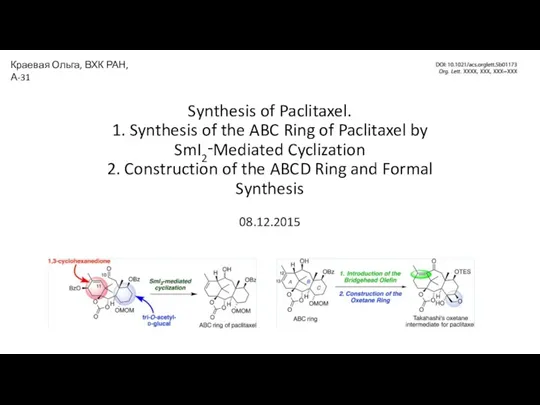 Synthesis of Paclitaxel
Synthesis of Paclitaxel Карбонаты
Карбонаты Углерод. Аллотропные состояния углерода
Углерод. Аллотропные состояния углерода Соли. Классификация и свойства солей
Соли. Классификация и свойства солей Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Химические свойства металлов
Химические свойства металлов Растворы и растворители
Растворы и растворители Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Гірські породи
Гірські породи Химические волокна (7 класс)
Химические волокна (7 класс) Равновесные электрохимические системы
Равновесные электрохимические системы Синтетические каучуки и их применение
Синтетические каучуки и их применение Биологически важные окислительно-восстановительные реакции органических соединений
Биологически важные окислительно-восстановительные реакции органических соединений Кристаллы и минералы
Кристаллы и минералы Кислород и его свойства
Кислород и его свойства Спектроскопия лазерных кристаллов
Спектроскопия лазерных кристаллов Подготовка к ГИА. В1. Периодический закон Д.И. Менделеева
Подготовка к ГИА. В1. Периодический закон Д.И. Менделеева Электрохимическая система
Электрохимическая система Ядовитые минералы
Ядовитые минералы Галогенопроизводные углеводородов (3)
Галогенопроизводные углеводородов (3) Барий. Щелочноземельные металлы
Барий. Щелочноземельные металлы