Содержание
- 2. Тест – экспресс 1) Электронная конфигурация атома углерода? 2) Разновидности простого вещества, образованные одним и тем
- 3. ОТВЕТЫ 1) Аллотропные видоизменения 2) 1s22s22p 3) Четыре 4) Метан СН4, силан SiH4 5) ЭО2 6)
- 4. Фокус-покус для народа: Стоит лишь подуть сквозь воду, Как она легко-легко Превратиться в молоко! СО2 +
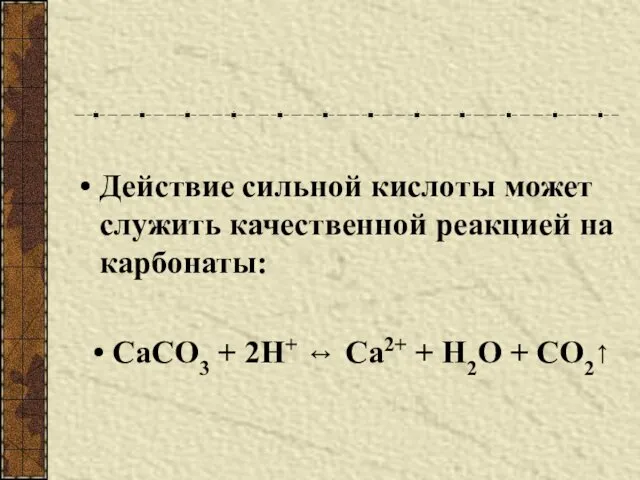
- 5. Действие сильной кислоты может служить качественной реакцией на карбонаты: СаСО3 + 2Н+ ↔ Са2+ + Н2О
- 6. Как можно собрать СО2 М(воздуха)=29, т.е. СО2 тяжелее воздуха Метод вытеснения воды невозможен из-за протекания реакции:
- 7. Угольная кислота диссоциирует ступенчато: 1.H2CO3 ↔ Н+ + HCO3- 2. HCO3- ↔ Н+ + CO32-
- 8. Соли угольной кислоты ↓ ↓ Нормальные Кислые (карбонаты) (гидрокарбонаты)
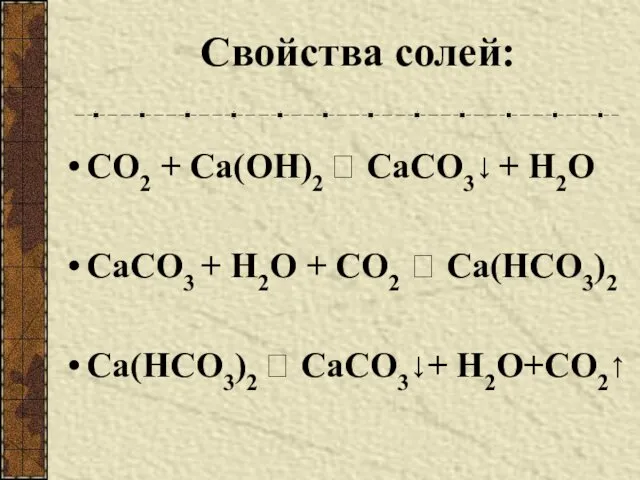
- 9. Свойства солей: СО2 + Са(ОН)2 ? СаСО3↓ + Н2О СаСО3 + Н2О + СО2 ? Са(НСО3)2
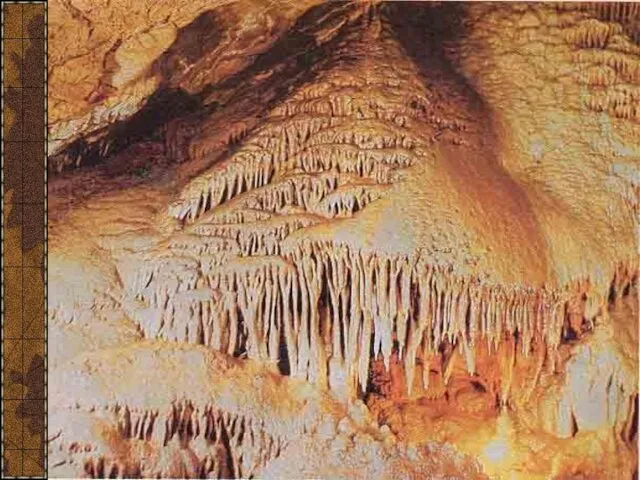
- 10. Красная пещера, или Кизил-Коба, самая крупная из 800 пещер Крыма. Она расположена в 3,5 км от
- 11. Сталагмиты
- 12. Сталактит «Пузатый»
- 13. Сталактит «Огненный»
- 17. Изучением карстовых пещер занимается наука – спелеология
- 18. Соли угольной кислоты: Мрамор, известняк, мел – СаСО3 На земле живут три брата Из семейства Карбонатов.
- 19. Доломит CaCO3. MgCO3 – обычно содержит глины и известняки, применяется для получения извести, солей магния, как
- 20. Сидерит FeCO3 – минерал бурого цвета, служит рудой для получения железа. Кальцинированная сода Na2CO3 – белый
- 21. Презентация разработки темы в курсе 9 класса. Подготовила учитель химии ОГРИНА СВЕТЛАНА ЮРЬЕВНА
- 23. Скачать презентацию
















 Химия в быту
Химия в быту Химия 8 класс. Введение в химию
Химия 8 класс. Введение в химию Полиэтилен - термопластичный полимер этилена
Полиэтилен - термопластичный полимер этилена Органическая химия. Олигосахариды. Полисахариды
Органическая химия. Олигосахариды. Полисахариды Химия аминокислот, пептидов и белков
Химия аминокислот, пептидов и белков Химические свойства металлов
Химические свойства металлов Эквивалент. Закон эквивалентов
Эквивалент. Закон эквивалентов Монокристаллы InSb. Свойства, выращивание, применение
Монокристаллы InSb. Свойства, выращивание, применение Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Моносахариды, дисахариды
Моносахариды, дисахариды Металлы. Металлы главной подгруппы
Металлы. Металлы главной подгруппы Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс
Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс Общие свойства металлов
Общие свойства металлов Газы, применяемые при сварке
Газы, применяемые при сварке Теория электролитической диссоциации
Теория электролитической диссоциации Соединения углерода
Соединения углерода Предмет органической химии
Предмет органической химии Фазовые равновесия. Физическая и коллоидная химия
Фазовые равновесия. Физическая и коллоидная химия Вуглеводи. Загальна характеристика вуглеводів, представники
Вуглеводи. Загальна характеристика вуглеводів, представники Алкадиены (диеновые углеводороды)
Алкадиены (диеновые углеводороды) Общие понятия неорганической химии. Химические свойства основных классов неорганических веществ. Лекция 3
Общие понятия неорганической химии. Химические свойства основных классов неорганических веществ. Лекция 3 Полибутадиен
Полибутадиен Биополимеры
Биополимеры Зелёная химия
Зелёная химия Растворы. Способы выражения концентрации раствора
Растворы. Способы выражения концентрации раствора Буферные растворы. Граф структуры. Теория электрической диссоциации. Химическое равновесие
Буферные растворы. Граф структуры. Теория электрической диссоциации. Химическое равновесие Кислородные соединения азота
Кислородные соединения азота Показатели жесткости воды
Показатели жесткости воды