Содержание
- 2. F:\videoplayback (online-video-cutter.com).mp4
- 3. Металлы главной подгруппы I группы (щелочные металлы) литий Li натрий Nа калий К рубидий Rb цезий
- 4. Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании. Металлы обладают электропроводностью и теплопроводностью.
- 5. Объясните «нестандартное поведение» натрия! Почему металл хранят под слоем керосина? Какое вещество сразу образует белый налет
- 6. План характеристики щелочных металлов: I. Атомы Положение атомов в ПСХЭ Особенности строения атомов Возможные степени окисления
- 7. Задания для самостоятельной работы: 1. Определи положение щелочных металлов в периодической системе химических элементов Д.И.Менделеева. Запиши
- 8. План характеристики щелочных металлов: I. Атомы Положение атомов в ПСХЭ Особенности строения атомов Возможные степени окисления
- 10. СТРОЕНИЕ АТОМОВ На внешнем энергетическом уровне атомы этих элементов содержат по одному электрону. Они легко отдают
- 11. ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
- 12. Серебристо-белые, кроме цезия (золотистый), мягкие (режутся ножом), с характерным блеском на свежесрезанной поверхности, Все они легкие
- 13. Химические свойства Все щелочные металлы чрезвычайно активны, во всех химических реакциях проявляют восстановительные свойства, отдают свой
- 14. Химические свойства
- 15. Щелочные металлы легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность: оксид образует только литий:
- 16. Взаимодействие с водородом, серой, фосфором, углеродом, кремнием протекает при нагревании: с водородом образуются гидриды: 2Na +
- 17. Все щелочные металлы реагируют с водой, литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется,
- 18. Щелочные металлы способны реагировать с разбавленными кислотами , однако реакция будет протекать неоднозначно… Взаимодействие с кислотами
- 19. Электролиз расплавов соединений щелочных металлов: 2МеCl = 2Ме + Cl2 4МеOH = 4Ме + 2Н2О +
- 20. Объясните «нестандартное поведение» металла! Почему металл хранят под слоем керосина? Какое вещество сразу образует белый налет
- 21. ВОПРОСЫ: От лития к францию у атомов щелочных металлов увеличивается Более сильным восстановителем, чем К будет
- 22. Решим задачу: Какой объем водорода выделится при взаимодействии 2,3 г натрия с водой ?
- 23. Рефлексия Железная логика Стальной характер Золотая голова Медный лоб
- 24. Домашнее задание. П.30, упражнения: 1. Исправить ошибки: Na + O2 ? Na2O K + H2O ?
- 25. Применение щелочных металлов Литий Для получения трития Получение сплавов для подшипников Восстановитель в органическом синтезе Химические
- 26. Применение щелочных металлов
- 27. Применение щелочных металлов Калий В гальванотехнике Калийные удобрения Для получения перекиси калия Катализатор Термическое получение металлов
- 28. Применение щелочных металлов
- 29. Применение щелочных металлов
- 30. Литий был открыт в 1817 г. А. Арфведсоном в минерале петалите. Берцелиус предложил назвать ее литионом
- 31. Натрий (от нем. Natrium от древнеевр. neter — бурлящее вещество. В 1807 г. Г.Дэви получил свободный
- 32. Калий (англ. Potassium, франц. Potassium, нем. Kalium) открыл в 1807 г. Г.Дэви, он именовал новый металл
- 33. При спектроскопическом анализе минерала лепидолита обнаружились две новые красные линии в красной части спектра. Эти линии
- 34. Цезий - первый элемент, открытый с помощью спектрального анализа. Р.Бунзен и Г.Кирхгофф обнаружили спектральные линии нового
- 35. Элемент был предсказан Д.И.Менделеевым (как Эка-цезий), и был открыт в 1939 г. Маргаритой Пере, сотрудницей Института
- 36. Галит
- 37. Природные соединения калия Сильвин
- 38. Природные соединения калия Карналит
- 39. Щелочные металлы способны реагировать с разбавленными кислотами с выделением водорода, однако реакция будет протекать неоднозначно, поскольку
- 40. Взаимодействие с кислотами Me+H2SO4(к)=Me2SO4+H2S+H2O
- 41. Химические свойства 2Na + Cl2 = 2NaCl (в атмосфере F2 и Cl2 щелочные Me самовоспламеняются) 4Li
- 42. Качественное определение щелочных металлов Li+ Na+ K+ Для распознавания соединений щелочных металлов по окраске пламени исследуемое
- 43. ОКСИДЫ ЩЕЛОЧНЫХ МЕТАЛЛОВ-ОСНОВНЫЕ Для получения оксидов натрия и калия нагревают смеси гидроксида, пероксида или надпероксида с
- 44. 1. Оксиды щелочных металлов обладают всеми свойствами, присущими основным оксидам: они реагируют с водой, кислотными и
- 45. Гидроксид натрия NаОН в технике известен под названиями едкий натр, каустическая сода, каустик. Техническое название гидроксида
- 46. Соли щелочных металлов — твердые кристаллические вещества ионного строения. . Nа2СO3 — карбонат натрия, образует кристаллогидрат
- 48. NаСl — хлорид натрия, галлит, или поваренная соль, эта соль вам хорошо известна из курса прошлого
- 49. Физические свойства щелочных металлов Щелочные металлы - серебристо–белые вещества, за исключением цезия - серебристо-желтого цвета, с
- 51. Скачать презентацию
















































 Растворимость, ее зависимость от разных факторов. Насыщенные и ненасыщенные растворы. Физико-химическая сущность растворения
Растворимость, ее зависимость от разных факторов. Насыщенные и ненасыщенные растворы. Физико-химическая сущность растворения Керамика на основе Al2O3
Керамика на основе Al2O3 Минералы и горные породы
Минералы и горные породы Алкены. Строение, изомерия, номенклатура
Алкены. Строение, изомерия, номенклатура Вещества молекулярного и немолекулярного строения. Типы кристаллических решеток
Вещества молекулярного и немолекулярного строения. Типы кристаллических решеток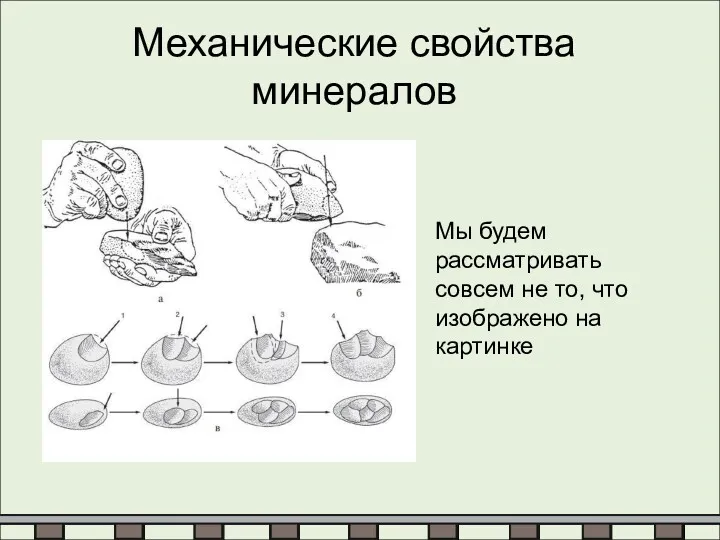 Механические свойства минералов
Механические свойства минералов Аурум
Аурум Объёмная доля компонента смеси
Объёмная доля компонента смеси Химическая связь
Химическая связь Магматические горные породы
Магматические горные породы Мембранный транспорт ионов: электродиффузионная теория
Мембранный транспорт ионов: электродиффузионная теория Свойства неорганических веществ. (Задание 37. ЕГЭ по химии)
Свойства неорганических веществ. (Задание 37. ЕГЭ по химии) Аффинаж солей урана. Получение оксидов урана
Аффинаж солей урана. Получение оксидов урана Растворение. Растворы.
Растворение. Растворы. Свойства алкадиенов и их получение
Свойства алкадиенов и их получение Вода – основа жизни на Земле
Вода – основа жизни на Земле Природный газ и нефть
Природный газ и нефть Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Применение спиртов
Применение спиртов Химия. Интересные факты. Как Менделеев открыл периодический закон?
Химия. Интересные факты. Как Менделеев открыл периодический закон? Закономерности химических элементов ряда Фибоначчи
Закономерности химических элементов ряда Фибоначчи Серная кислота и её свойства
Серная кислота и её свойства Минералы и их основные морфологические характеристики
Минералы и их основные морфологические характеристики Летучие яды. Токсичные газы
Летучие яды. Токсичные газы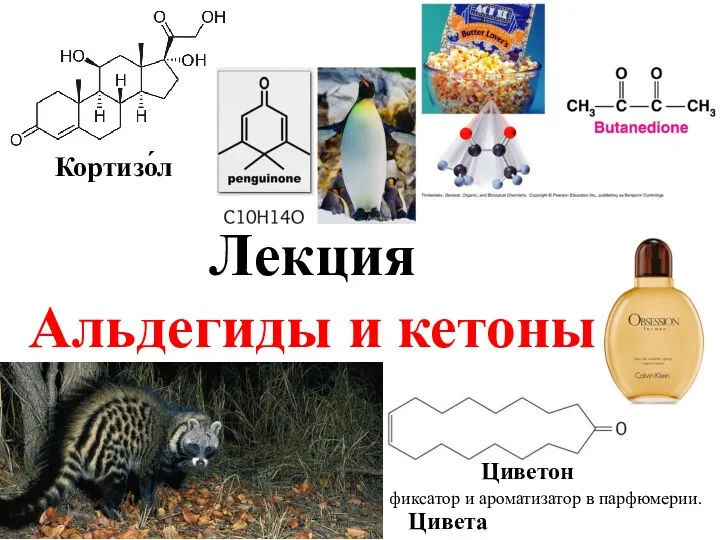 Альдегиды и кетоны. Циветон
Альдегиды и кетоны. Циветон Чисті речовини і суміші
Чисті речовини і суміші Алюминий и его соединения. Характеристика химического элемента: 3-й период, 3-я А подгруппа
Алюминий и его соединения. Характеристика химического элемента: 3-й период, 3-я А подгруппа Природный и синтетический каучуки. Резина
Природный и синтетический каучуки. Резина