Содержание
- 2. Молекулярные вещества Молекулярные вещества — это вещества, мельчайшими структурными частицами которых являются молекулы Молекулы — наименьшая
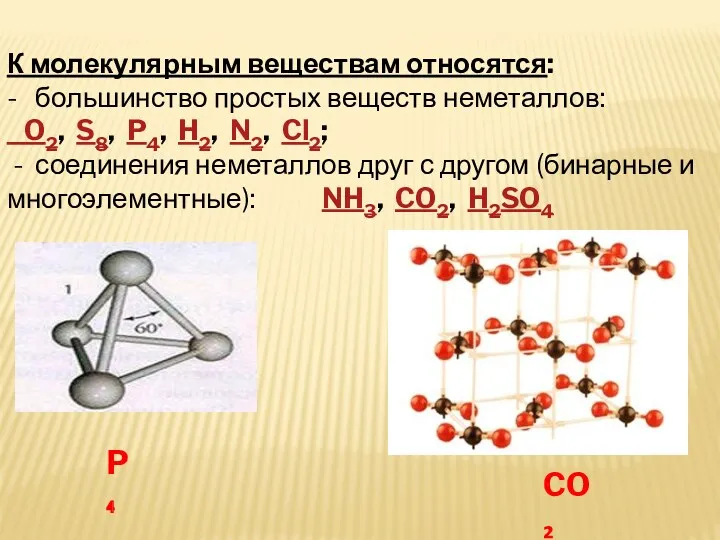
- 3. К молекулярным веществам относятся: - большинство простых веществ неметаллов: O2, S8, P4, H2, N2, Cl2; -
- 5. Немолекулярные вещества — это вещества, мельчайшими структурными частицами которых являются атомы или ионы. Ион — это
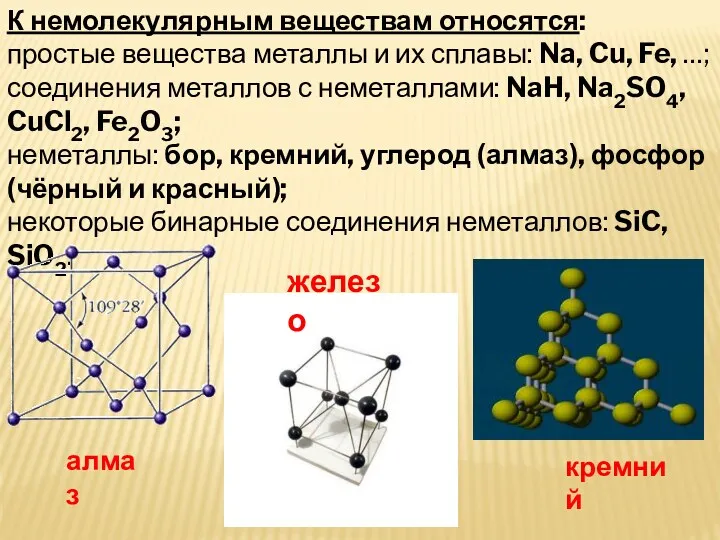
- 6. К немолекулярным веществам относятся: простые вещества металлы и их сплавы: Na, Cu, Fe, …; соединения металлов
- 7. Кристаллическая структура — такая совокупность атомов, в которой с каждой точкой кристаллической решетки связана определенная группа
- 8. Кристаллические решетки
- 9. ВЕЩЕСТВА С АТОМНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙ Состоят из атомов, связанных друг с другом в бесконечный трехмерный каркас.
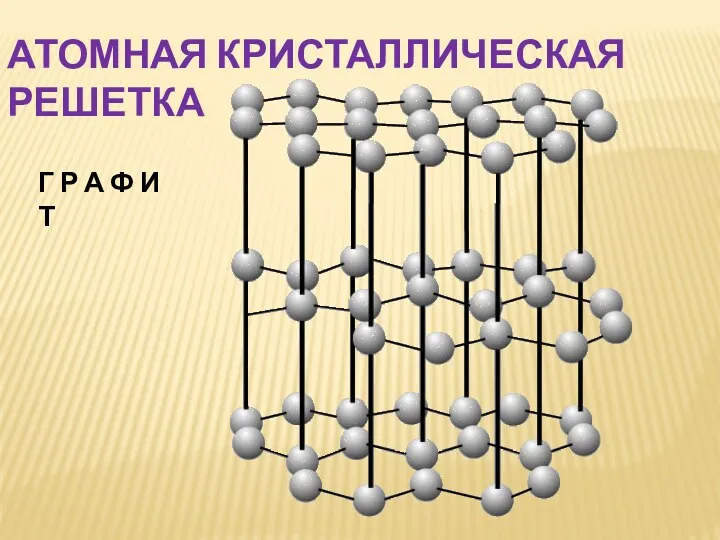
- 10. АТОМНАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Г Р А Ф И Т
- 11. ВЕЩЕСТВА С МОЛЕКУЛЯРНОЙ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКОЙ В узлах находятся молекулы, которые удерживаются слабыми силами межмолекулярного притяжения. СВОЙСТВА:
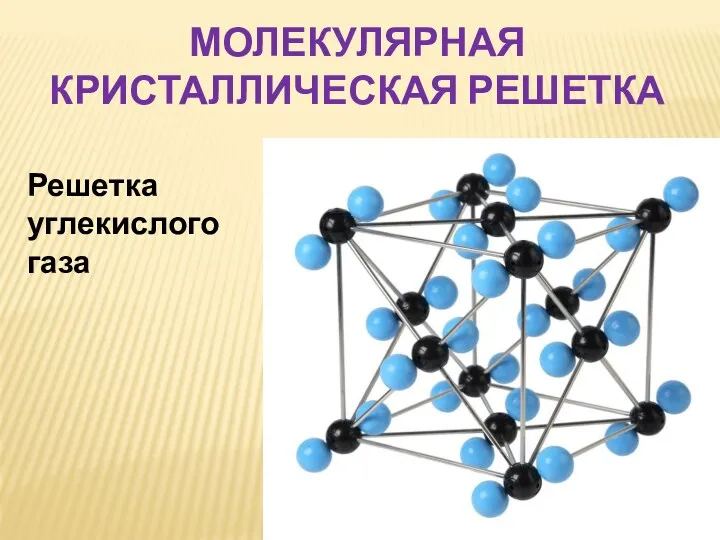
- 12. Решетка углекислого газа МОЛЕКУЛЯРНАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
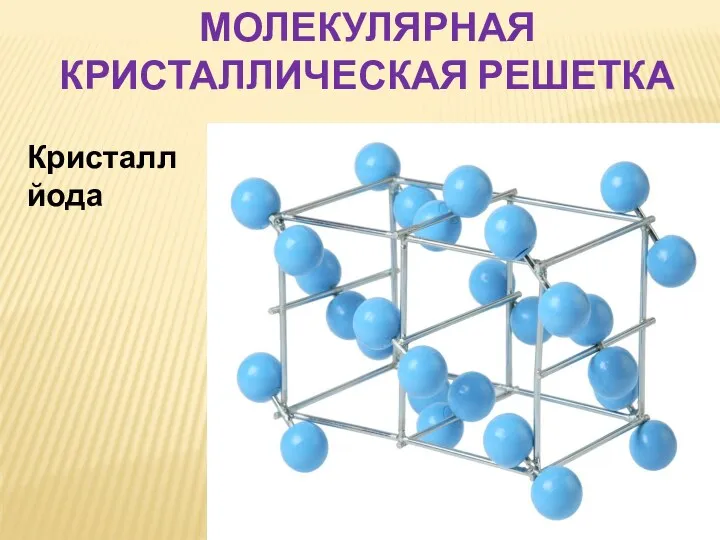
- 13. МОЛЕКУЛЯРНАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Кристалл йода
- 14. ИОННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА СВОЙСТВА: твердые, прочные, но хрупкие высокие температуры плавления при растворении в воде распадаются
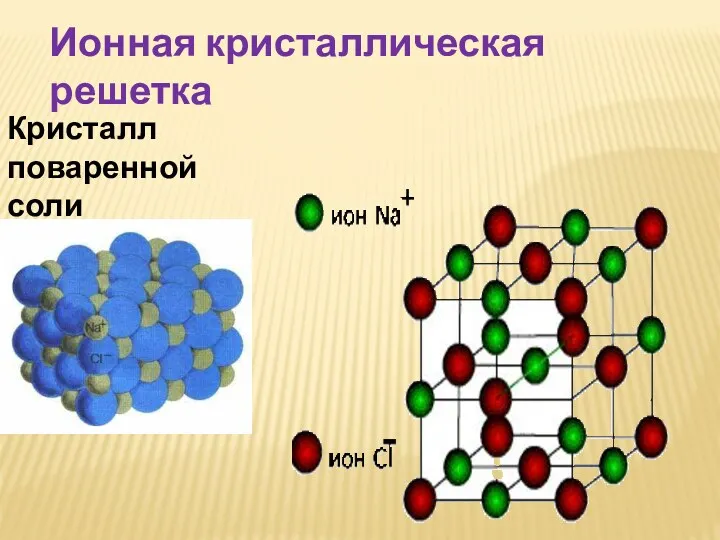
- 15. Ионная кристаллическая решетка Кристалл поваренной соли
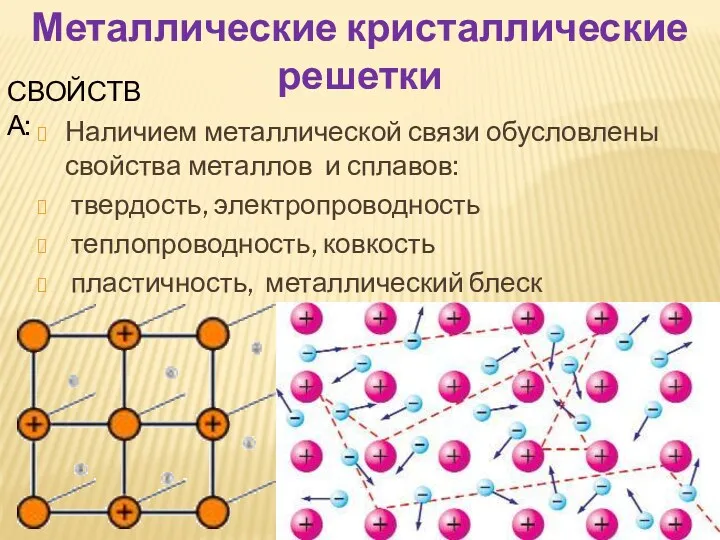
- 16. Наличием металлической связи обусловлены свойства металлов и сплавов: твердость, электропроводность теплопроводность, ковкость пластичность, металлический блеск Металлические
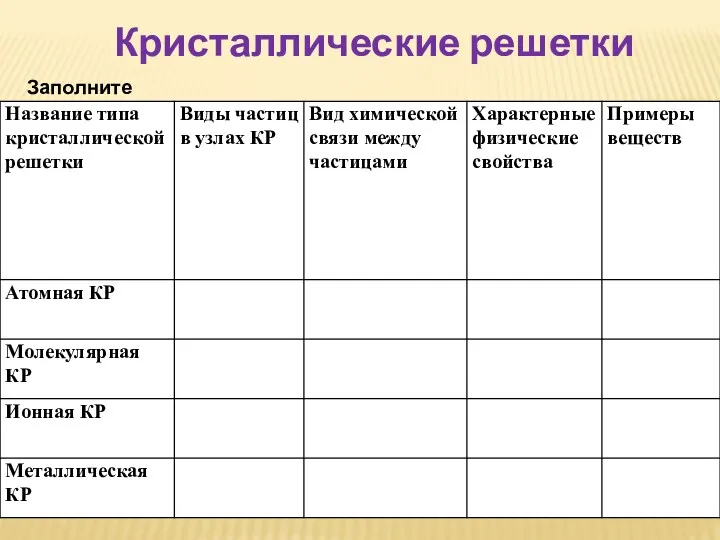
- 17. Кристаллические решетки Заполните таблицу:
- 18. К веществам молекулярного строения относится: а) Si б) SiO₂ в) C г) CO₂ Твердое вещество, раствор
- 20. Скачать презентацию









 Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Магия кристаллов
Магия кристаллов Пластмаси. Види пластмас. (11 клас)
Пластмаси. Види пластмас. (11 клас) Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ Производство полимеров
Производство полимеров Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте
Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте Геохимия гидротермального процесса
Геохимия гидротермального процесса Защита металлоконструкций от коррозии
Защита металлоконструкций от коррозии Химия металлов: влияние металлов на организм человека
Химия металлов: влияние металлов на организм человека Типы химических реакций
Типы химических реакций Органическая химия
Органическая химия Химия титанорганических соединений
Химия титанорганических соединений Соли и их свойства
Соли и их свойства Соединения серы
Соединения серы Химическая связь
Химическая связь Нанотехнологии в школьном образовании. Семинар учителей химии
Нанотехнологии в школьном образовании. Семинар учителей химии Генетическая связь между классами веществ
Генетическая связь между классами веществ Беломорская соль, проектная работа
Беломорская соль, проектная работа Химические свойства спиртов
Химические свойства спиртов Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока
Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Значение органической химии в жизни человека
Значение органической химии в жизни человека Классификация химических реакций
Классификация химических реакций Полезные геологические химические соединения. Получение меди из малахита
Полезные геологические химические соединения. Получение меди из малахита Механическая смесь и растворы
Механическая смесь и растворы Общая характеристика реакций органических соединений. Кислотные и основные свойства органических соединений
Общая характеристика реакций органических соединений. Кислотные и основные свойства органических соединений Применение солей
Применение солей Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс