Содержание
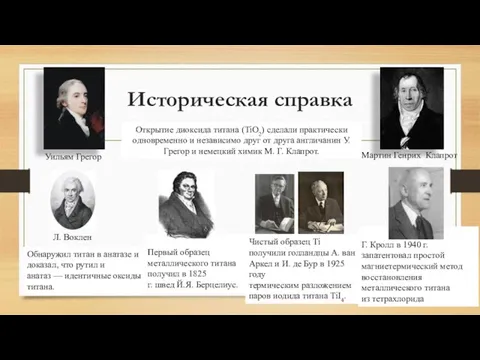
- 2. Чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 году термическим
- 3. Порядковый номер: 22 IV Б – группа Период 4 Элемент d — семейства Относительная атомная масса
- 4. 1s22s22p63s23p63d24s2 Строение электронной оболочки атома титана
- 5. Физические свойства Лёгкий прочный металл серебристо-белого цвета; Существует в виде двух аллотропических модификаций: ниже температуры 882,5
- 6. Коррозионные свойства
- 7. Нахождение в природе
- 8. Тi образует органические производные 2ух основных типов: 1-тип производных, в которых атом титана непосредственно связан с
- 9. Алкилгалогениды титана(IV) TiXnR4-n R – метил, этил, бутил X – Cl, Br, I Также могут быть
- 10. Метилтрихлорид титана TiCl3(CH3) темно-фиолетовые кристаллы растворим в углеводородах и их галогенпроизводных устойчив в отсутствии влаги и
- 11. Этилтрихлорид титана TiCl3(C2H5) красноватая жидкость распадающуюся за 24 ч при 20 °С Пропилтрихлорид титана TiCl3(С3Н7) и
- 12. Диалкилдигалогениды титана
- 13. Диметилдихлорид и диэтилдихлорид титана ТiСl2(СН3)2 черно-фиолетовые кристаллы растворимые в углеводородах (гексан) растворы окрашены в желтый цвет
- 14. Триалкилмоногалогениды титана
- 15. Тетраметилтитан Ti(CH3)4 Блестящие желтые иглообразные кристаллы Устойчив лишь при низких температурах при температуре выше 0° С
- 16. Тетраэтилтитан и тетрапропилтитан Ti(C2H5)4 Ti(C3H7)4 оранжево-желтые кристаллы чрезвычайно неустойчив
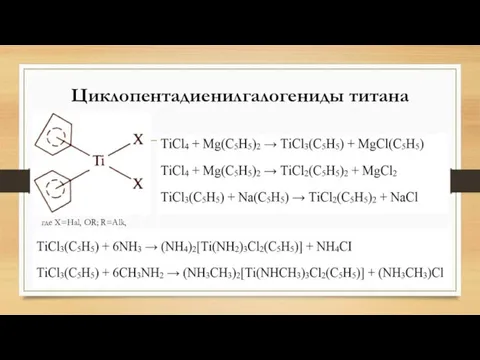
- 17. Циклопентадиенилгалогениды титана где X=Hal, OR; R=Alk, Аг
- 18. Диметилдициклопентадиенилтитан Тi(С5Н5)2(СН3)2 Оранжевые иглообразные кристаллы В темноте устойчив к действию кислорода и воды на свету быстро
- 19. Дициклопентадиенилтитан Чрезвычайно легко окисляется кислородом воздуха С концентрированной соляной кислотой образует дициклопентадиенилдихлорид титана Труднорастворим в жидких
- 20. Катализаторы Циглера — Натта
- 21. Производные ортотитановой кислоты В качестве производных ортотитановой кислоты выступают ее эфиры. Взаимодействие алкоголятов спиртов с тетрахлоридом
- 22. Получение в промышленности В промышленности получают при взаимодействии тетрахлорида титана с органическими спиртами в присутствии акцептора
- 23. Эфиры ортотитановой кислоты способны к реакции переэтерификации: Тетрахлорид титана реагирует с алкиленоксидами в среде органических растворителей:
- 24. Химические свойства Гидролиз эфиров ортотитановой кислоты: Комплекс распадается на спирт и оксиэфир, который выделить не удается,
- 25. Получение олигомерных ортотитанатов при помощи термической конденсации ортотитанов: Реакциями алкоголиза или переэтерификацией можно получать эфиры с
- 26. Реакции ортотитанатов с органическими кислотами или их ангидридами приводят к получению ацильных производных. Достаточно легко происходит
- 27. Внутренние комплексы титана (хелаты) Атом титана обладает способностью образовывать координационные связи с увеличением координационного числа до
- 28. Получение и химические свойства Ацетилацетон легко взаимодействует с ортоэфирами титана, образуя моно- и дизамещенные ацетилацетонатные производные:
- 29. Реакция между ацетилацетоном и тетрахлоридом титана дает трихлортитанацетилацетонат и дихлортитан-бис-(ацетилацетонат): Эти же соединения могут быть получены
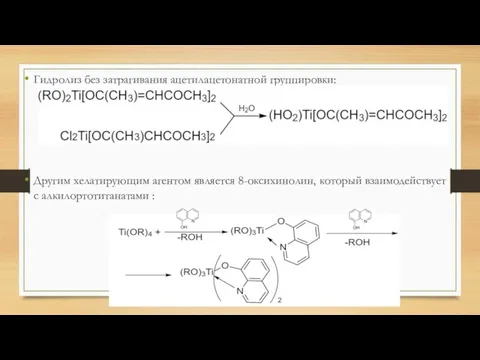
- 30. Гидролиз без затрагивания ацетилацетонатной группировки: Другим хелатирующим агентом является 8-оксихинолин, который взаимодействует с алкилортотитанатами :
- 31. Применение Эфиры ортотитановой кислоты могут катализировать полимеризацию некоторых непредельных органических соединений, а также реакции переэтерификации эфиров
- 32. Элементоорганические титансодержащие полимеры Полититаноорганооксаны В качестве исходных продуктов для получения титанорганических полимеров применяют соединения четырехвалентного титана.
- 33. При введении большего количества воды или при нагреве продуктов реакции происходит дальнейшее отщепление бутоксигрупп и поликонденсация
- 34. Свойства полимерных титанорганических соединений: Высокая химическая устойчивость Теплостойкость Хорошая адгезия к металлу и стеклу.
- 35. Полититаноорганосилоксаны Реакция гетерофункциональной конденсации При соконденсации α,ω-диорганодигидроксисилоксанов с такими тетрафункциональными соединениями, как тетрахлориды или тетраалкоксиды кремния,
- 36. Полученные тетрафункциональные крестообразные олигомеры имеют четыре равных по длине диорганосилоксановых фрагмента, содержащих концевые силанольные группы. Термической
- 37. Полититаноорганосилоксаны спироциклического строения Гетерофункциональная соконденсация ди- и тетрафункциональных мономеров может приводить и к образованию полимеров спироциклической
- 38. При гетерофункциональной конденсации тетрагидрокситетрафенилциклотетрасилоксана с тетрабутоксититаном, взятых в соотношении 2:1, было получено и выделено соединение со
- 39. Полититаноорганосилоксаны разветвленного строения Осуществлена реакция между α,ω-дигидроксидиметилсилоксанами и тетрабутоксититаном: Для получения полимера линейной структуры необходимо придерживаться
- 41. Скачать презентацию



































 Бензин. Производство бензина
Бензин. Производство бензина Types of chemical reactions
Types of chemical reactions соединения VI группы продвинутая версия
соединения VI группы продвинутая версия Азотсодержащие органические соединения
Азотсодержащие органические соединения Органическая химия. Лекция 13
Органическая химия. Лекция 13 Химическое равновесие. Смещение химического равновесия
Химическое равновесие. Смещение химического равновесия Современные положения теории А.М. Бутлерова
Современные положения теории А.М. Бутлерова Химические формулы. Относительная молекулярная масса
Химические формулы. Относительная молекулярная масса Изотопный обмен
Изотопный обмен Растворы. Вычисление массовой доли растворенного вещества в растворе. Урок для 8-го класса
Растворы. Вычисление массовой доли растворенного вещества в растворе. Урок для 8-го класса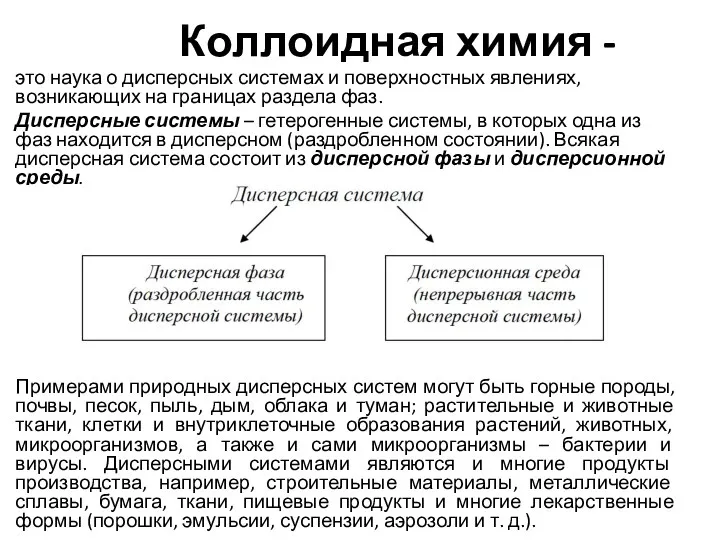 Коллоидная химия
Коллоидная химия Алкены. Этиленовые углеводороды, олефины
Алкены. Этиленовые углеводороды, олефины Nucleic acids
Nucleic acids Общая и медицинская химия
Общая и медицинская химия Создание косметических средств
Создание косметических средств Лекарственные средства из группы карбоновых кислот и их производных калия ацетат, кальция лактат, натрия цитрат
Лекарственные средства из группы карбоновых кислот и их производных калия ацетат, кальция лактат, натрия цитрат Алюминий и бор
Алюминий и бор Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Титриметрический анализ. (Лекция 22)
Титриметрический анализ. (Лекция 22) проект по биологииНаучно-исследовательская работа
проект по биологииНаучно-исследовательская работа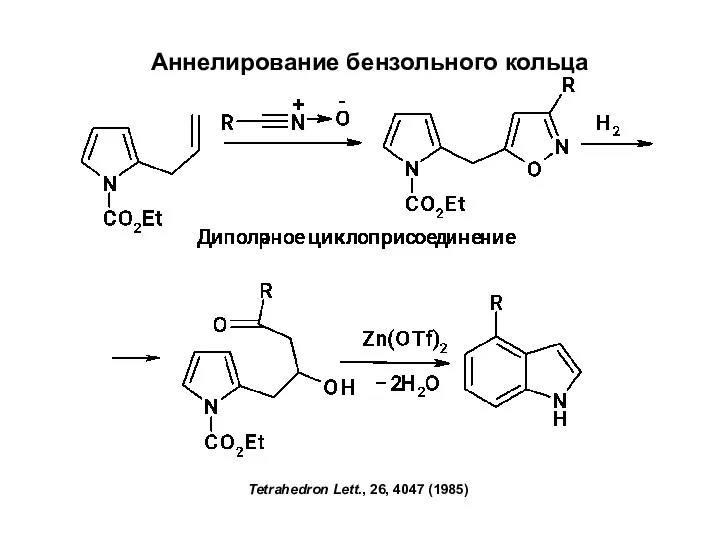 Аннелирование бензольного кольца
Аннелирование бензольного кольца Строение атома. Теории строения атома
Строение атома. Теории строения атома Анализ начальных участков изотерм адсорбции
Анализ начальных участков изотерм адсорбции Многоатомные спирты
Многоатомные спирты Щелочноземельные металлы. Химические свойства
Щелочноземельные металлы. Химические свойства Азот и его свойства
Азот и его свойства Нефть. Способы её переработки. Фракции нефти
Нефть. Способы её переработки. Фракции нефти Процесс электролиза
Процесс электролиза