Содержание
- 2. Аминокислоты – гетерофункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу – NH2 и карбоксильную группу
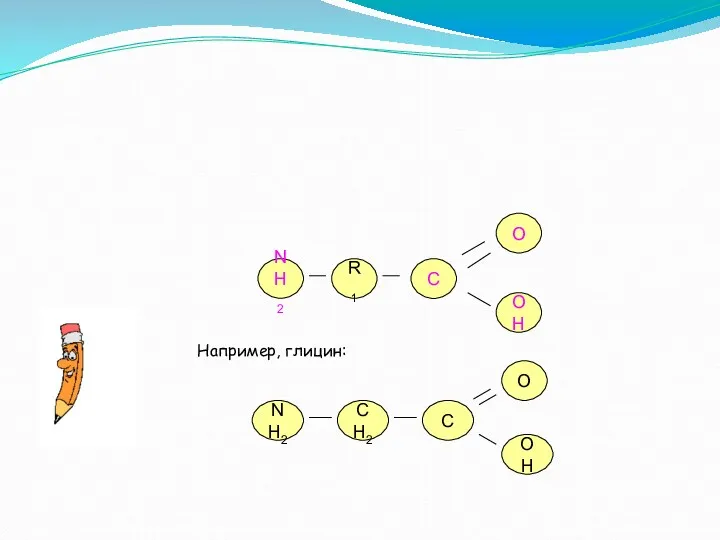
- 3. NH2 R1 C OH Например, глицин: NH2 OH C CH2 O O
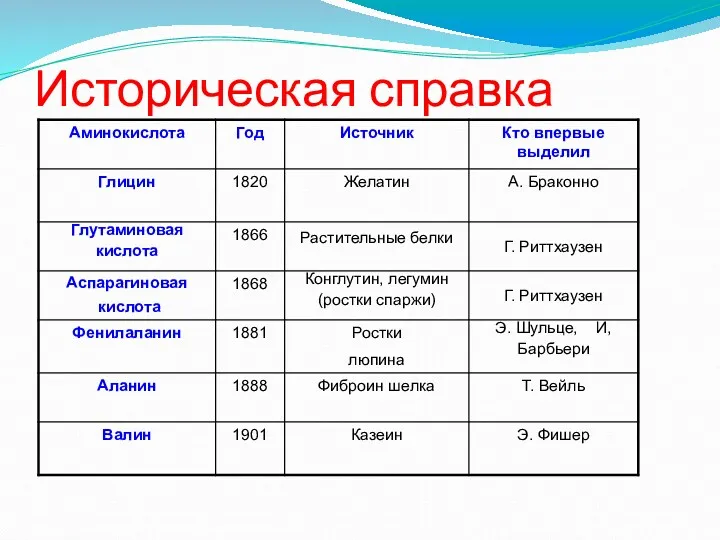
- 4. Историческая справка
- 5. Классификация По взаимному расположению функциональных групп: γ β α γ β α γ β α С
- 6. Классификация 2. По количеству функциональных групп : моноаминомонокарбоновые С – С – СООН | NH2 3-аминопропановая
- 7. Изомерия аминокислот Для аминокислот характерны следующие виды изомерии: а) углеродного скелета: СН3 – СН2– СН –
- 8. Изомерия аминокислот б) расположения функциональной группы : γ β α СН3 – СН2– СН- СООН α-
- 9. Физические свойства Аминокислоты: бесцветные кристаллические вещества сладкие на вкус хорошо растворяются в воде имеют температуру плавления
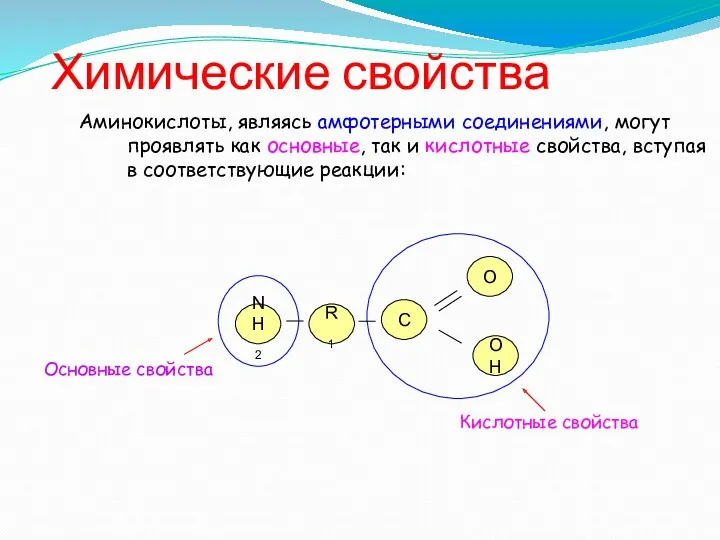
- 10. Химические свойства Аминокислоты, являясь амфотерными соединениями, могут проявлять как основные, так и кислотные свойства, вступая в
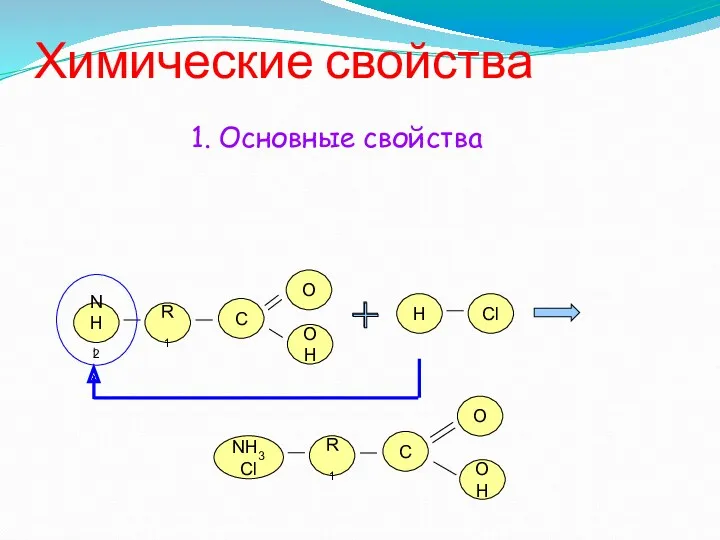
- 11. Химические свойства NH2 R1 О OH C 1. Основные свойства NH3Cl R1 О OH C H
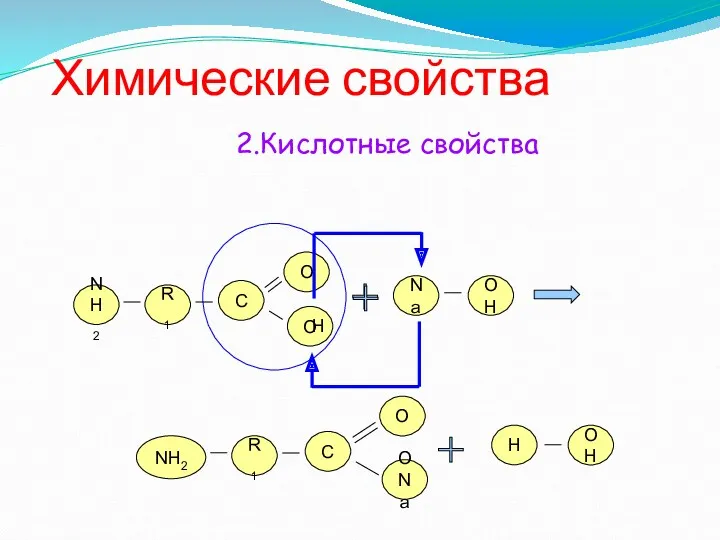
- 12. Химические свойства NH2 R1 О O C NH2 R1 О ONa C Na OH 2.Кислотные свойства
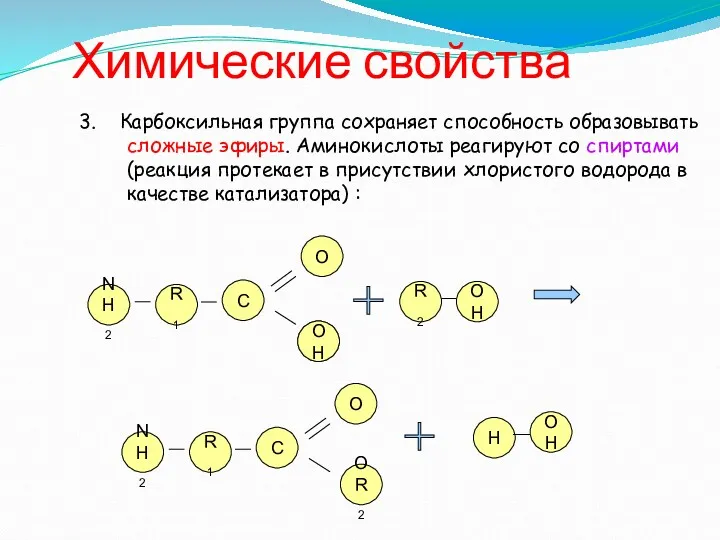
- 13. Химические свойства 3. Карбоксильная группа сохраняет способность образовывать сложные эфиры. Аминокислоты реагируют со спиртами (реакция протекает
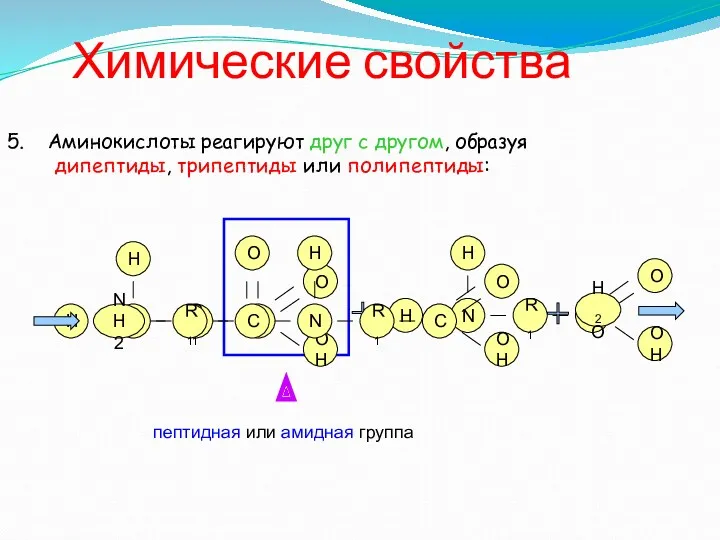
- 14. Химические свойства 5. Аминокислоты реагируют друг с другом, образуя дипептиды, трипептиды или полипептиды: N R1 C
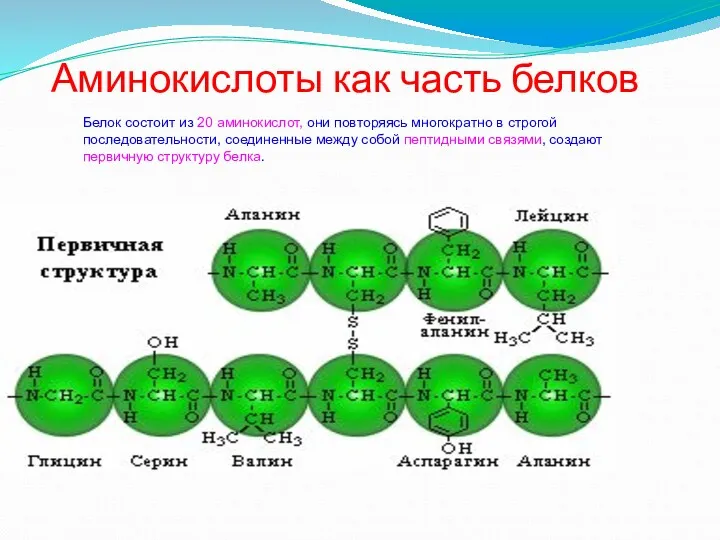
- 15. Аминокислоты как часть белков Белок состоит из 20 аминокислот, они повторяясь многократно в строгой последовательности, соединенные
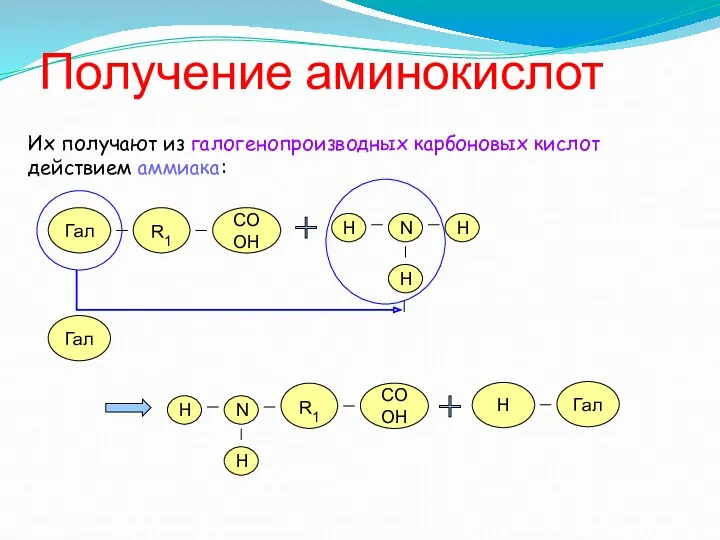
- 16. Получение аминокислот Их получают из галогенопроизводных карбоновых кислот действием аммиака: R1 Гал COOH H N H
- 17. Получение аминокислот в промышленности гидролизом белков. Смесь аминокислот обычно получают кислотным гидролизом белков.
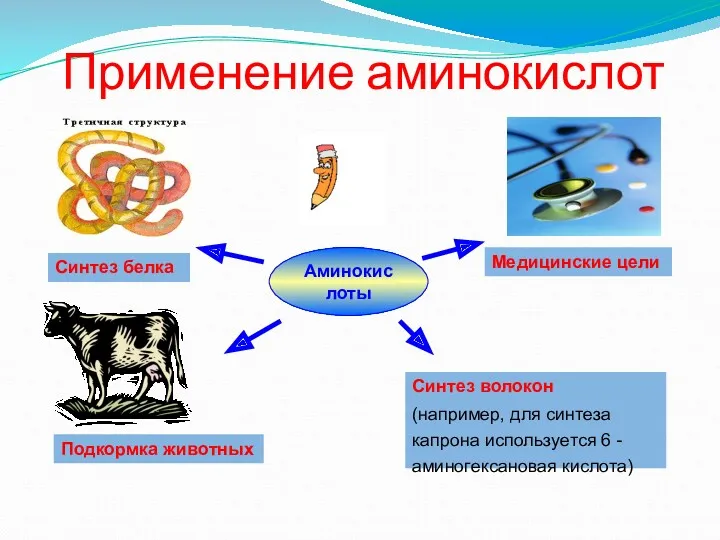
- 18. Применение аминокислот Аминокислоты Синтез белка Медицинские цели Подкормка животных Синтез волокон (например, для синтеза капрона используется
- 20. Скачать презентацию







 Натуральный и синтетический каучуки. Резина
Натуральный и синтетический каучуки. Резина Алкины — углеводороды, содержащие тройную связь между атомами углерода
Алкины — углеводороды, содержащие тройную связь между атомами углерода Проект узла регенерации растворителя уксусной кислоты производства терефталевой кислоты
Проект узла регенерации растворителя уксусной кислоты производства терефталевой кислоты Теория электролитической диссоциации
Теория электролитической диссоциации Свойства химических элементов и закономерность их изменения
Свойства химических элементов и закономерность их изменения Реакции ионного обмена. Теория химического строения органических соединений. 9 класс
Реакции ионного обмена. Теория химического строения органических соединений. 9 класс Валентность элементов. Определение валентности по формулам
Валентность элементов. Определение валентности по формулам Пластмаси та їх роль у сучасному виробництві
Пластмаси та їх роль у сучасному виробництві Биологически важные гетероциклы
Биологически важные гетероциклы Оксиды. Классификация. Получение. Свойства
Оксиды. Классификация. Получение. Свойства Средства гигиены
Средства гигиены Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Этот удивительный песок
Этот удивительный песок Заттардың агрегаттық күйі
Заттардың агрегаттық күйі Химия p-элементов. VI и VII группы главные подгруппы
Химия p-элементов. VI и VII группы главные подгруппы Классификация химических реакций. 8 класс
Классификация химических реакций. 8 класс Агрегатные состояния вещества
Агрегатные состояния вещества Техника безопасности на уроках химии. Решение экспериментальных задач по теме Неметаллы. Практическая работа №2
Техника безопасности на уроках химии. Решение экспериментальных задач по теме Неметаллы. Практическая работа №2 Презентации-задания к урокам химии по различным темам
Презентации-задания к урокам химии по различным темам Соединения углерода
Соединения углерода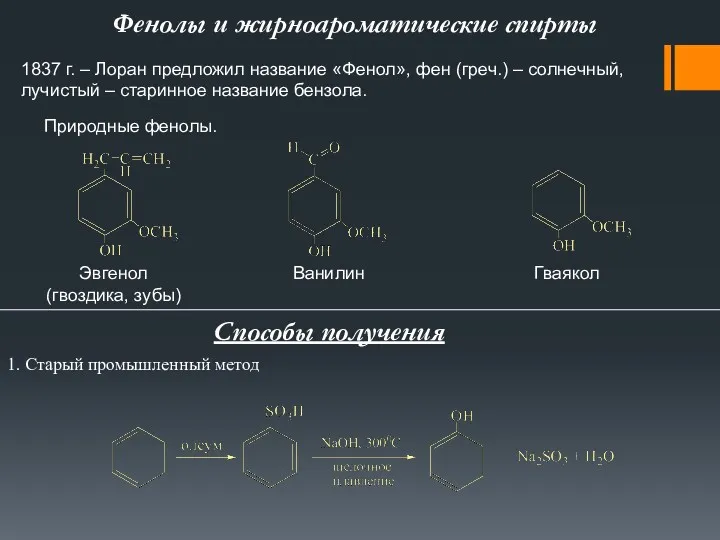 Фенолы и жирноароматические спирты
Фенолы и жирноароматические спирты Бензин: догадкии реальность
Бензин: догадкии реальность Фосфор и его соединения
Фосфор и его соединения НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Координационные соединения
Координационные соединения Конструкционные материалы
Конструкционные материалы Электролитическая диссоциация. Занятие 14
Электролитическая диссоциация. Занятие 14 20231009_zhyostkost_vody
20231009_zhyostkost_vody