Содержание
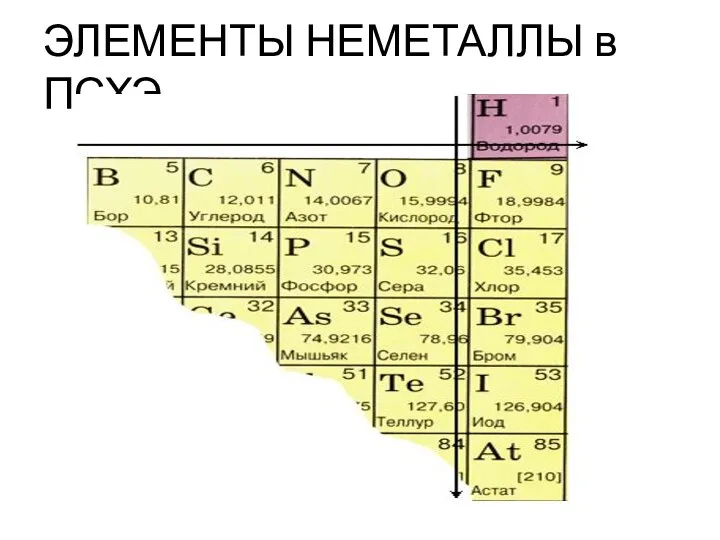
- 2. ЭЛЕМЕНТЫ НЕМЕТАЛЛЫ в ПСХЭ
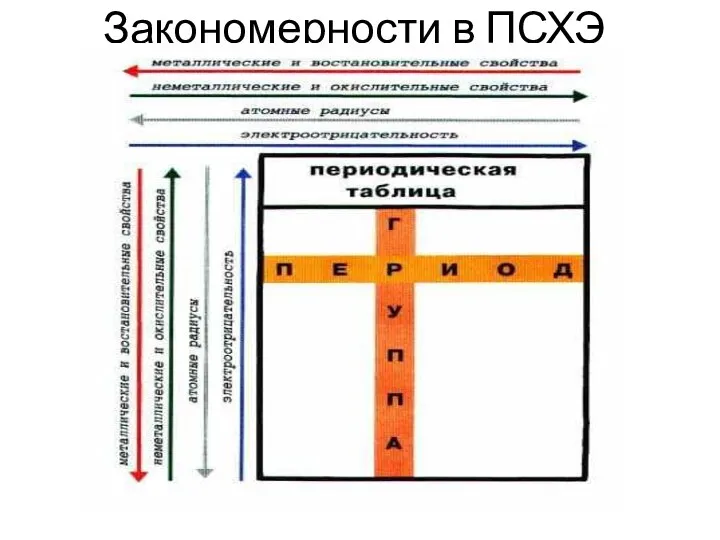
- 3. Закономерности в ПСХЭ
- 4. №1 Как меняется число электронов на внешнем энергетическом уровне от кремния к хлору? Как меняется радиус
- 5. №2 а)…3S23P2 б )…2S22P5 в) 1S 22S 22P 3 г )…4S24P2 Определите химический элемент
- 6. №3 а) S или P в)As или Cl У какого элемента в большей степени выражены неметаллические
- 7. №4 Какие химические элементы –неметаллы существуют в природе в виде простых веществ? Почему? Какие соединения неметаллов
- 8. №5 вещество кристаллическая решетка 1)ГРАФИТ А)МОЛЕКУЛЯРНАЯ 2)БЕЛЫЙ ФОСФОР Б)ИОННАЯ 3)ОЗОН В)МЕТАЛЛИЧЕСКАЯ 4)КРЕМНИЙ Г)АТОМНАЯ Установить соответствие между
- 9. №6 А) КАЛИЕМ Б) АЛЮМИНИЕМ В)ХЛОРОМ Г)ВОДОРОДОМ окислительные свойства сера проявляет при взаимодействии с :
- 10. №7 А) КИСЛОРОДОМ Б) ГИДРОКСИДОМ НАТРИЯ В) АЗОТНОЙ КИСЛОТОЙ Г)НАТРИЕМ Восстановительные свойства сера проявляет при взаимодействии
- 11. №8 1)NO 2)NO2 3)Cl2O7 4) SiO 5) N2O 6) SO2 Выбрать кислотные оксиды. Запишите соответствующие цифры
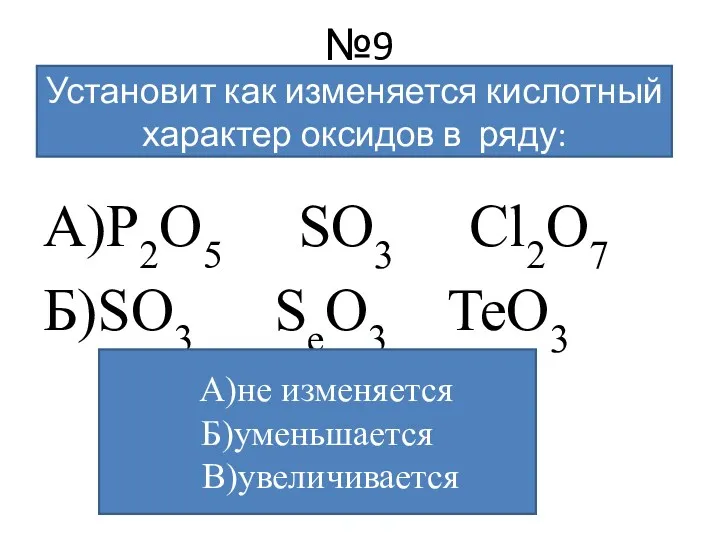
- 12. №9 А)P2O5 SO3 Cl2O7 Б)SO3 SeO3 TeO3 Установит как изменяется кислотный характер оксидов в ряду: А)не
- 13. №10 SiO2 NaOH NaCL CaO H2O HNO3 1 2 3 4 5 6 Выбрать с какими
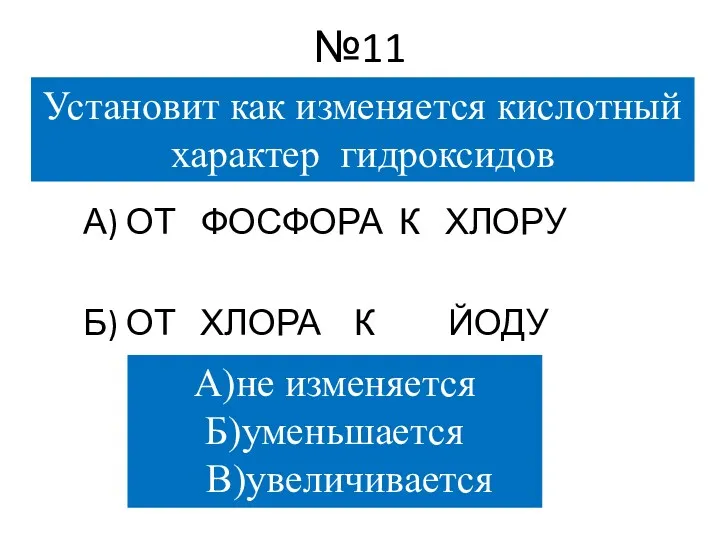
- 14. №11 А) ОТ ФОСФОРА К ХЛОРУ Б) ОТ ХЛОРА К ЙОДУ Установит как изменяется кислотный характер
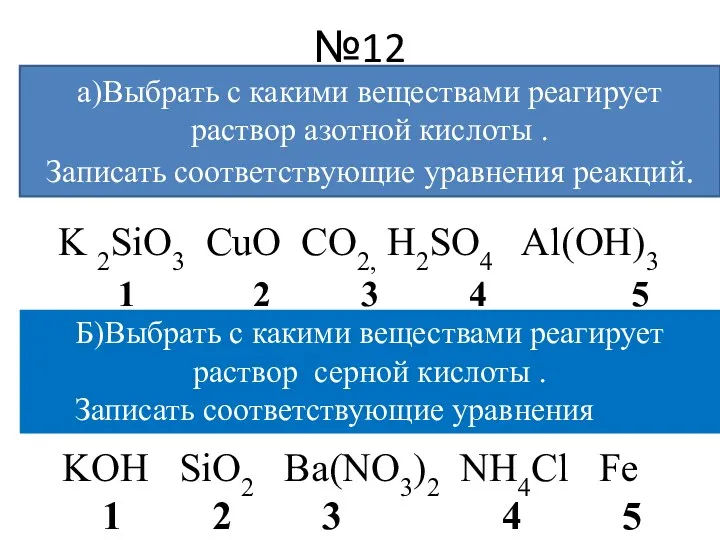
- 15. №12 K 2SiO3 CuO CO2, H2SO4 Al(OH)3 1 2 3 4 5 а)Выбрать с какими веществами
- 16. №13 УГЛЕРОДА--- АЗОТА ---КИСЛОРОДА ---ФТОРА Укажите как меняется характер водных растворов этих соединений А) не изменяется
- 17. №14 Летучее водородное соединение NH3 CH4 H2O HCL РЕАГЕНТЫ А) Zn, KOH, Cu(OH)2 Б) Na, SO2,
- 18. №15 а)Zn + H2SO4 --?H2S +….+ H2O б)Zn +HNO3-?NH4NO3 +…+ H2O в)Si + NaOH + H2O
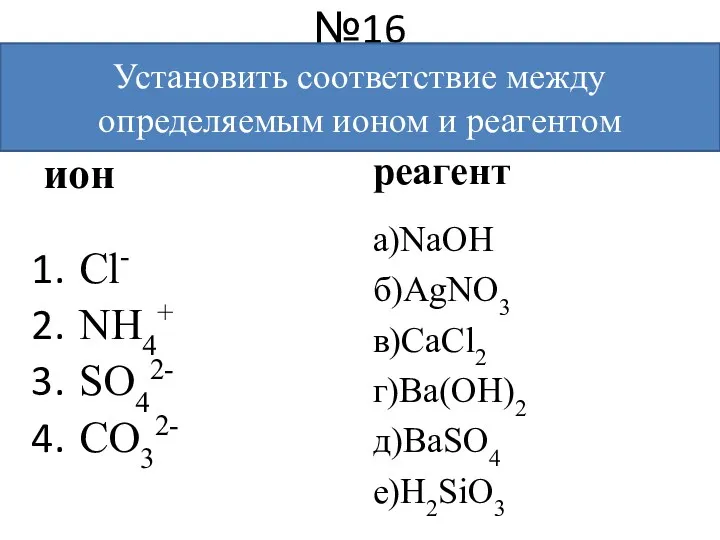
- 19. №16 ион Cl- NH4+ SO42- CO32- реагент а)NaOH б)AgNO3 в)CaCl2 г)Ba(OH)2 д)BaSO4 е)H2SiO3 Установить соответствие между
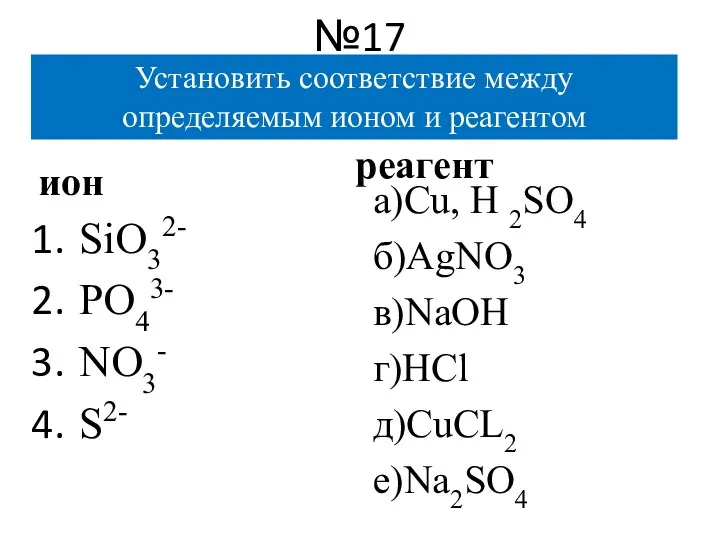
- 20. №17 ион SiO32- PO43- NO3- S2- реагент а)Cu, H 2SO4 б)AgNO3 в)NaOH г)HCl д)CuCL2 е)Na2SO4 Установить
- 22. Скачать презентацию












 Классификация и свойства оксидов
Классификация и свойства оксидов Элементы VII группы периодической таблицы Д.И. Менделеева
Элементы VII группы периодической таблицы Д.И. Менделеева Многоядерные ароматические углеводороды
Многоядерные ароматические углеводороды Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння
Тепловий ефект хімічних реакцій. Екзотермічні і ендотермічні реакції. Термохімічні рівняння Закон сохранения массы вещества
Закон сохранения массы вещества Оксигеновмісні сполуки. Одноатомні та багатоатомні спирти. Феноли. Лекція №6
Оксигеновмісні сполуки. Одноатомні та багатоатомні спирти. Феноли. Лекція №6 Физические явления в химии. Чистые вещества и смеси
Физические явления в химии. Чистые вещества и смеси Аналитическая химия
Аналитическая химия Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас
Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник
Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник Электронный помощник по химии (8 класс)
Электронный помощник по химии (8 класс) Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений
Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений Окислительно – восстановительные реакции
Окислительно – восстановительные реакции Хімічні властивості насичених одноатомних спиртів. Одержання етанолу
Хімічні властивості насичених одноатомних спиртів. Одержання етанолу Алкалоїди. Поняття алкалоїди і їх функції
Алкалоїди. Поняття алкалоїди і їх функції Методика “Кольоропис”
Методика “Кольоропис” Продукция UNIL
Продукция UNIL Геохимическая классификация элементов
Геохимическая классификация элементов Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Химия в решении сырьевой проблемы
Химия в решении сырьевой проблемы Анализ лекарственных средств паминофенола, ароматических кислот: бензойная кислота, натрия бензоат, салициловая кислота
Анализ лекарственных средств паминофенола, ароматических кислот: бензойная кислота, натрия бензоат, салициловая кислота Составление уравнений химических реакций. Закон сохранения массы веществ
Составление уравнений химических реакций. Закон сохранения массы веществ Поширення солей у природі
Поширення солей у природі Тотығу-тотықсыздану реакциялары
Тотығу-тотықсыздану реакциялары Кислород. Электронное строение и свойства
Кислород. Электронное строение и свойства Степень окисления ОВР
Степень окисления ОВР Основные законы химии
Основные законы химии