Содержание
- 2. Проверка ДЗ 9м: H2SO4, SO2, NO2, HNO3, KMnO4 9ч:H2SO4 SO2 H2S
- 3. ОВР Реакции протекающие с изменением степеней окисления – называются окислительно-восстановительными реакциями (ОВР). Окислитель – химический элемент,
- 4. ОВР Окислительно-восстановительные реакции – такие реакции, в которых меняется степень окисления элементов. С + О2 =
- 5. ОВР С + О2 = СО2 e- Процесс отдачи электронов называют окислением, а процесс присоединения –
- 6. Метод электронно-ионного баланса Окислительно-восстановительные реакции бывает сложно уровнять. K2Cr2O7 + H2SO4 + H2S = Cr2(SO4)3 +
- 7. Метод электронно-ионного баланса K2Cr2O7 + 4H2SO4 + 3H2S = Cr2(SO4)3 + 7H2O + 3S(т) + K2SO4
- 8. Метод электронно-ионного баланса K2Cr2O7 + 4H2SO4 + 3H2S = Cr2(SO4)3 + 7H2O + 3S(т) + K2SO4
- 9. Метод электронно-ионного баланса K2Cr2O7 + 4H2SO4 + 3H2S = Cr2(SO4)3 + 7H2O + 3S(т) + K2SO4
- 10. Метод электронно-ионного баланса K2Cr2O7 + 4H2SO4 + 3H2S = Cr2(SO4)3 + 7H2O + 3S(т) + K2SO4
- 11. Ещё один пример 1. Сначала записываем схему реакции: S + HNO3 = H2SO4 + NO
- 12. Метод электронно-ионного баланса Сначала записываем схему реакции. Определяем окислитель и восстановитель. S + HNO3 = H2SO4
- 13. Метод электронно-ионного баланса Сначала записываем схему реакции. Определяем окислитель и восстановитель. Под схемой реакции записываем в
- 14. Метод электронно-ионного баланса Сначала записываем схему реакции. Определяем окислитель и восстановитель. Под схемой реакции записываем в
- 15. Метод электронно-ионного баланса Сначала записываем схему реакции. Определяем окислитель и восстановитель. Под схемой реакции записываем в
- 16. Метод электронно-ионного баланса Сначала записываем схему реакции. Определяем окислитель и восстановитель. Под схемой реакции записываем в
- 17. Метод электронно-ионного баланса Попробуем: HCl + Cu + O2 ? CuCl2 + H2O
- 19. Скачать презентацию
















 Аллотропия
Аллотропия Основные классы неорганических соединений
Основные классы неорганических соединений Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Тяжелые металлы. Опасность токсичных металлов для организма
Тяжелые металлы. Опасность токсичных металлов для организма Основные синтетические полимеры
Основные синтетические полимеры Кислотные дожди
Кислотные дожди Механизмы трансформации энергии в фотосинтезе
Механизмы трансформации энергии в фотосинтезе 20230330_zakony_termodinamiki_i_kinetika
20230330_zakony_termodinamiki_i_kinetika S-элементтердің жалпы сипаттамасы
S-элементтердің жалпы сипаттамасы 20230219_prezentatsiya_k_uroku_neft
20230219_prezentatsiya_k_uroku_neft Общая характеристика элементов главной подгруппы второй группы
Общая характеристика элементов главной подгруппы второй группы Розв’язування задач на приготування розчинів із кристалогідратів
Розв’язування задач на приготування розчинів із кристалогідратів Термодинамика растворов неэлектролитов
Термодинамика растворов неэлектролитов Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Технология монокристаллов и особо чистых веществ
Технология монокристаллов и особо чистых веществ Оксиды и гидроксиды металлов. 11 класс
Оксиды и гидроксиды металлов. 11 класс Химические реакции или химические явления
Химические реакции или химические явления Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Факторы и процессы формирования химического состава подземных вод
Факторы и процессы формирования химического состава подземных вод Комплексиметрическое титрование
Комплексиметрическое титрование Электролиз. Классификация
Электролиз. Классификация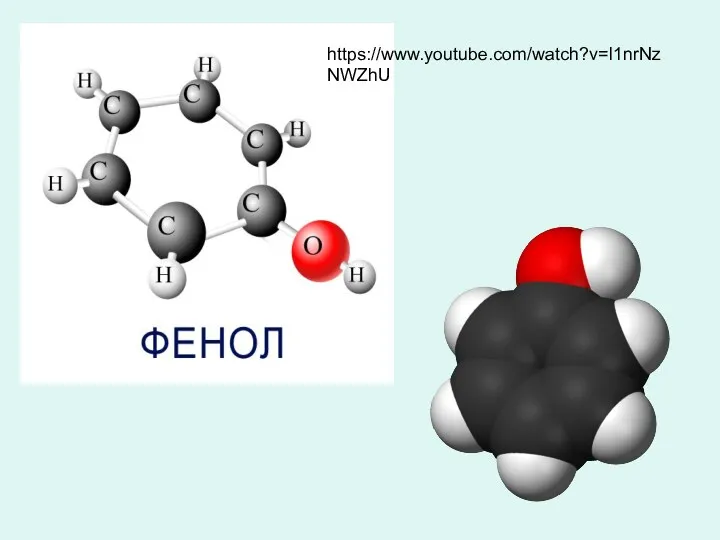 Фенол. Феноловая катастрофа
Фенол. Феноловая катастрофа Составление формул молекулярных простых веществ
Составление формул молекулярных простых веществ Щавелевая кислота
Щавелевая кислота Нанотехнологии и Наноматериалы
Нанотехнологии и Наноматериалы Кислоты. Определение и классификация
Кислоты. Определение и классификация Исследование Е. Е. Вагнера в области терпенов и камфоры
Исследование Е. Е. Вагнера в области терпенов и камфоры