Содержание
- 2. В окислительно-восстановительных реакциях переход электронов от восстановителей к окислителям происходит непосредственно при контакте частиц. При этом
- 3. Процессы взаимного превращения химической и электрической форм энергии называют электрохимическими процессами. Электрохимические процессы можно разделить на
- 4. О направлении окислительно-восстановительных реакций можно судить по изменению энергии Гиббса системы (ΔG). В соответствии с законами
- 5. Понятие об электродном потенциале Сущность возникновения электродного потенциала заключается в следующем: при погружении металла в раствор
- 6. Между металлом и раствором возникает разность потенциалов, которая называется электродным потенциалом. По мере перехода ионов в
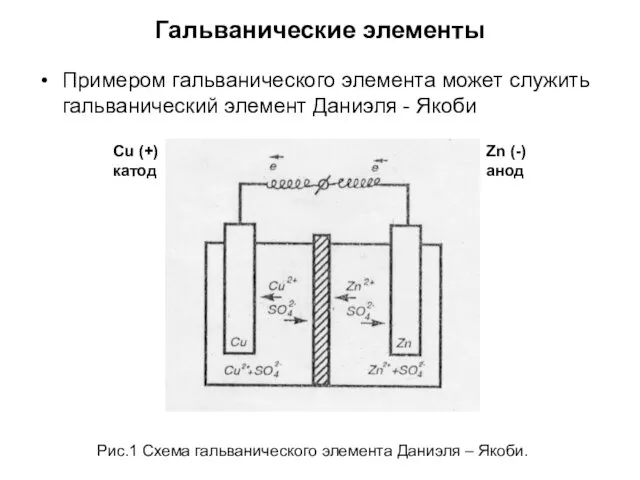
- 7. Гальванические элементы Примером гальванического элемента может служить гальванический элемент Даниэля - Якоби Рис.1 Схема гальванического элемента
- 8. Гальванический элемент состоит из медной пластины, погруженной в раствор CuSO4, и цинковой пластины, погруженной в раствор
- 9. На поверхности медной пластины также возникает двойной электрический слой и устанавливается равновесие: Cu + mH2O Cu(H2O)2+
- 10. В результате перехода электронов от цинка к меди равновесие на цинковом электроде сместится вправо, поэтому в
- 11. При работе элемента Даниэля - Якоби протекают следующие процессы: 1. реакция окисления цинка Zn - 2e
- 12. Суммируя электродные реакции, получаем: Zn + Cu2+ = Cu + Zn2+ При схематической записи, заменяющий рисунок
- 13. Стандартный водородный электрод и водородная шкала потенциалов Абсолютные значения электродных потенциалов экспериментально определить невозможно. Однако можно
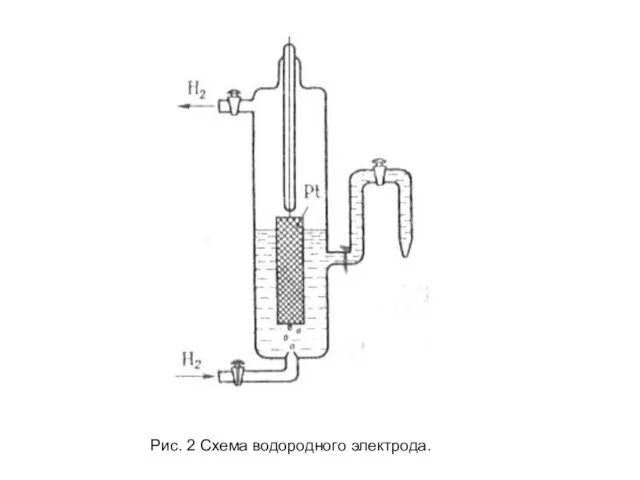
- 14. Рис. 2 Схема водородного электрода.
- 15. При контакте платины с молекулярным водородом происходит адсорбция водорода на платине. Адсорбированный водород, взаимодействуя с молекулами
- 16. Абсолютное значение потенциала водородного электрода неизвестно, но условно считают за нуль потенциал стандартного водородного электрода, т.е.
- 17. Понятие о стандартном электродном потенциале. Уравнение Нернста Стандартный электродный потенциал металлического электрода – это потенциал этого
- 18. Стандартные электродные потенциалы металлов указывают на меру окислительно-восстановительной способности металла и его ионов. Чем более отрицательное
- 19. Электродный потенциал зависит от природы металла, температуры и концентрации ионов в растворе (уравнение Нернста): ЕMn+ /
- 20. Понятие о стандартном окислительно-восстановительном потенциале. Направление окислительно-восстановительных процессов При использовании инертных электродов в гальванических элементах (угольно-графитовых,
- 21. В общем виде равновесие на электродах для простых систем записывается уравнением: Окисл. форма + ne ⇔
- 22. Пример 1 Реакция Sn2+Cl2 + 2Fe3+Cl3 2Fe2+Cl2 + Sn4+Cl4 Sn2+ + 2Fe3+ 2Fe2+ + Sn4+ Sn2+
- 23. Пример 2 Уравнение 2KMnO4 + 10FeSO4 + 8H2SO4 = 2MnSO4 + 5Fe2(SO4)3 + K2SO4 + 8H2O
- 24. ЭЛЕКТРОЛИЗ. ЗАКОНЫ ФАРАДЕЯ Электролиз - процесс раздельного окисления и восстановления на электродах, осуществляемый при прохождении постоянного
- 25. В качестве инертных анодов обычно используют графит и платину. Инертный анод является лишь передатчиком электронов, а
- 26. При наличии в растворе нескольких типов катионов и анионов на катоде в первую очередь должны восстанавливаться
- 27. Восстановительный процесс на катоде в водных растворах имеет следующие особенности: 1) Катионы металлов со стандартным электродным
- 28. В идеальных условиях осуществления электролиза необходимо приложить противоположную по знаку ЭДС гальванического элемента. Однако реальные электрохимические
- 29. Водородное перенапряжение позволяет электрохимически выделить на катоде более активные металлы (находящиеся в ряду напряжений между алюминием
- 30. Анодное перенапряжение - это дополнительное напряжение, прикладываемое к аноду (при этом потенциал анода смещается далее в
- 31. Например, при электролизе СuВr2 на электродах произойдут следующие процессы: СuВr2 Сu2+ + 2Вr¯; Н2О Н+ +
- 32. При электролизе кислородосодержащих кислот и их солей (SO42-,NO3-, PO43-) на аноде окисляются молекулы воды с выделением
- 33. Процесс электролиза широко применяется в различных областях современной техники. Электролизом солей с нерастворимыми анодами получают (гидрометаллургия)
- 35. Скачать презентацию






























 Получение уксусной кислоты и опыты с ней
Получение уксусной кислоты и опыты с ней Получение лиофобных коллоидных растворов методом пептизации на примере золя берлинской лазури
Получение лиофобных коллоидных растворов методом пептизации на примере золя берлинской лазури Реакции деструкции макромолекул
Реакции деструкции макромолекул Морфология тел полезных ископаемых
Морфология тел полезных ископаемых Галогены - химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева
Галогены - химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева Формирование системы знаний о веществе. Лекция 14-15
Формирование системы знаний о веществе. Лекция 14-15 Соли. Классификация. Физические и химические свойства. Получение и применение солей
Соли. Классификация. Физические и химические свойства. Получение и применение солей Неметаллические и композиционные материалы
Неметаллические и композиционные материалы Ненасыщенные углеводороды. Алкены
Ненасыщенные углеводороды. Алкены Многоядерные ароматические углеводороды
Многоядерные ароматические углеводороды 20190430_otkrytyy_urok_kislotypptx
20190430_otkrytyy_urok_kislotypptx Ендотермічні реакції на службі людини
Ендотермічні реакції на службі людини Ионное произведение воды. Водородный показатель воды
Ионное произведение воды. Водородный показатель воды Виды присадок к моторным топливам
Виды присадок к моторным топливам Кислородсодержащие соединения серы
Кислородсодержащие соединения серы Алюминий и его соединения
Алюминий и его соединения Фосфор и его соединения. 9 класс
Фосфор и его соединения. 9 класс Строение атома. Классификация ядер атомов
Строение атома. Классификация ядер атомов Колоїдний захист
Колоїдний захист Решение задач. Способы выражения состава раствора
Решение задач. Способы выражения состава раствора Свойства, получение и применение алканов. Циклоалканы
Свойства, получение и применение алканов. Циклоалканы Электрохимическая коррозия
Электрохимическая коррозия Проект Кабинет химии будущего
Проект Кабинет химии будущего Процессы алкилирования
Процессы алкилирования Белоктар. Биохимиясы
Белоктар. Биохимиясы ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА
ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА Учение об агрегатных состояниях вещества. Газообразное состояние
Учение об агрегатных состояниях вещества. Газообразное состояние Роль хімії у розв`язанні екологічної проблеми
Роль хімії у розв`язанні екологічної проблеми