Содержание
- 2. Модуль 2. Электрохимическая коррозия Лекция 2.1 – самопроизвольный процесс разрушения металла под действием электролитов, при котором
- 3. Электрохимическая коррозия Процесс электрохимической коррозии наблюдается всегда, когда на поверхности металла появляется электролит. Электролит – любая
- 4. В практике мы обыкновенно сталкиваемся с тремя видами коррозии и сразу возникает вопрос к какому типу
- 5. Модуль 2. Электрохимическая коррозия Лекция 2.1 Электролит - раствор NaCl) H+, Н2О, Na+, Cl- ,ОН- ,
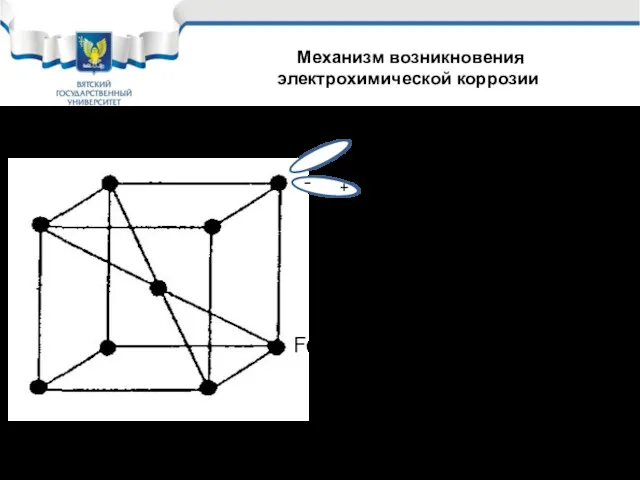
- 6. Fe+2 1.1 Fe - 2e → Fe2+ 1.2 Fe2+ + 2е → Fe Механизм возникновения электрохимической
- 7. Механизм возникновения электрохимической коррозии При одновременном протекании 4 – ех реакций на поверхности металла устанавливается средний
- 8. Екор – потенциал коррозии, образующийся за счёт одновременного протекания на нём двух электрохимических реакций очень важное
- 9. Коррозионный потенциал возникает всегда когда выполняется термодинамическое условие электрохимической коррозии Термодинамическое условие: ЕMeравн Коррозионный потенциал довольно
- 10. Насколько часто выполняется термодинамическое условие электрохимической коррозии? ЕMeравн В обычной воде есть следующие виды молекул и
- 11. Al Zn Fe Ni H2 Cu Ag O2 -1,5 -0,79 -0,44 -0,23 0 +0,34 1,23 Термодинамика
- 12. Теория компромиссного потенциала Рассмотренная теория электрохимической коррозии, объясняющая ее возникновение через компромиссный потенциал коррозии называется теорией
- 13. Локальный характер протекания электрохимической коррозии Катодная и анодная реакции коррозионного процесса могут одновременно протекать на всей
- 14. Причины локальности электрохимической Причин локального протекания электрохимической коррозии много: неоднородность металла; (примеси других металлов, наличие неметаллических
- 15. Отсюда много видов локальной коррозии: язвенная, питтинговая (точечная), коррозия пятнами, межкристаллитная, коррозионное растрескивание, коррозионная усталость и
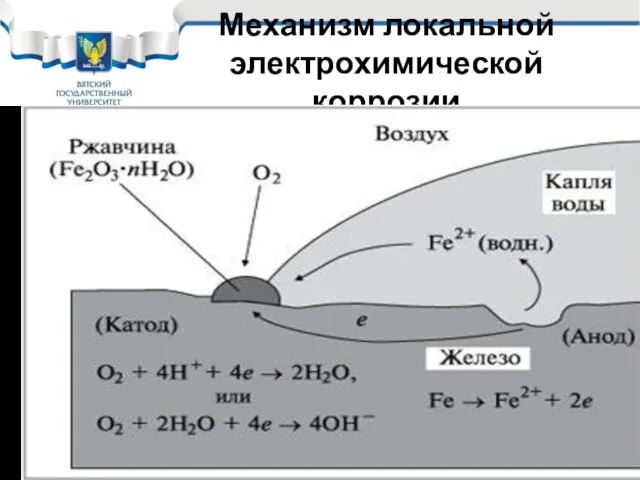
- 16. Механизм локальной электрохимической коррозии
- 17. Локальный характер протекания электрохимической коррозии В результате переноса ионов и электронов в электролите и в металле
- 18. Особенности анодной реакции коррозионного процесса Анодная реакция коррозионного процесса, заключающаяся в окислении металла с получением разнообразных
- 19. Гидратированные катионы [Ме(Н2О)]ne+ Комплексные соединения [Ме(Кn)]m+ , [Ме(Кn)]m- Оксиды и гидроксиды МеО, Ме(ОН)2 Сложные анионы металла
- 20. Особенности электрохимической коррозии Растворимые продукты коррозии не оказывают влияние на скорость коррозии, а неплотные тормозят ее
- 21. Возникает всегда, когда на поверхности металла появляется электролит; Протекает в виде двух сопряженных электрохимических реакций; На
- 22. Теория локальных элементов Электрохимическая теория компромиссного потенциала возникла не первой. Первой возникла теория локальных элементов. Она
- 23. Теория локальных элементов Так как в реальной практике электрохимическая коррозия часто протекает локально и в виде
- 24. Химический механизм коррозии в электролитах Впервые о химическом механизме коррозии в электролитах заговорили лет 40 назад.
- 25. Химический механизм коррозии в электролитах При электрохимическом механизме коррозии зависимость скорости коррозии от потенциала должна быть
- 27. Скачать презентацию















![Гидратированные катионы [Ме(Н2О)]ne+ Комплексные соединения [Ме(Кn)]m+ , [Ме(Кn)]m- Оксиды и](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/126959/slide-18.jpg)






 Галогены
Галогены Коррозия металлов
Коррозия металлов Заключительный урок в 8 классе Тест по химии.
Заключительный урок в 8 классе Тест по химии. Технология производства сложных полиэфиров
Технология производства сложных полиэфиров Вред Coca-Cola на организм человека
Вред Coca-Cola на организм человека Оксиды и гидроксиды металлов. 11 класс
Оксиды и гидроксиды металлов. 11 класс Непредельные углеводороды
Непредельные углеводороды Аммиак
Аммиак Мыло
Мыло Олово и свинец
Олово и свинец Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі
Судың диссоциациялануы. Сутектік көрсеткіш. Тұздар гидролизі Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления
Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления Ультраосновные породы (гипербазиты)
Ультраосновные породы (гипербазиты) Коррозия металлов
Коррозия металлов Строение атома. Периодический закон и периодическая система элементов
Строение атома. Периодический закон и периодическая система элементов Кислородные соединения азота
Кислородные соединения азота Карбоновые кислоты
Карбоновые кислоты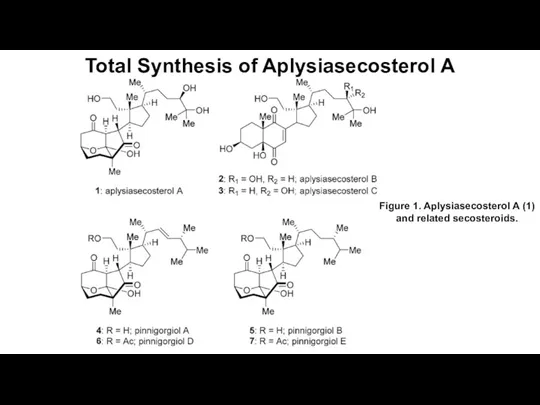 Total Synthesis of Aplysiasecosterol A
Total Synthesis of Aplysiasecosterol A Кислоты и основания. (Лекция 16)
Кислоты и основания. (Лекция 16) Stirring in liquid media
Stirring in liquid media Химия в быту
Химия в быту Ископаемые углеводороды
Ископаемые углеводороды NaHSO4. Гидросульфат натрия
NaHSO4. Гидросульфат натрия Современные тенденции развития химии
Современные тенденции развития химии Иондық байланыс
Иондық байланыс Вклад ученых-химиков в победу в Великой Отечественной войне
Вклад ученых-химиков в победу в Великой Отечественной войне ЕГЭ по химии. Анализ результатов решения (часть 2)
ЕГЭ по химии. Анализ результатов решения (часть 2) Органические и неорганические кислоты
Органические и неорганические кислоты