Содержание
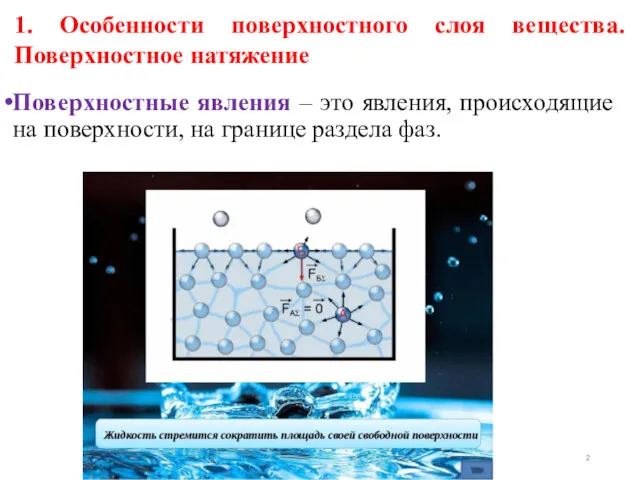
- 2. Поверхностные явления – это явления, происходящие на поверхности, на границе раздела фаз. 1. Особенности поверхностного слоя
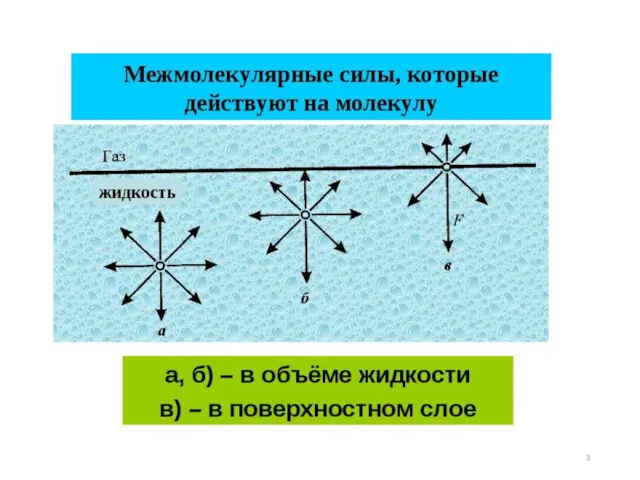
- 4. Молекулы поверхностного слоя обладают некоторым избытком энергии по сравнению со внутренними, что позволяет им удерживаться на
- 5. Поверхностное натяжение – это сила, стягивающая гипотетическую пленку на поверхности жидкости и противодействующая ее растяжению Увеличение
- 6. Из определения следует: G = σ∙s σ = [Дж/м2=Н∙м/м2= Н/м] – поверхностное натяжение; s – площадь
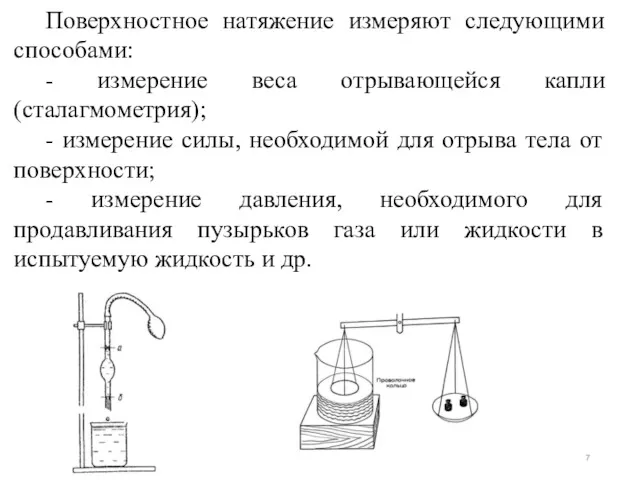
- 7. Поверхностное натяжение измеряют следующими способами: - измерение веса отрывающейся капли (сталагмометрия); - измерение силы, необходимой для
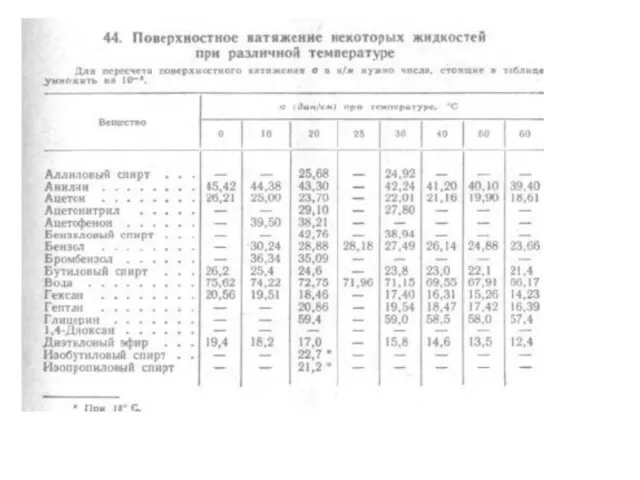
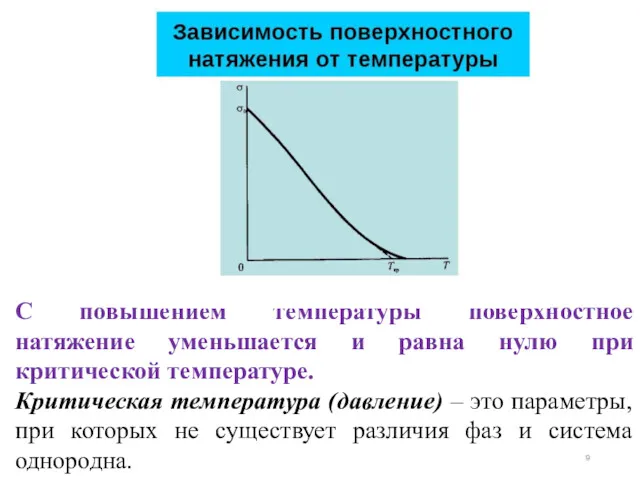
- 9. С повышением температуры поверхностное натяжение уменьшается и равна нулю при критической температуре. Критическая температура (давление) –
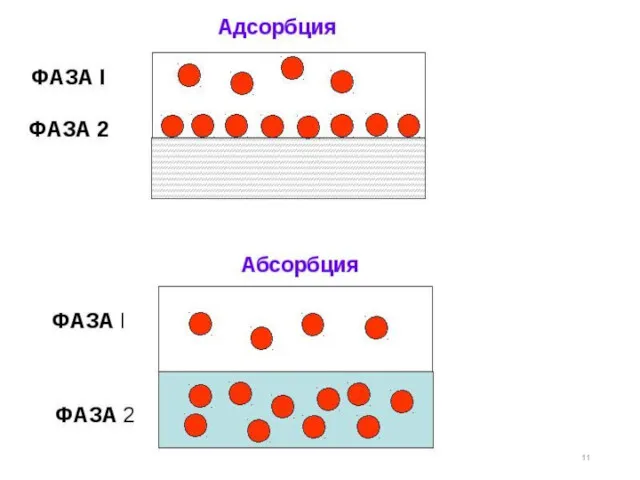
- 10. 2. Адсорбция. Основные понятия и определения. Виды адсорбции и их применение Адсорбция (Г) – это самопроизвольное
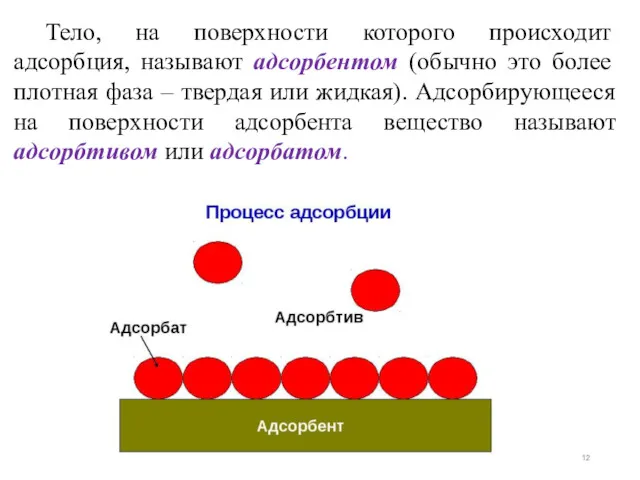
- 12. Тело, на поверхности которого происходит адсорбция, называют адсорбентом (обычно это более плотная фаза – твердая или
- 13. Измеряют адсорбцию как количество адсорбата, отнесенное к единице площади или массы адсорбента Г (гамма) = кмоль/м2;
- 14. Из второго закона термодинамики следует, адсорбция протекает самопроизвольно в случае, если адсорбция приводит к уменьшению свободной
- 15. Термодинамический смысл процесса адсорбции: Вблизи поверхности твердого тела или жидкости в следствии наличия свободно поверхностной энергии
- 16. В зависимости от агрегатных состояний адсорбента и адсорбтива различают следующие виды адсорбции: - адсорбция газа на
- 17. Если процесс перехода вещества из объема фазы к поверхности сопровождается снижением величины σ, то вещество будет
- 18. Если растворенное вещество не изменяет σ адсорбция Г=0 и вещество равномерно распределено между поверхностным слоем и
- 20. При адсорбции одновременно протекают как физические, так и химические взаимодействия. В зависимости от преобладающего процесса: 1.
- 22. Применение адсорбции: для очистки газовых промышленных выбросов от вредных примесей (SO2, SH2 и др.). Например, для
- 23. 3. Адсорбция на границе раствор-газ Процесс адсорбции на границе описывается уравнение изотермы адсорбции Гиббса: С –
- 24. Из уравнения следует, что если: (с повышением концентрации σ понижается), то Г>0 – адсорбция идет (с
- 25. Значение производной dσ/dC, взятой с обратным знаком называется, поверхностной активностью (g): g = - dσ/dC Поверхностная
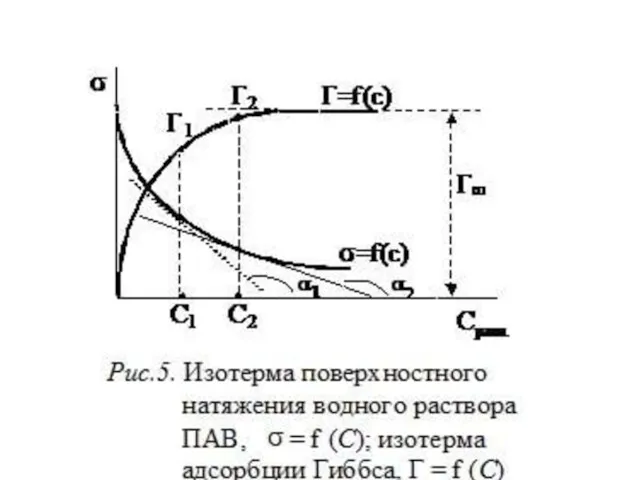
- 26. Графический метод определения адсорбции Находят экспериментально зависимость σ = f (C) (изотерма поверхностного натяжения). Проводят графическое
- 29. 4. Классификация веществ по поверхностной активности. Правило Дюкло-Траубе Поверхностно-активные вещества – это вещества, добавление которых к
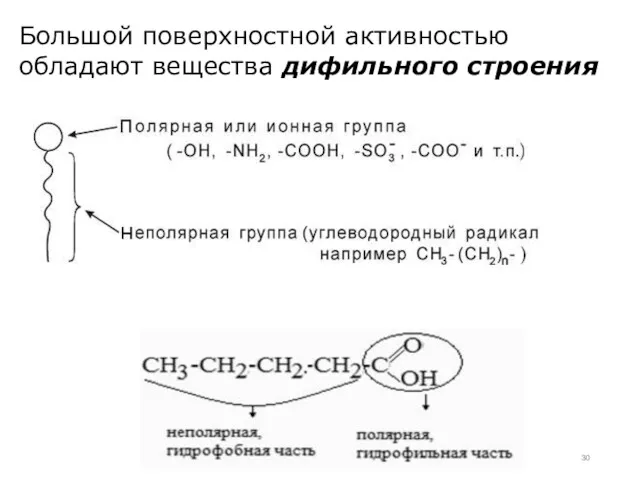
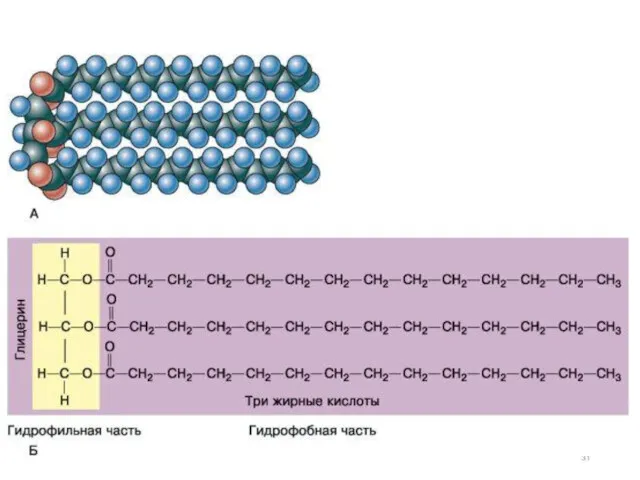
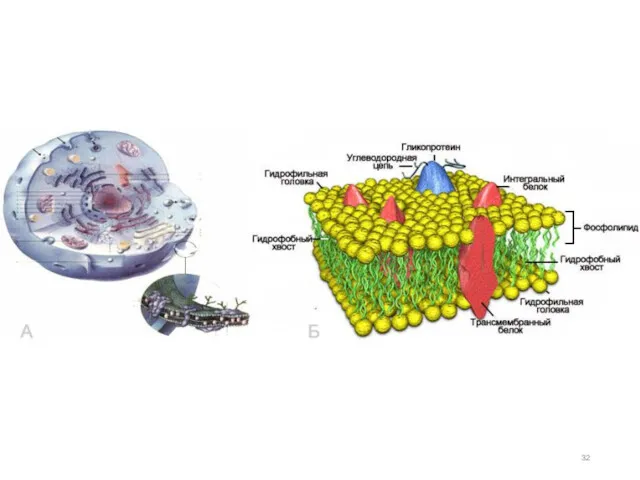
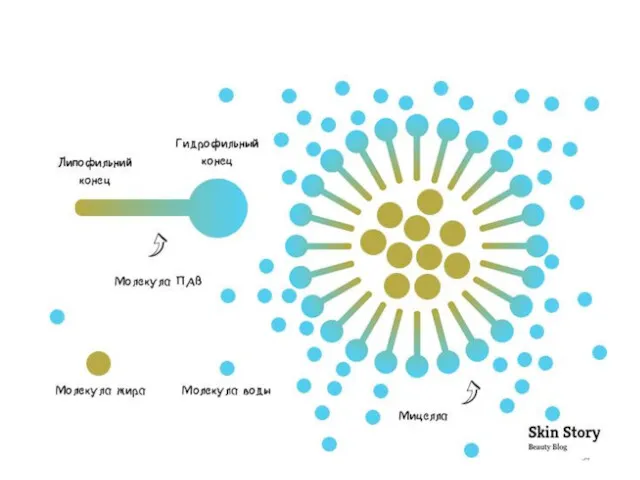
- 30. Большой поверхностной активностью обладают вещества дифильного строения
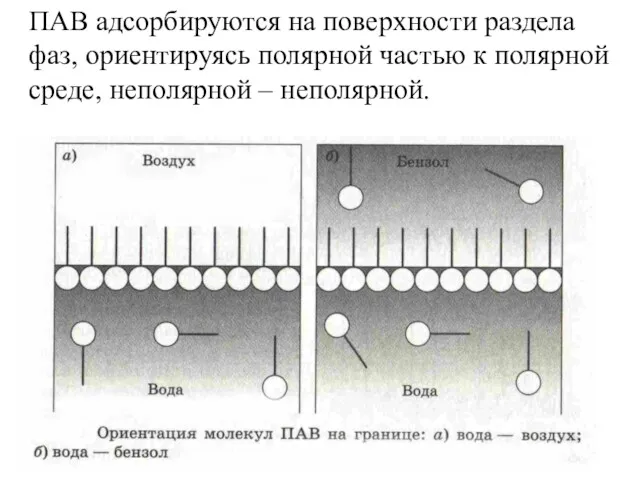
- 33. ПАВ адсорбируются на поверхности раздела фаз, ориентируясь полярной частью к полярной среде, неполярной – неполярной.
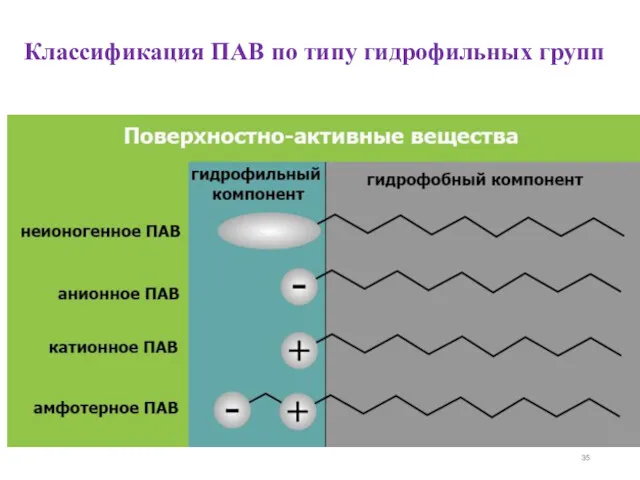
- 35. Классификация ПАВ по типу гидрофильных групп
- 36. -По типу гидрофильных групп различают неионные (неионогенные) и ионные (ионогенные) ПАВ. Неионогеные существуют в растворе в
- 37. Анионактивные ПАВ: карбоновые кислоты и их соли (мыла), алкилсульфаты, алкилсульфонаты, алкиларилсульфонаты, фенолы и др. Катионактивные ПАВ:
- 38. Поверхностно-инактивные вещества – это вещества, добавление которых к жидкости увеличивает ее поверхностное натяжение. ПАВ самопроизвольно переходят
- 39. Поверхностно-неактивные вещества – это вещества, добавление которых к жидкости не изменяет ее поверхностное натяжение. ПАВ равномерно
- 41. При экспериментальном изучении адсорбции на границе жидкость-газ Дюкло и Траубе установили следующую зависимость: поверхностная активность в
- 42. Правило выполняется при следующих условиях: при комнатной температуре; при малых концентрациях ПАВ (при больших концентрациях достигается
- 43. Адсорбция газов и жидкостей на поверхности твердого тела Теория мономолекулярной адсорбции Ленгмюра. В 1915 году И.
- 44. Основные положение теории Ленгмюра: 1). Поверхность адсорбента ограничена. Адсорбция вещества происходит не на всей поверхности, а
- 45. Уравнение изотермы мономолекулярной адсорбции Ленгмюра имеет вид: где А и А∞ ‑ соответственно величина адсорбции газа
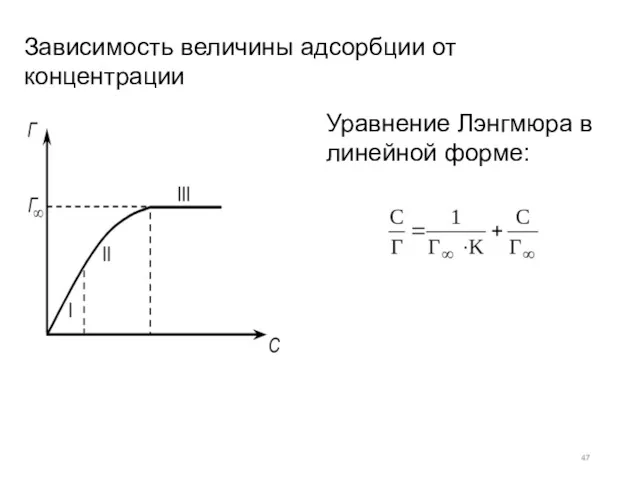
- 46. Уравнение Лэнгмюра для адсорбции из растворов: где Г – Гиббсовская адсорбция при концентрации С; Г∞– максимальная
- 47. Зависимость величины адсорбции от концентрации Уравнение Лэнгмюра в линейной форме:
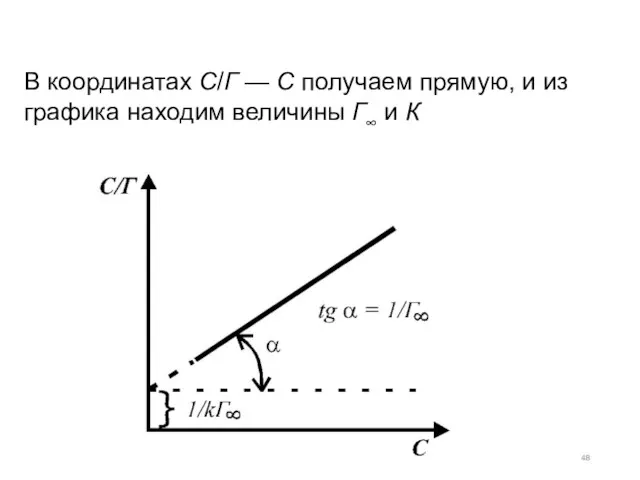
- 48. В координатах С/Г — С получаем прямую, и из графика находим величины Г∞ и К
- 49. Уравнением Фрейндлиха Адсорбция из растворов может быть описана уравнением Фрейндлиха, которое в данном случае имеет вид
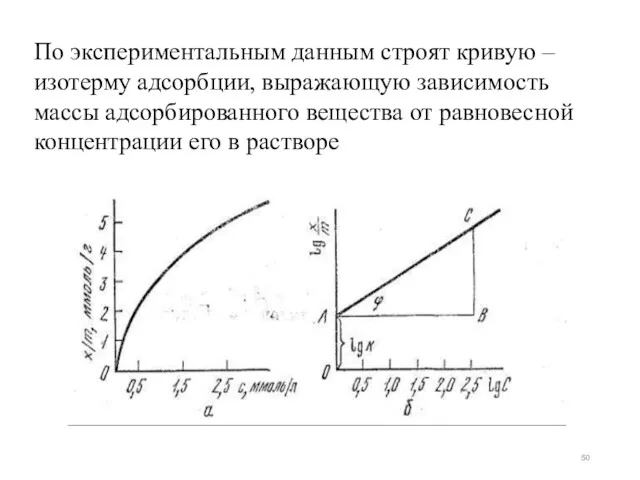
- 50. По экспериментальным данным строят кривую – изотерму адсорбции, выражающую зависимость массы адсорбированного вещества от равновесной концентрации
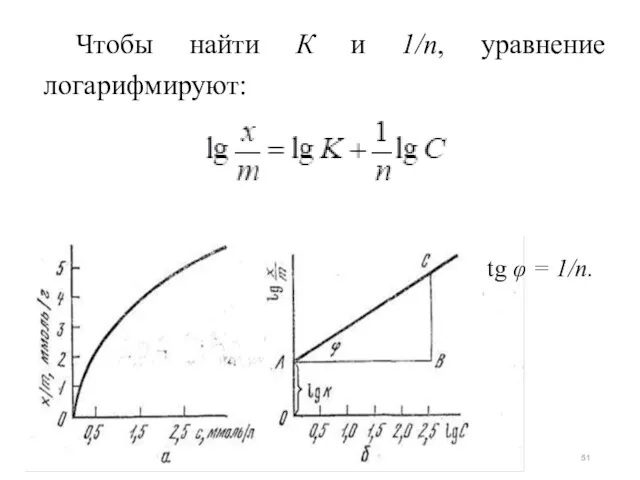
- 51. Чтобы найти К и 1/n, уравнение логарифмируют: tg φ = 1/n.
- 52. Полимолекулярная адсорбция (теория БЭТ). Основные положения.
- 53. Адсорбция из растворов электролитов Адсорбция из водных растворов электролитов происходит, как правило, таким образом, что на
- 54. Обменная адсорбция представляет собой процесс обмена ионов между раствором и твердой фазой, при котором твердая фаза
- 55. При специфической адсорбции адсорбция на поверхности твердой фазы ионов какого-либо вида не сопровождается выделением в раствор
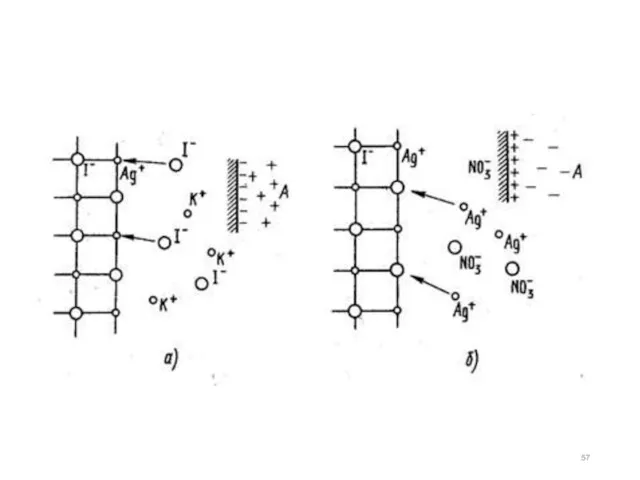
- 56. Пример. Рассмотрим адсорбцию ионов раствора КI на поверхности кристалла AgI. На поверхности кристаллов иодида серебра в
- 58. Если кристаллы AgI находятся в контакте с раствором AgNO3, то на поверхности кристаллов будут адсорбироваться ионы
- 59. Мицеллообразование в растворах ПАВ Под мицеллой (МЦ) ПАВ понимают ассоциат дифильных молекул, лиофильные группы которых обращены
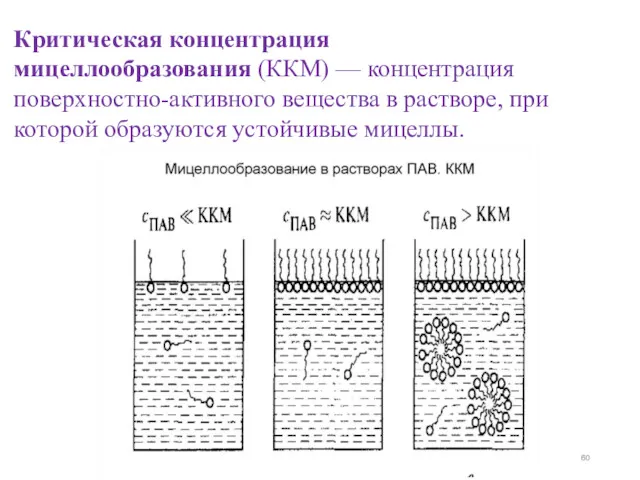
- 60. Критическая концентрация мицеллообразования (ККМ) — концентрация поверхностно-активного вещества в растворе, при которой образуются устойчивые мицеллы.
- 61. Растворы МЦобразующих ПАВ делят на 2 группы: 1) гомогенные при С 2) микрогетерогенные при С> СККМ
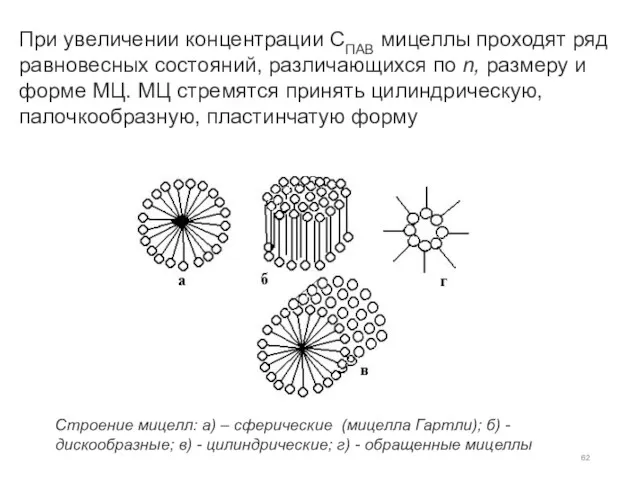
- 62. При увеличении концентрации СПАВ мицеллы проходят ряд равновесных состояний, различающихся по n, размеру и форме МЦ.
- 64. При ↑ концентрации СПАВ, превышающую ККМ в 10-50 раз в системе, ↓ подвижность мицелл и ↑
- 65. Мицеллы ионогенных ПАВ обычно заряжены, их заряд зависит от кислотно-основных свойств функциональных групп ПАВ и других
- 66. Явление растворения веществ в МЦПАВ называется солюбилизацией. В водных МЦ ПАВ солюбилизируются вещества, нерастворимые в воде:
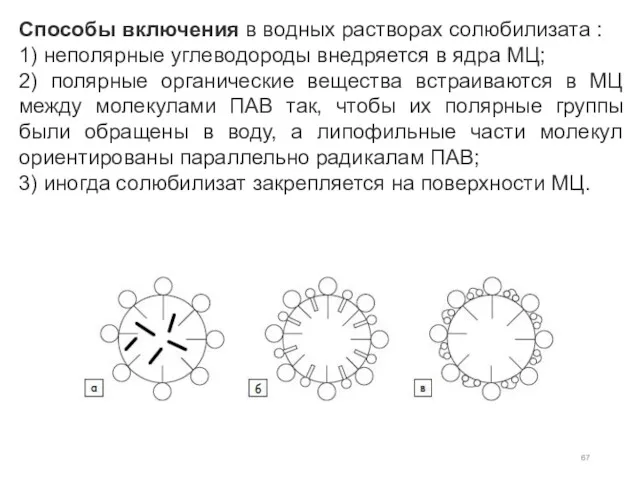
- 67. Способы включения в водных растворах солюбилизата : 1) неполярные углеводороды внедряется в ядра МЦ; 2) полярные
- 69. Скачать презентацию


![Из определения следует: G = σ∙s σ = [Дж/м2=Н∙м/м2= Н/м]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/123303/slide-5.jpg)









































 Хімічне виробництво сталі
Хімічне виробництво сталі Композиты как материалы конструкционного назначения
Композиты как материалы конструкционного назначения Химия в искусстве
Химия в искусстве Соли
Соли Кислородсодержащие соединения серы. Оксиды, кислоты, соли
Кислородсодержащие соединения серы. Оксиды, кислоты, соли Функциональные производные карбоновых кислот
Функциональные производные карбоновых кислот Xимия. Cr, Cu, Fe, Zn
Xимия. Cr, Cu, Fe, Zn Своя игра по химии
Своя игра по химии Мыло. Мылящие вещества в природе
Мыло. Мылящие вещества в природе Золото. История открытия
Золото. История открытия Сера и её соединения
Сера и её соединения Хімічний склад жувальної гумки
Хімічний склад жувальної гумки Рецепты литературы в химических опытах
Рецепты литературы в химических опытах Нуклеиновые кислоты
Нуклеиновые кислоты Горение топлива
Горение топлива Прикладные аспекты химии поверхностно-активных веществ
Прикладные аспекты химии поверхностно-активных веществ Гравиметрический метод анализа
Гравиметрический метод анализа Растворы ВМС
Растворы ВМС Основы коррозии и защиты металлов. Химическая коррозия
Основы коррозии и защиты металлов. Химическая коррозия Алюминий және оның қосылыстары
Алюминий және оның қосылыстары АТФ молекуласының құрылысы мен қызметтері
АТФ молекуласының құрылысы мен қызметтері алкадиены
алкадиены Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение
Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение Транспортное обеспечение внесения удобрений
Транспортное обеспечение внесения удобрений Щелочные металлы
Щелочные металлы 20230816_belki_2
20230816_belki_2 Электроотрицательность. Степень окисления. Валентность
Электроотрицательность. Степень окисления. Валентность Основные понятия органической химии. Лекция № 1
Основные понятия органической химии. Лекция № 1