Содержание
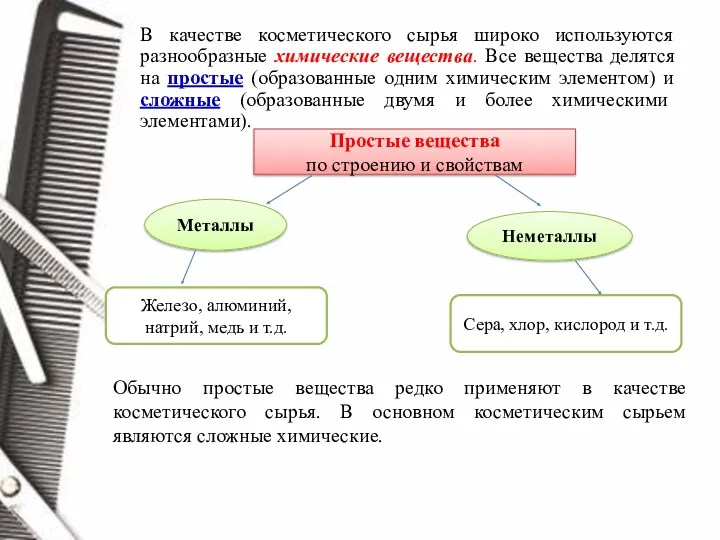
- 2. В качестве косметического сырья широко используются разнообразные химические вещества. Все вещества делятся на простые (образованные одним
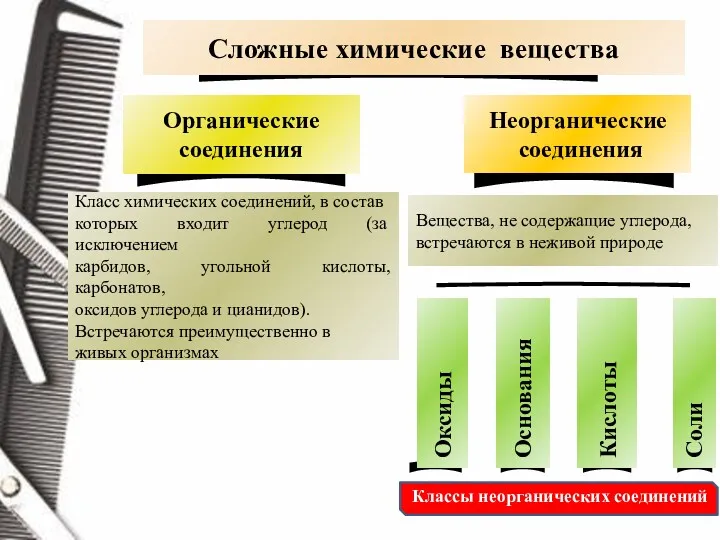
- 3. Классы неорганических соединений
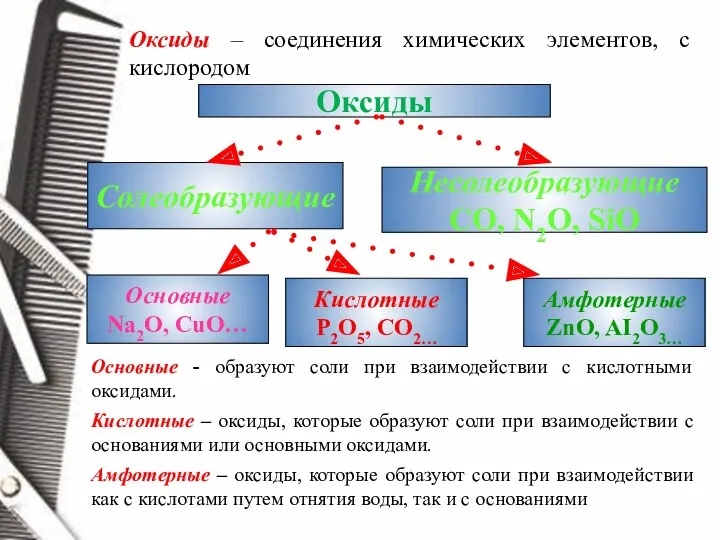
- 4. Оксиды – соединения химических элементов, с кислородом Оксиды Солеобразующие Несолеобразующие CO, N2O, SiO Основные Na2O, CuO…
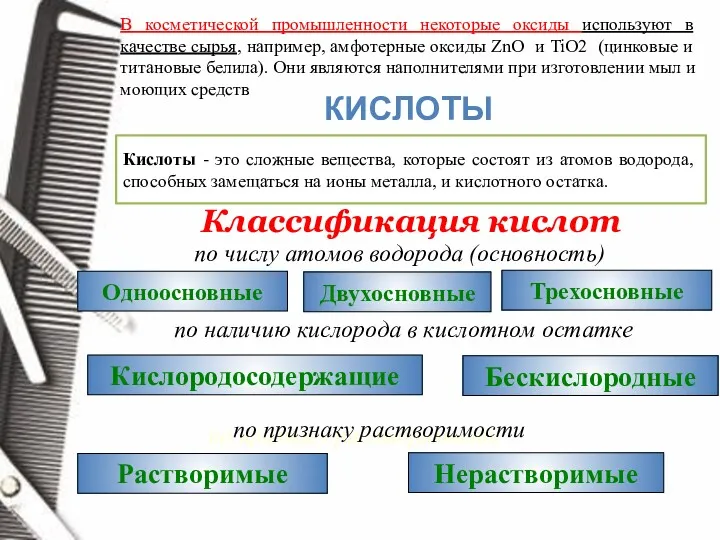
- 5. В косметической промышленности некоторые оксиды используют в качестве сырья, например, амфотерные оксиды ZnO и TiO2 (цинковые
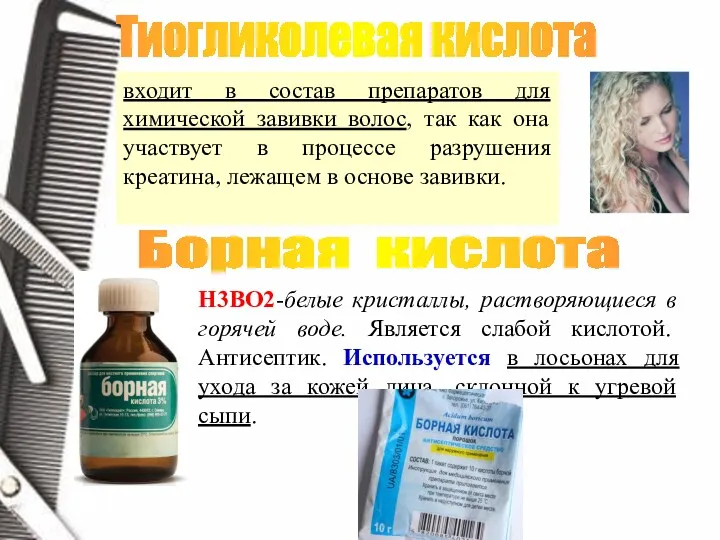
- 7. В парфюмерно-косметической промышленности наиболее часто используют карбоновые кислоты: бензойную, борную, салициловую, лимонную, уксусную, молочную, щавелевую, а
- 8. Молочная (аоксипропионовая) кислота СН3-СНОН-СООН –бесцветные гигроскопические кристаллы. Растворяется в воде, ацетоне. Используется в очищающих и регенерирующих
- 9. Уксусная кислота СН3СООН –бесцветная прозрачная жидкость с резким запахом и кислым вкусом, хорошо растворяется в воде,
- 10. НООС-СООН - простейшая двухосновная карбоновая кислота, кристаллическое вещество (t плавления 189 ° С), растворяется в воде,
- 11. входит в состав препаратов для химической завивки волос, так как она участвует в процессе разрушения креатина,
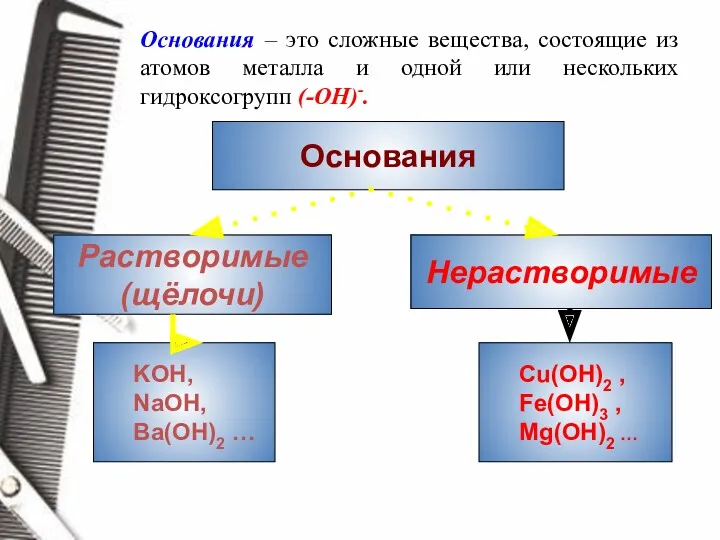
- 12. Основания – это сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп (-ОН)-.
- 13. ОСНОВАНИЯ Общая формула оснований M(OH)n, где n - степень окисления (заряд иона) металла. Также существуют бескислородные
- 14. Некоторые основания применяют в косметической промышленности: аммиак, гидроксид калия, гидроксид натрия. Нашатырный спирт (каустическая сода) -
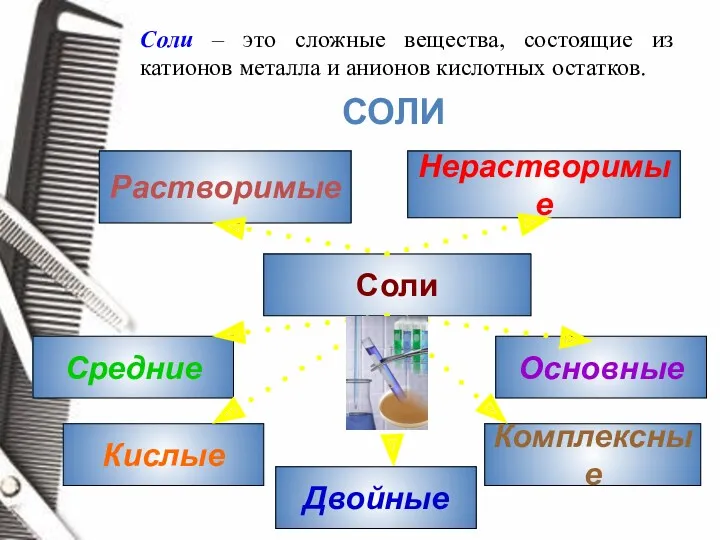
- 15. Соли – это сложные вещества, состоящие из катионов металла и анионов кислотных остатков. Соли Растворимые Нерастворимые
- 16. Средние соли – это продукты полного замещения атомов водорода в молекуле кислоты атомами металла или полного
- 17. Многие соли являются важным косметическим сырьем, например: хлорид натрия, карбонат и бикарбонат натрия, сульфит и бисульфит
- 18. Классификация органических соединений Гетероциклические Карбоциклические Углеродные атомы, соединенные в циклы Органические соединения, содержащие циклы, в состав
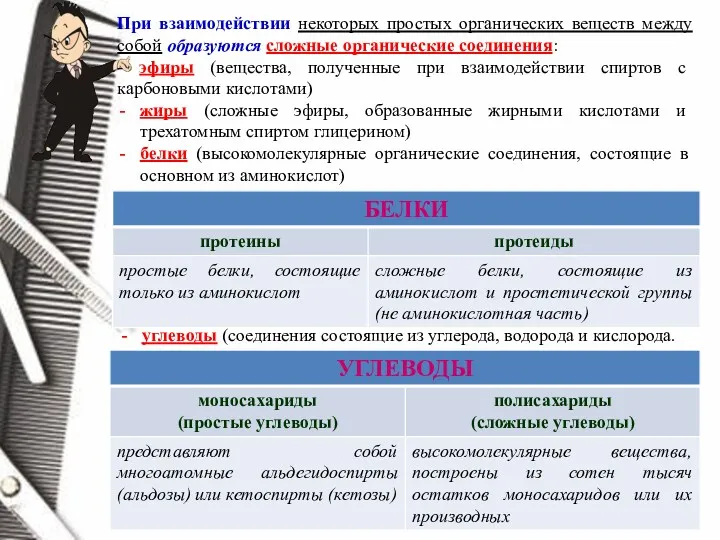
- 19. При взаимодействии некоторых простых органических веществ между собой образуются сложные органические соединения: - эфиры (вещества, полученные
- 21. Скачать презентацию










 Химия в жизни общества
Химия в жизни общества Organic molecules
Organic molecules Первичная переработка нефти
Первичная переработка нефти Состав газированной воды
Состав газированной воды Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома
Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома Галогены (солеобразующие)
Галогены (солеобразующие) Склад та властивості основних класів неорганічних сполук
Склад та властивості основних класів неорганічних сполук Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями
Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями Катионы 1, 2 аналитических групп
Катионы 1, 2 аналитических групп Углекислый газ
Углекислый газ Неон. Получение
Неон. Получение Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
 Химическая связь
Химическая связь Углеводы Cn(H2O)m
Углеводы Cn(H2O)m Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Типы химических реакций в органической химии
Типы химических реакций в органической химии СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ
СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Хімічні сполуки у побуті
Хімічні сполуки у побуті Основные классы неорганических веществ
Основные классы неорганических веществ Мир первозданной красоты. Природные уникумы Урала
Мир первозданной красоты. Природные уникумы Урала Химический элемент и вещество
Химический элемент и вещество Тема 1. Металлы и сплавы
Тема 1. Металлы и сплавы Влияние спирта на здоровье человека
Влияние спирта на здоровье человека Превращения веществ. Роль химии в жизни человека
Превращения веществ. Роль химии в жизни человека Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива
Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива