Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома презентация
Содержание
- 2. План урока Характеристика химического элемента железа по его положению в ПСХЭ и строению атома(самостоятельно) Нахождение в
- 3. Положение в Периодической системе
- 4. Строение атома С. О. : +2, +3
- 6. Получение Восстановление железа из его оксидов водородом при нагревании 3H2+ Fe2O3 = 3H2O + 2Fe Восстановление
- 7. Физические свойства Твердое Серо-серебристое Блестящее Хорошо проводит тепло и электрический ток Достаточно ковкое и пластичное Обладает
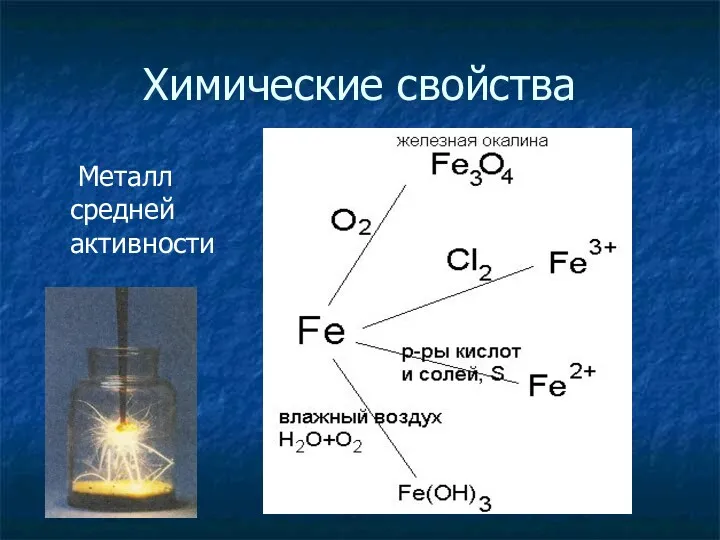
- 8. Химические свойства Металл средней активности
- 9. Химические свойства: 1. Взаимодействие с простыми веществами - неметаллами. Fe + S= FeS (при нагревании) 2Fe
- 10. Задание: воспользуйтесь информационными ресурсами и укажите области применения железа и его сплавов. Составьте схему: Fe
- 11. Биологическая роль железа. Заполните таблицу, используя дополнительные источники информации Какова роль железа в жизни человека и
- 13. Скачать презентацию









 Вода-растворитель. Работа воды в природе
Вода-растворитель. Работа воды в природе Бутадиеновые каучуки
Бутадиеновые каучуки Общая характеристика авиационных материалов, тенденции их развития
Общая характеристика авиационных материалов, тенденции их развития Водород
Водород Азотная кислота
Азотная кислота Периодический закон и Периодическая система химических элементов Д.И. Менделеева
Периодический закон и Периодическая система химических элементов Д.И. Менделеева Альдегиды и карбоновые кислоты
Альдегиды и карбоновые кислоты Углеводы. Общая характеристика углеводов
Углеводы. Общая характеристика углеводов Алкадиены
Алкадиены Атомы химических элементов
Атомы химических элементов Спирти. Історична довідка
Спирти. Історична довідка Минералогия литофильных редких элементов. Цирконий и гафний
Минералогия литофильных редких элементов. Цирконий и гафний Предмет и задачи химии. Вещества и их свойства (продолжение)
Предмет и задачи химии. Вещества и их свойства (продолжение) Additives for Polymeric Materials
Additives for Polymeric Materials Ионная химическая связь
Ионная химическая связь Основные свойства и механизмы упрочнения КМ
Основные свойства и механизмы упрочнения КМ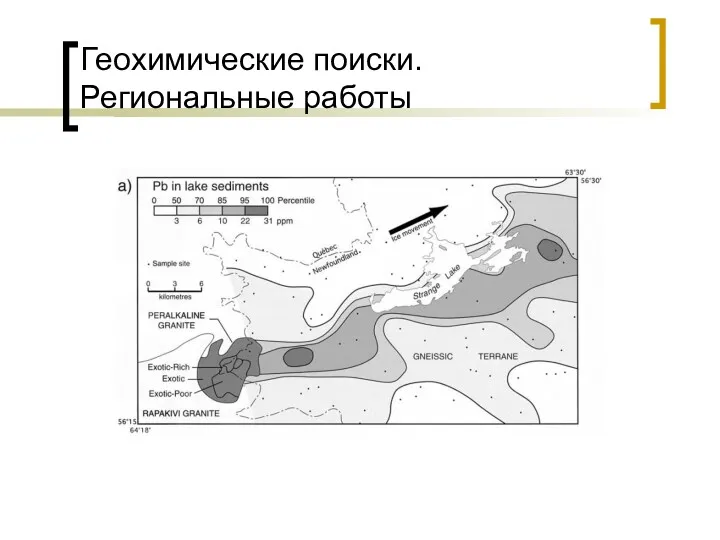 Геохимические поиски. Региональные работы
Геохимические поиски. Региональные работы Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров
Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров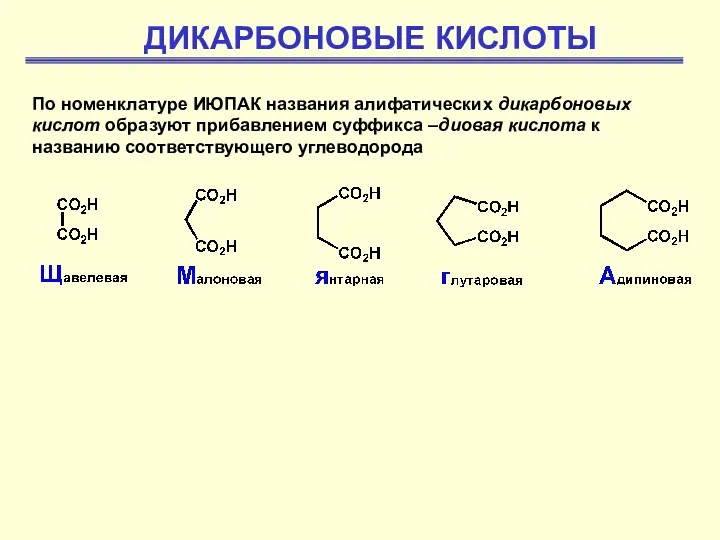 Дикарбоновые кислоты
Дикарбоновые кислоты Мыла и синтетические моющие средства
Мыла и синтетические моющие средства ПВХ
ПВХ Предмет аналитической химии, ее структура
Предмет аналитической химии, ее структура Азот и его соединения. Повторение
Азот и его соединения. Повторение Значення хімічних процесів у природі
Значення хімічних процесів у природі Органічні розчинники
Органічні розчинники Псевдоморфозы. Образование псевдоморфоз
Псевдоморфозы. Образование псевдоморфоз Расчеты по химическим уравнениям. 8 класс
Расчеты по химическим уравнениям. 8 класс Механические свойства минералов
Механические свойства минералов