Слайд 2

Повторение
1. Из каких элементарных частиц состоит атом?
2. Что показывает для
элемента его порядковый номер?
3. С чем совпадает номер периода?
4. С чем совпадает номер группы?
5. У какого элемента на третьем слое пять электронов?
6. Что с электронами в химических реакциях делают металлы?
7. Что с электронами в химических реакциях делают неметаллы?
Слайд 3
Начальная классификация элементов
Металлы Неметаллы
Переходные Инертные
элементы газы
Слайд 4

ТРИАДЫ ДЕБЕРЕЙНЕРА 1840 г.
Иоган Вольфанг Деберейнер – немецкий химик. Первая попытка
классификации.
Слайд 5
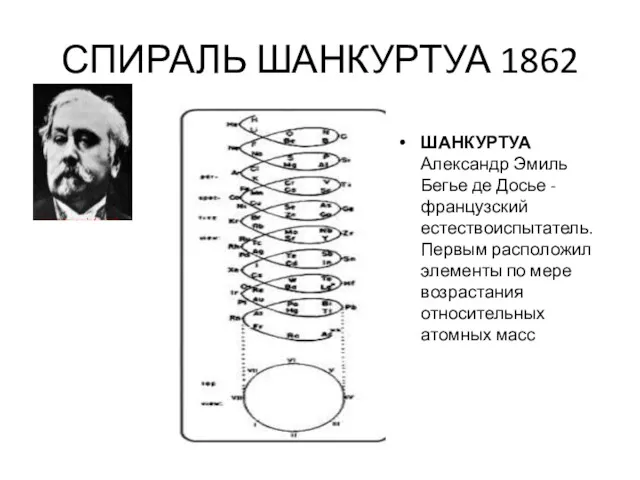
СПИРАЛЬ ШАНКУРТУА 1862
ШАНКУРТУА Александр Эмиль Бегье де Досье - французский естествоиспытатель.
Первым расположил элементы по мере возрастания относительных атомных масс
Слайд 6

ТАБЛИЦА МЕЙЕРА 1864
Юлиус Лотар Мейер – немецкий химик. Наряду с Менделеевым
считается создателем Периодической системы
Слайд 7

История открытия
S
Сера
Ar = 32
SO3 – кислотный оксид
H2SO4 - серная
кислота
H2S
Слайд 8
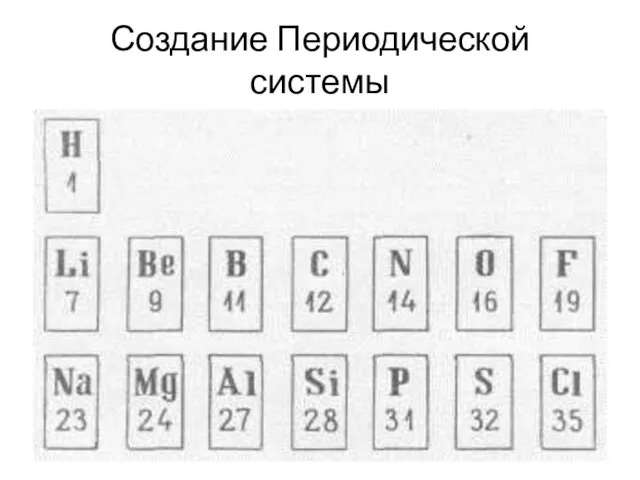
Создание Периодической системы
Слайд 9

Закономерности по горизонтали
Na Mg Al Si P S Cl Ar
24
27 28 31 32 35,5 40
+1 +2 +3 +4 +5 +6 +7 ----
Na2O MgO Al2O3 SiO2 P2O5 SO3 Cl2O7 ----
NaOH Mg(OH)2 Al(OH)3 H2SiO3 H3PO4 H2SO4 HClO4 ----
-4 -3 -2 -1 ----
SiH4 PH3 H2S HCl ----
В периодах заряд ядра увеличивается плавно
Число электронов на внешнем слое от 1 до 8
Металлические свойства……; неметаллические …….
+Основные свойства…………; кислотные свойства……
Слайд 10

Закономерности по вертикали
Li +3 )2)1 +1 Li2O LiOH
Na +11 )2)8)1 +1
Na2O NaOH
K +19 )2)8)8)1 +1 K2O KOH
В главных подгруппах заряд ядра увеличивается скачками
Число электронов на внешнем слое не меняется
Радиус атома……………
Металлические свойства ……
Неметаллические свойства……..
Степени окисления не изменяются
Основные свойства …….; кислотные свойства……..
Слайд 11

Формулировки периодического закона
Свойства химических элементов, так же как форма и свойства
их соединений находятся в периодической зависимости от массы атомов.
Д.И. Менделеев 1869 г.
Свойства химических элементов, так же как форма и свойства их соединений находятся в периодической зависимости от зарядов атомных ядер.
Слайд 12

Сравнение элементов по активности
План
Определяем, какие свойства надо сравнить металлические или
неметаллические (если элементы расположен с 1 по 3 группу, значит это металл, и мы сравниваем способность отдавать электроны; если с 4 по 7 группу, значит это неметаллы и мы сравниваем способность принимать электроны)
Определяем сколько слоев в каждом атоме и сколько электронов на внешнем слое.
Исходя из этого сравниваем способность отдавать или принимать электроны. Кто легче отдаст электроны, тот более сильный металл. Кто легче примет электроны, тот более сильный неметалл
Слайд 13

Сравнить по активности серу и хлор
Элементы расположены в 6 и 7
группе периодической системы, значит это неметаллы и мы должны сравнить способность принимать электроны
Записываю строение каждого атома S)2)8)6 Cl)2)8)7
Радиусы у атомов примерно одинаковы, только у серы на внешнем слое 6 электронов и принять ей надо 2 электрона, а у хлора на внешнем слое 7 электронов и принять ему надо только 1 электрон. Хлор легче примет электроны, а значит он более активен.
Слайд 14

Ответ на вопрос должен выглядеть так:
S)2)8)6 Cl)2)8)7
Хлор активней серы, так
как ему легче принять 1 электрон на 3 слой, чем сере принять 2 электрона на тот же слой
Слайд 15

Сравнить по активности бериллий и магний
Оба элемента во второй группе –
металлы. Сравниваем способность отдавать электроны.
Ве)2)2 Mg)2)8)2
У обоих металлов на внешнем слое по 2 электрона, только у магния 3 слоя, а значит у него больше радиус атома, электроны расположены дальше от ядра и отдать их ему будет легче, а значит он более сильный металл
Слайд 16

Ответ на вопрос должен выглядеть так:
Ве)2)2 Mg)2)8)2
Магний активней бериллия, потому
что ему легче отдать 2 электрона с третьего слоя, чем бериллию 2 электрона со второго слоя.















 Тема. Водородная связь
Тема. Водородная связь Анализ жидких средств для мытья посуды
Анализ жидких средств для мытья посуды Углерод. Аллотропные модификации
Углерод. Аллотропные модификации Материалы с малой плотностью
Материалы с малой плотностью Полимеры. Степень полимеризации
Полимеры. Степень полимеризации Застосування алканів
Застосування алканів Классы неорганических веществ
Классы неорганических веществ Индикаторы на кухне
Индикаторы на кухне Чисті речовини і суміші
Чисті речовини і суміші Синтетикалық пиретроидтар. Инсектицидтердің тиомочевиндер, нейтротоксиндер, гормоналды, авермектиндер, карбаматтар
Синтетикалық пиретроидтар. Инсектицидтердің тиомочевиндер, нейтротоксиндер, гормоналды, авермектиндер, карбаматтар Решение задач по теме: «Электролиз»
Решение задач по теме: «Электролиз» Углеводы. Урок по химии для 9 класса
Углеводы. Урок по химии для 9 класса Химическая промышленность России
Химическая промышленность России Кислоты. Состав и классификация кислот. Формулы и названия основных неорганических кислот
Кислоты. Состав и классификация кислот. Формулы и названия основных неорганических кислот Кривая охлаждения железа и структуры сплавов
Кривая охлаждения железа и структуры сплавов Основные классы неорганических соединений
Основные классы неорганических соединений Альбитит-грейзеновые месторождения
Альбитит-грейзеновые месторождения Жёсткость воды и способы её устранения. Практическая работа №6. 9 класс
Жёсткость воды и способы её устранения. Практическая работа №6. 9 класс Теория строения органического вещества. 10 класс
Теория строения органического вещества. 10 класс Катионы 1, 2 аналитических групп
Катионы 1, 2 аналитических групп Периодические системы химических элементов
Периодические системы химических элементов Токсикология пестицидов
Токсикология пестицидов Алкадиены
Алкадиены Электролитическая диссоциация. Реакции ионного обмена
Электролитическая диссоциация. Реакции ионного обмена Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей Нуклеозиды. Нуклеиновые кислоты
Нуклеозиды. Нуклеиновые кислоты Чипсы: польза или вред. Химия
Чипсы: польза или вред. Химия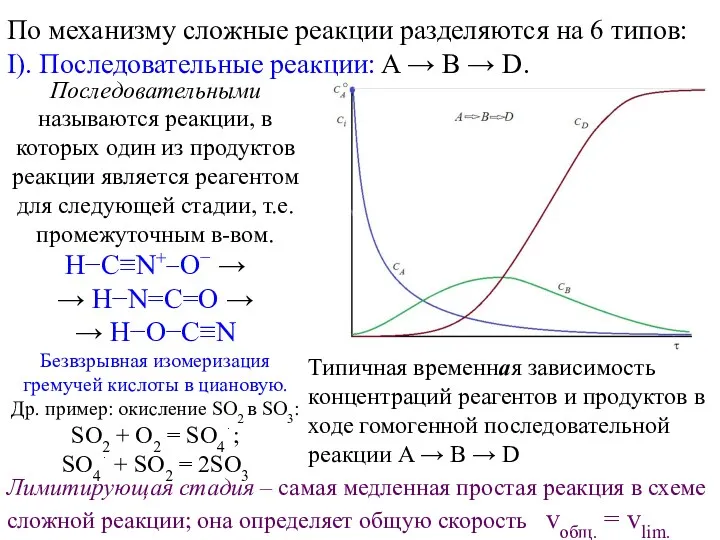 Сложные реакции по механизму
Сложные реакции по механизму