Содержание
- 2. 1.Понятие о спиртах. Если в молекулах У.В. атом водорода заместить на гидроксильную группу, то получатся соединения
- 3. Спиртами называются органические вещества, в которых гидроксильная группа связана с углеводородным радикалом. С2Н6 – этан; С2Н5
- 4. ОН – группа называется функциональной группой. Функциональной называется группа атомов, определяющая принадлежность вещества к определённому классу.
- 5. Запомним, друг, и я и ты, Чем отличаются спирты. В них углерод и гидроксид, И каждый
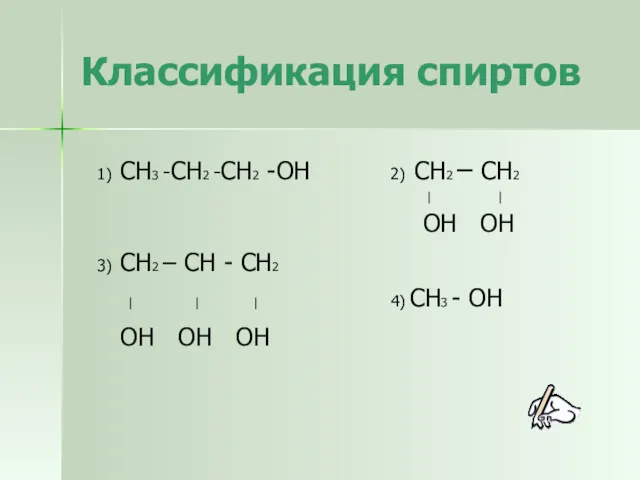
- 6. Классификация спиртов 1) СН3 -СН2 -СН2 -ОН 2) СН2 – СН2 | | ОН ОН 3)
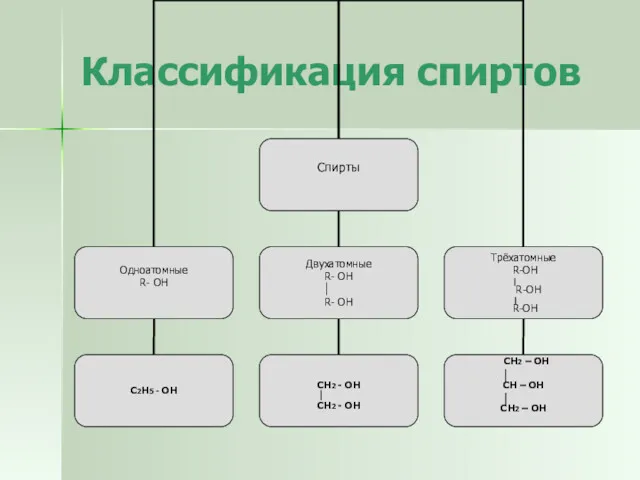
- 7. Классификация спиртов
- 8. Номенклатура спиртов. Задание 2. Просмотрите таблицу и сделайте вывод о номенклатуре спиртов
- 9. Номенклатура спиртов СН3 –СН-СН2-ОН СН2 – СН2 СН2 – СН - СН2 | | | |
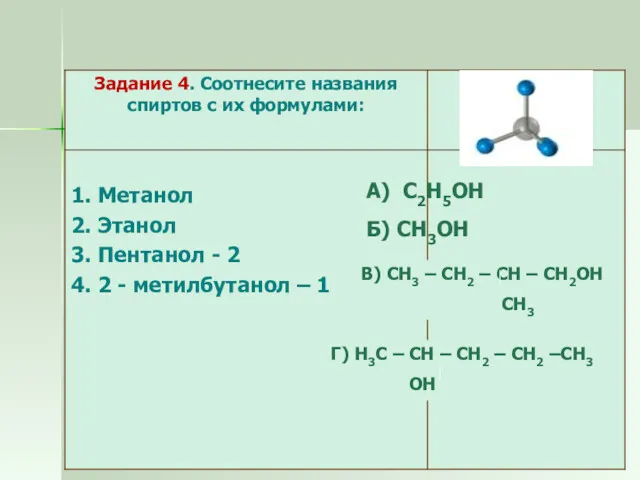
- 10. Г) Н3С – СН – СН2 – СН2 –СН3 ОН А) С2Н5ОН Б) СН3ОН В) СН3
- 11. Вывод Названия одноатомных спиртов образуются из названия углеводорода с самой длинной углеродной цепью, содержащей гидроксильную группу,
- 12. Одноатомный спирт - метанол Жидкость без цвета с температурой кипения 64С, характерным запахом Легче воды. Горит
- 13. Метанол - яд Ядовитое действие метанола основано на поражении нервной и сосудистой системы. Приём внутрь 5—10
- 14. Одноатомный спирт - этанол Бесцветная жидкость с характерным запахом и жгучим вкусом, температурой кипения78С. Легче воды.
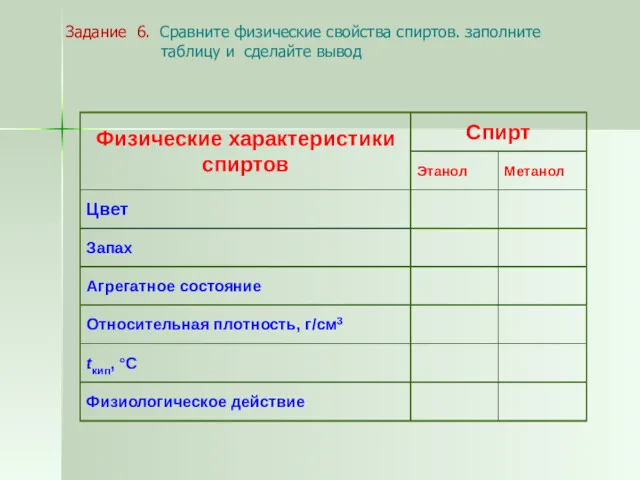
- 15. Задание 6. Сравните физические свойства спиртов. заполните таблицу и сделайте вывод
- 16. Запомни !
- 17. Химические свойства Горение спиртов (эксперимент). С2Н5ОН + 3О2 2СО2+ 3Н2О
- 18. Вывод Химические свойства спиртов определяются наличием функциональной группы - ОН.
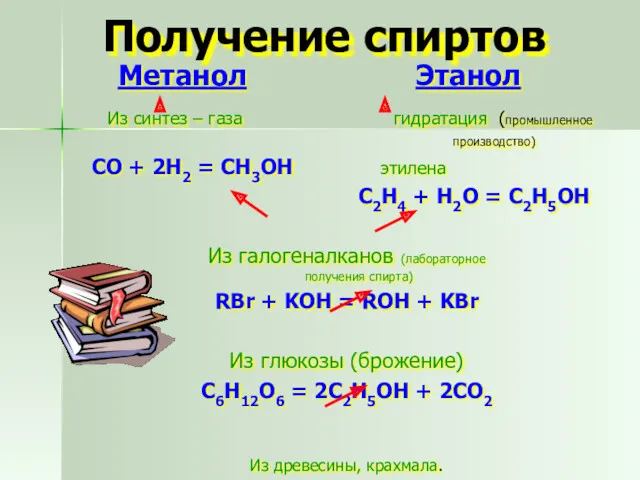
- 19. Получение спиртов Метанол Этанол Из синтез – газа гидратация (промышленное производство) СО + 2Н2 = СН3ОН
- 20. Применение этилового спирта Производство каучука (резины), исходя из спирта. Растворитель в лакокрасочной и химико-фармацевтической промышленности. Для
- 21. Этанол в косметике и парфюмерии— растворитель для духов и лосьонов.
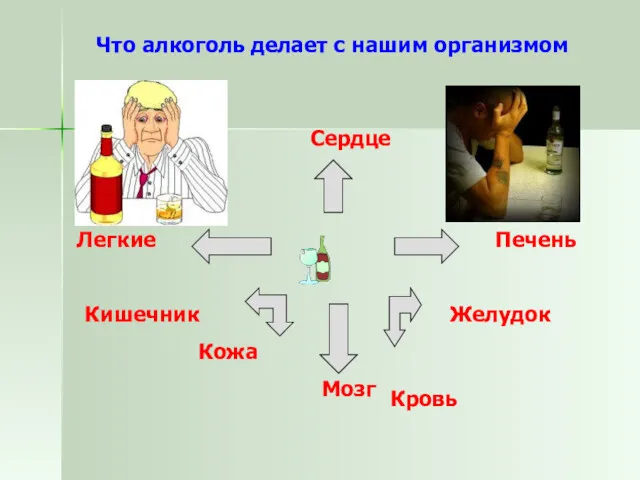
- 22. Что алкоголь делает с нашим организмом Мозг Кровь Печень Желудок Кишечник Легкие Сердце Кожа
- 23. Вредное воздействие этанола В начале опьянения страдают структуры коры больших полушарий; активность центров мозга, управляющих поведением,
- 24. Вредное воздействие этанола Изменения структуры мозга, вызванные многолетней алкогольной интоксикацией, почти необратимы, и даже после длительного
- 25. Вредное воздействие этанола Алкоголь крайне неблагоприятно влияет на сосуды головного мозга. В начале опьянения они расширяются,
- 26. Многоатомный спирт -этиленгликоль Этиленгликоль — представитель предельных двухатомных спиртов — гликолей. Название гликоли получили вследствие сладкого
- 27. Применение этиленгликоля Важным свойством этиленгликоля является способность понижать температуру замерзания воды, от чего вещество нашло широкое
- 28. Этиленгликоль - яд Дозы вызывающие смертельное отравление этиленгликолем варьируются в широких пределах - от 100 до
- 29. Многоатомный спирт - глицерин Глицерин – трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная, сладкая на вкус жидкость.
- 30. Применение глицерина Применяется в производстве взрывчатых веществ нитроглицерина. При обработке кожи. Как компонент некоторых клеёв. При
- 31. Качественная реакция на многоатомные спирты
- 33. Скачать презентацию
























 Химия в жизни общества
Химия в жизни общества Organic molecules
Organic molecules Первичная переработка нефти
Первичная переработка нефти Состав газированной воды
Состав газированной воды Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома
Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома Галогены (солеобразующие)
Галогены (солеобразующие) Склад та властивості основних класів неорганічних сполук
Склад та властивості основних класів неорганічних сполук Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями
Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями Катионы 1, 2 аналитических групп
Катионы 1, 2 аналитических групп Углекислый газ
Углекислый газ Неон. Получение
Неон. Получение Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
 Химическая связь
Химическая связь Углеводы Cn(H2O)m
Углеводы Cn(H2O)m Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Типы химических реакций в органической химии
Типы химических реакций в органической химии СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ
СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Хімічні сполуки у побуті
Хімічні сполуки у побуті Основные классы неорганических веществ
Основные классы неорганических веществ Мир первозданной красоты. Природные уникумы Урала
Мир первозданной красоты. Природные уникумы Урала Химический элемент и вещество
Химический элемент и вещество Тема 1. Металлы и сплавы
Тема 1. Металлы и сплавы Влияние спирта на здоровье человека
Влияние спирта на здоровье человека Превращения веществ. Роль химии в жизни человека
Превращения веществ. Роль химии в жизни человека Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива
Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива