Содержание
- 2. План лекції: Актуальність теми. Епідеміологія анемій. Показники крові у дітей різного віку. Класифікація анемій. Залізодефіцитні анеміі.
- 3. Епідеміологія анемій Анемії є досить розповсюдженим захворюванням у дітей і, особливо, залізодефіцитна анемія. За даними ВООЗ
- 4. ЕРИТРОЦИТИ норма – у новонароджених – 3,9-5,5 Т/л, у малюків – 3,5-5,5 Т/л, у старших дітей
- 5. 1. Кольоровий показник – Нв х 3 / Ер х 100 - в нормі 0,85-1,05 2.
- 6. МСV (Мean Сorpuscular Volume) – середній об’єм еритроцита. Значення, що знаходяться в межах 80-100 фл (фемтолітр
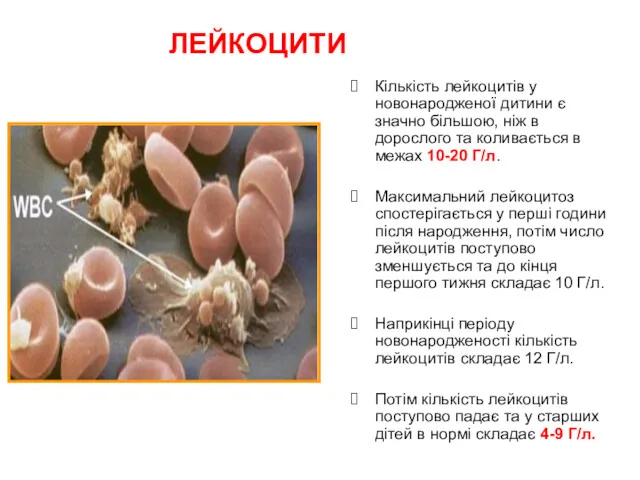
- 7. ЛЕЙКОЦИТИ Кількість лейкоцитів у новонародженої дитини є значно більшою, ніж в дорослого та коливається в межах
- 8. ФІЗІОЛОГІЧНІ ПЕРЕХРЕСТИ І перехрест 5-7 день ІІ перехрест 5-6 рік
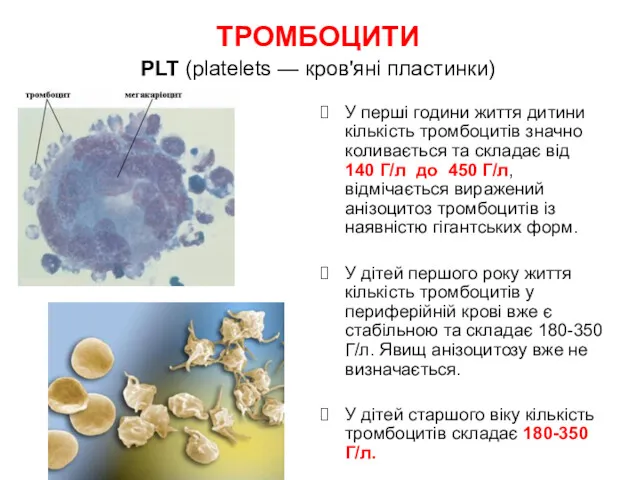
- 9. ТРОМБОЦИТИ PLT (platelets — кров'яні пластинки) У перші години життя дитини кількість тромбоцитів значно коливається та
- 10. Анемії Анемії – це група захворювань, які характеризуються зниженням в одиниці об'єму крові вмісту гемоглобіну та
- 11. Класифікація анемій Анемії внаслідок порушення кровотворення: Дефіцитні (залізо-, білково-, вітаміно-) Апластичні (вроджені та набуті; з ураженням
- 12. ЗАЛІЗОДЕФІЦИТНА АНЕМІЯ Залізодефіцитна анемія – патологічний стан, що характеризується зниженням вмісту гемоглобіну через дефіцит заліза в
- 13. ЗАЛІЗОДЕФІЦИТНА АНЕМІЯ Виникнення залізодефіцитних анемій залежить від багатьох факторів: бідності депо (порушення трансплацентраної передачі заліза, недоношеність,
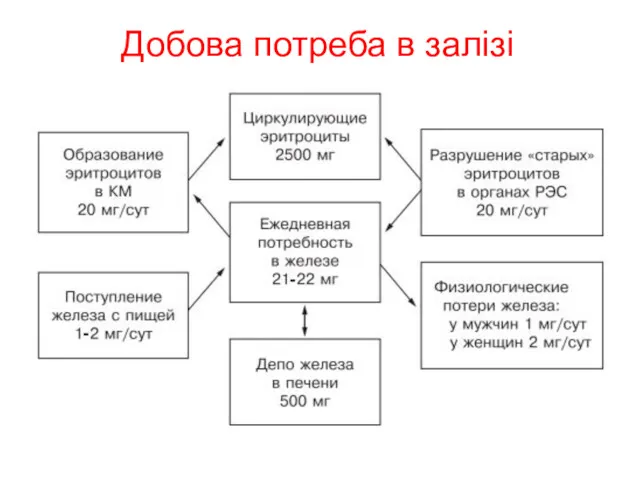
- 14. Добова потреба в залізі
- 15. Добова потреба в залізі для різних вікових груп Вагітні Жінки Чоловіки Підлітки Діти Малюки 0,5-1,0 1,0
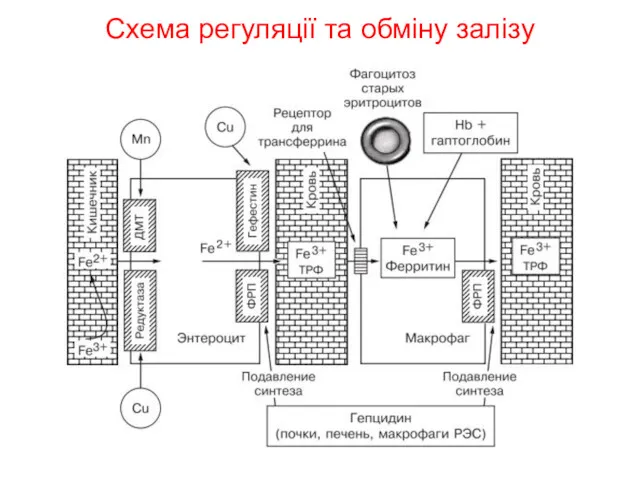
- 16. У організмі здорової людини міститься приблизно 3-5 г заліза (приблизно 35 мг/кг). Залізо, яке міститься в
- 17. Схема регуляції та обміну залізу
- 18. Розвиток дефіциту заліза має чітку стадійність: Схильність до розвитку дефіциту заліза (вегетаріанство, підлітковий вік, наявність хронічних
- 19. При латентному (скритому) дефіциті заліза на фоні дефіциту заліза у тканинних депо зменшується його транспортний фонд,
- 20. Розвиток дефіциту заліза
- 21. Виокремлюють наступні стадії ЗДА: · регенераторну - характеризується збільшенням синтеза еритрицитів у відповідь на гіпоксію, пов’язану
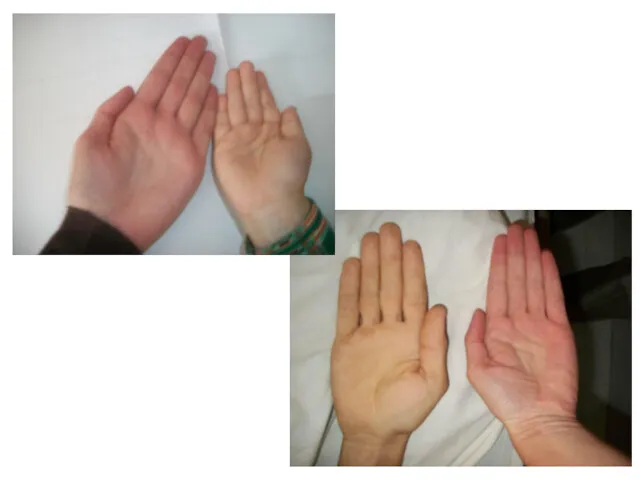
- 22. Скарги при ЗДА ПРОЯВИ ГІПОКСІЇ Слабкість Підвищена стомлюваність Задишка Серцебиття Головний біль Запаморочення Порушення сну Зниження
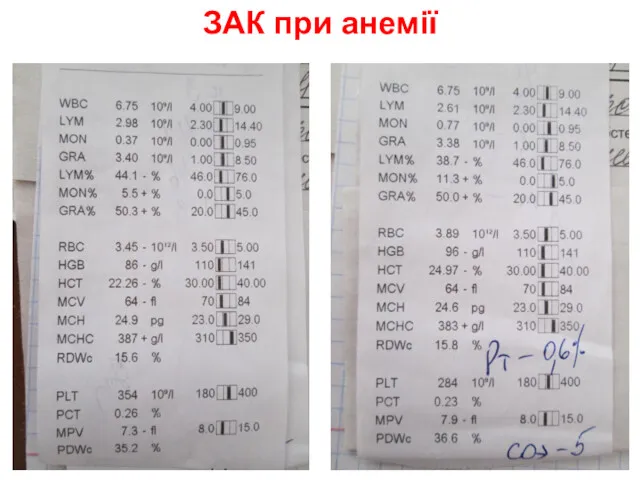
- 24. 1. Зниження вмісту гемоглобіну та еритроцитів у крові дитини; 2. Зниження середнього вмісту гемоглобіну в еритроциті
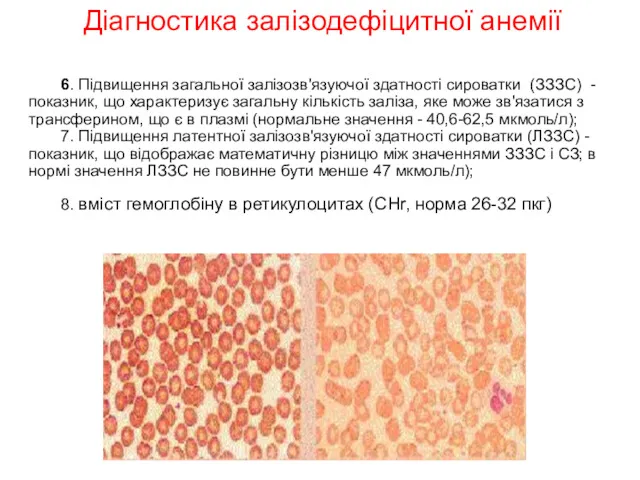
- 25. 6. Підвищення загальної залізозв'язуючої здатності сироватки (ЗЗЗС) - показник, що характеризує загальну кількість заліза, яке може
- 26. Діагностика залізодефіцитної анемії
- 27. ЗАК при анемії
- 28. Згідно Протоколу лікування ЗДА у дітей (Наказ МОЗ України № 9 від 10.01.2005 р.) основними принципами
- 29. У клітинах слизової оболонки кишок залізо утворює комплекс із білком апоферитином, а потім переходить у феритин,
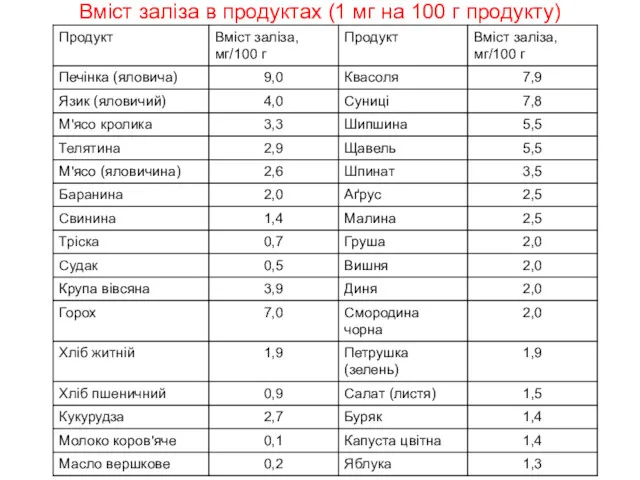
- 30. Вміст заліза в продуктах (1 мг на 100 г продукту)
- 31. В середньому добову лікувальну дозу ділять на 3 прийоми. Більші дози не підвищують ефективність лікування, але
- 32. Препаратами заліза, які використовуються для в/м введення, – ферум-лек, мальтофер (в 1 ампулі препарату міститься 100
- 33. Показаннями до застосування препаратів заліза парентерально є: - непереносимість препаратів заліза при пероральному застосуванні; стани після
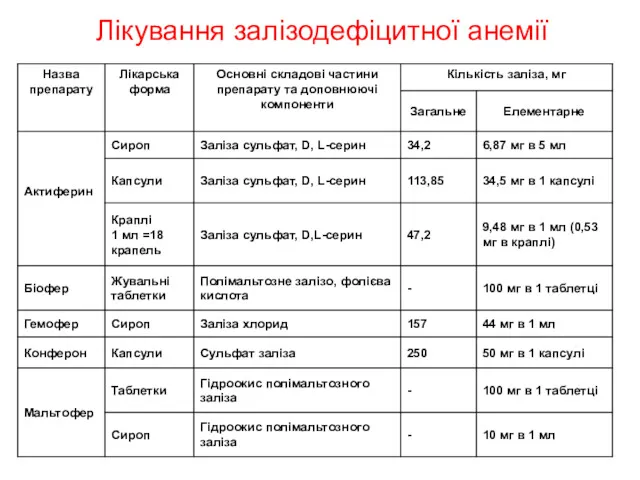
- 34. Лікування залізодефіцитної анемії
- 35. Контроль ефективності лікування ЗДА Ферротерапія може бути проконтрольована за наступними показниками: Ретикулоцитарна реакція на 10-12 день
- 36. Симптоми отруєння залізом Інтоксикація розвивається при пероральному прийомі чистого заліза в дозі більше 60 мг/кг. Смертельна
- 37. Отруєння залізом Невідкладна терапія: промивання шлунку; молоко, яєчний білок; ентеросорбенти, сольові послаблювальні; при прийомі смертельної дози
- 38. Профілактика ЗДА (Американська колегія педіатрії) Недоношені немовлята (гестаційний вік Доношеним немовлятам на виключно грудному вигодовуванні рекомендується
- 39. Клінічний приклад Дівчинка Валентина, 2 роки 3 міс., знаходилася з 23.01.2012 р. на лікуванні в онкогематологічному
- 40. Клінічний приклад Дівчинка Наталя, 2 роки 8 міс., знаходилася з 22.02.2012 р. на лікуванні в онкогематологічному
- 41. Гостра постгеморагічна анемія пов'язана з одноразовою масивною крововтратою. Швидка втрата 10-25% крові у новонароджених викликає симптоми
- 42. Хронічна постгеморагічна анемія - пов'язана з немасивними кровотечами, що тривало повторюються. Етіологія: у новонароджених фетоматеринські трансфузії,
- 43. Гемолітичні анемії Гемолітичні анемії – група захворювань, що супроводжуються патологічно підвищеним руйнуванням еритроцитів, тобто скороченням тривалості
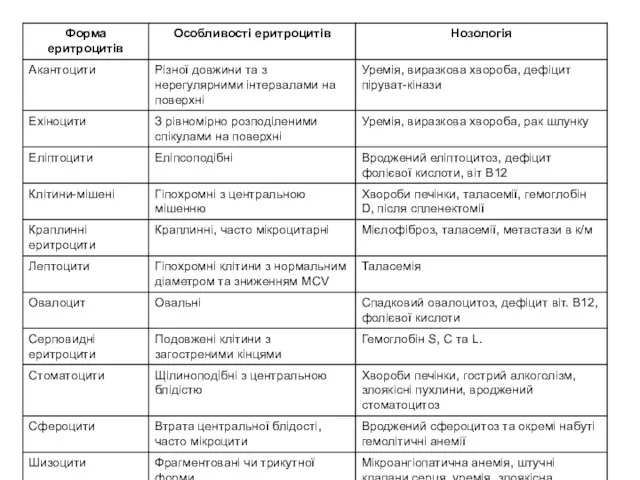
- 44. Класифікація ГА (Р.Е. Берман, В.К. Воган (1994)) I. Вроджені гемолітичні анемії (зумовлені внутрішньо-еритроцитарними аномаліями): Вроджені гемолітичні
- 45. II. Набуті гемолітичні анемії (повязані з зовнішніми екстраеритроцитарними факторами): а. Гемолітичні анемії, пов'язані з дією пасивно
- 46. Спадкова сфероцитарна анемія типу Мінковського-Шоффара Найбільш поширена форма спадкових гемолітичних анемій без порушення гемоглобіну. Хвороба передається
- 47. КЛІНІКА захворювання проявляється уже в ранньому віці. Класична картина анемії проявляється у кінці дошкільного віку. Перебіг
- 48. Внаслідок постійного напруження у роботі кісткового мозку в дітей з хронічною ГА час від часу можуть
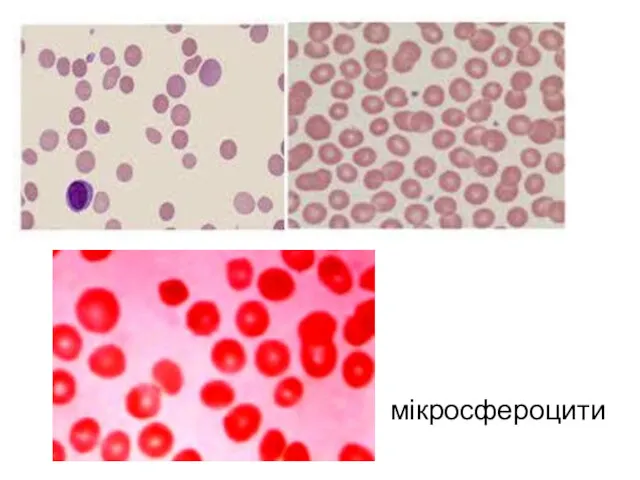
- 49. У аналізі крові відмічається анемія, ретикулоцитоз, підвищується рівень непрямого білірубіну. Морфологічне дослідження виявляє зменшення середнього діаметру
- 50. мікросфероцити
- 51. ВИЗНАЧЕННЯ ОСМОТИЧНОЇ РЕЗИСТЕНТНОСТІ ЕРИТРОЦИТІВ ОСМОТИЧНА РЕЗИСТЕНТНІСТЬ: Новонароджені - максимальна = 0,36-0,4%, мінімальна = 0,48-0,52% Старші діти
- 52. Диференціальний діагноз. Анемія Мінковського-Шоффара може проявлятися уже в неонатальному періоді, і тоді потребує диференціальної діагностики з
- 53. ЛІКУВАННЯ: 1. Консервативне лікування у період гемолітичного кризу - боротьба з білірубіновою інтоксикацією: крапельні вливання 10%
- 54. Клінічний приклад Хлопчик 7 років. Скарги на блідість, слабкість, запаморочення, біль та тяжкість у підребер'ях. За
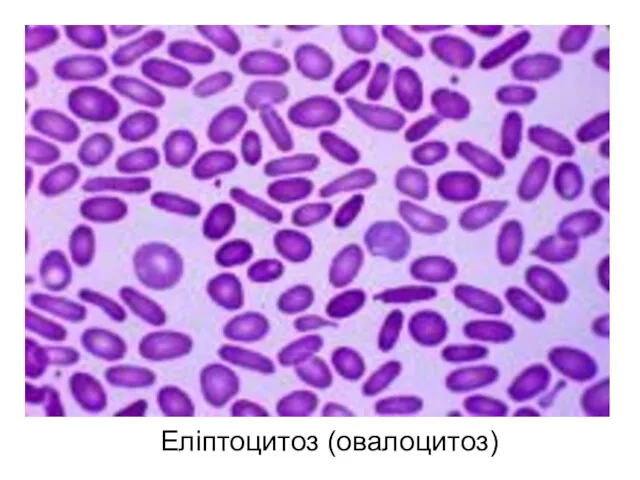
- 56. Еліптоцитоз (овалоцитоз)
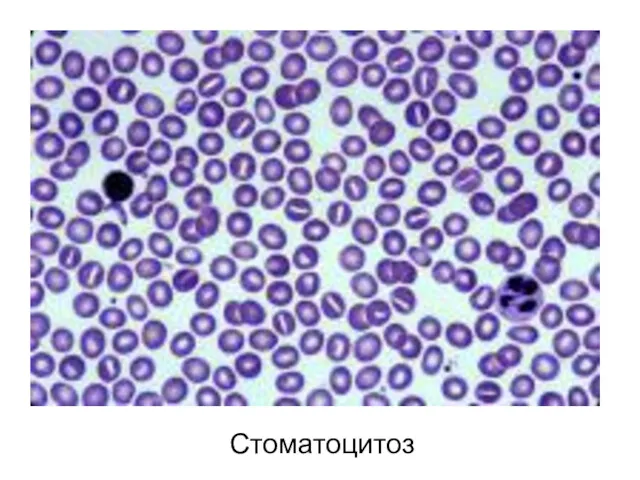
- 57. Стоматоцитоз
- 58. ФЕРМЕНТОПАТІЇ Цю групу ГА називають вродженими несфероцитарними ГА, оскільки при них відсутній сфероцитоз і не змінюється
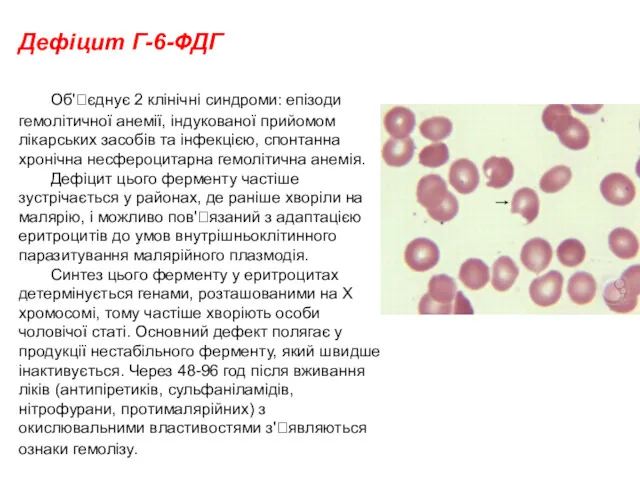
- 59. Дефіцит Г-6-ФДГ Об'єднує 2 клінічні синдроми: епізоди гемолітичної анемії, індукованої прийомом лікарських засобів та інфекцією, спонтанна
- 60. Серед гемолітичних анемій досить поширені анемії, зумовлені дією хімічних речовин та отрут (свинець, бензол, мідь, оцтова
- 61. Гемоглобінопатії (ГП) – генетично зумовлені стани, пов'язані з порушенням синтезу гемоглобіну або амінокислотного складу у структурі
- 62. ТАЛАСЕМІЯ Гетерогенне спадкове захворювання, що об'єднує групу гіпохромних анемій, яке умовно поділяють на велику таласемію (тяжка
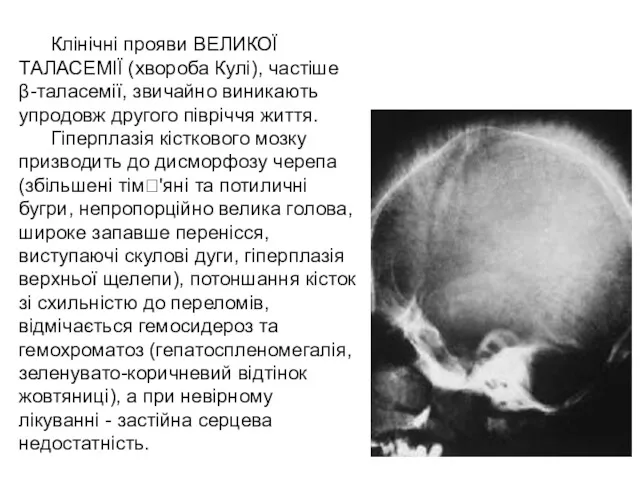
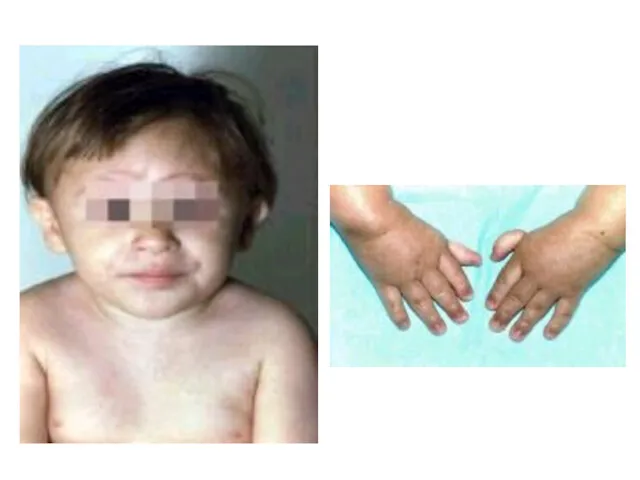
- 63. Клінічні прояви ВЕЛИКОЇ ТАЛАСЕМІЇ (хвороба Кулі), частіше β-таласемії, звичайно виникають упродовж другого півріччя життя. Гіперплазія кісткового
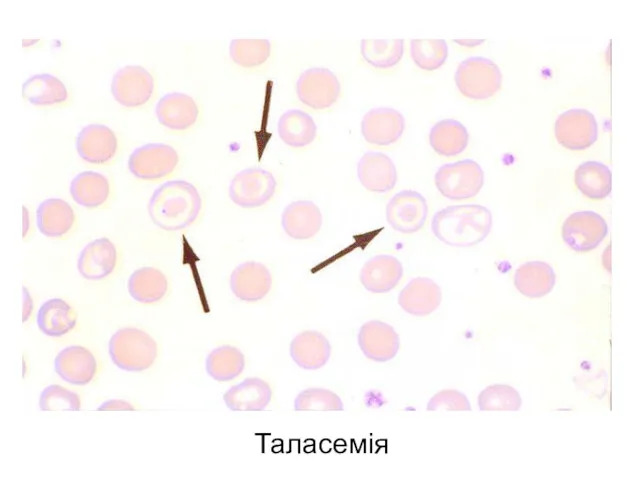
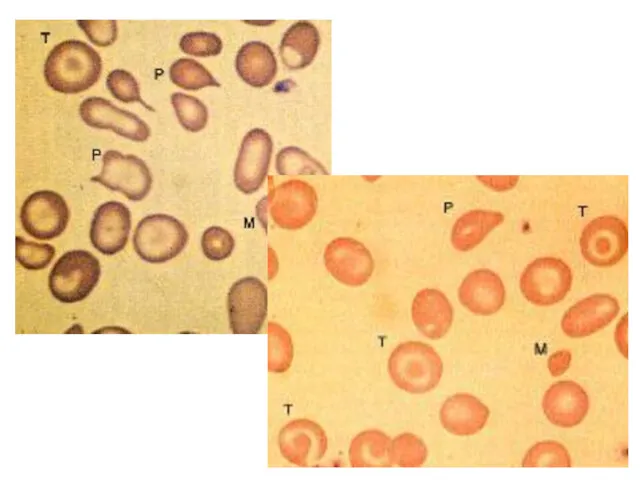
- 64. Аналіз крові характеризується гіпохромною, мікроцитарною анемією, наявністю тілець Гейнца, пойкілоцитозом, анізоцитозом, поліхромією, ретикулоцитозом, мішенеподібними еритроцитами, підвищенням
- 65. Таласемія
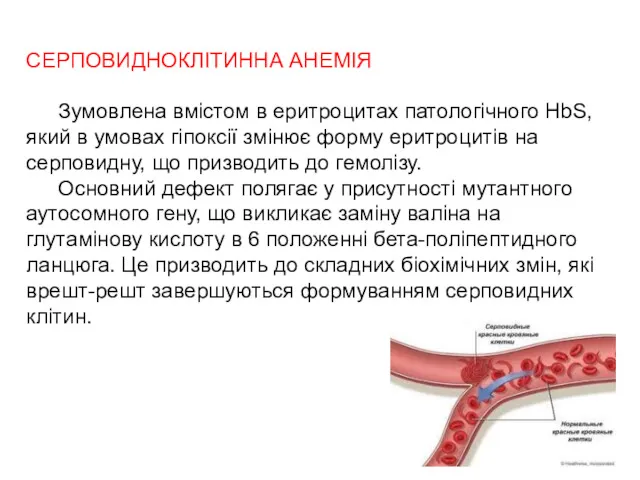
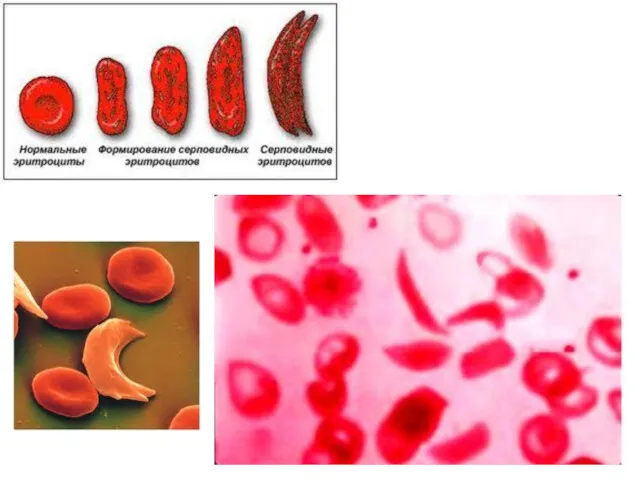
- 67. СЕРПОВИДНОКЛІТИННА АНЕМІЯ Зумовлена вмістом в еритроцитах патологічного HbS, який в умовах гіпоксії змінює форму еритроцитів на
- 68. Перебіг хвороби характеризується больовими приступами, пов'язаними з оклюзією дрібних кровоносних судин у результаті спонтанного "серпління" еритроцитів
- 70. У крові відмічається нормохромна анемія з рівнем гемоглобіну 50-90 г⁄л, ретикулоцитоз, серповидні еритроцити, нормобласти з тільцями
- 71. ПРОФІЛАКТИКИ гемолітичних анемій немає. Існує лише профілактика гемолітичних кризів, які найбільш часто провокуються інтеркурентною інфекцією. У
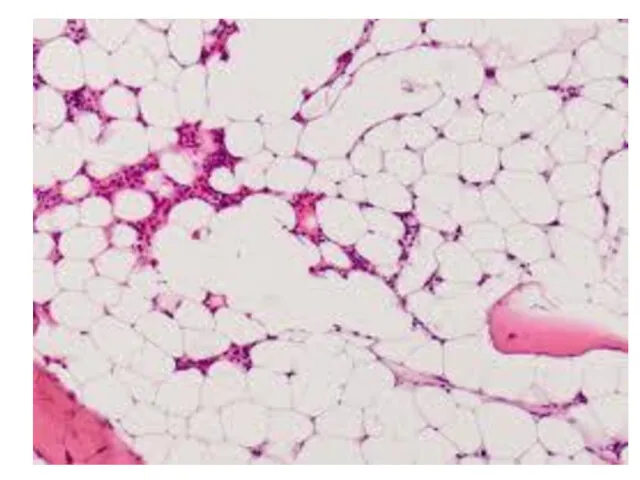
- 72. Апластична анемія – це захворювання, провідною клінічною рисою якого є периферична панцитопенія, що супроводжується зниженням клітинності
- 73. В основі патогенезу захворювання лежить ураження гемоцитопоезу на рівні ранніх клітин-попередників, що приводить до порушення еритро-,
- 74. Апластична анемія – це захворювання, провідною клінічною рисою якого є периферична панцитопенія, що супроводжується зниженням клітинності
- 76. Аналіз периферичної крові демонструє панцитопенію зі збереженням рівня лімфоцитів; характерним є одночасне зниження рівню гемоглобіну (
- 77. За ступенем тяжкості: - середньо-тяжка форма – гранулоцити більше 0,5х109/л, ретикулоцитів більше 1%, при проведенні стернальної
- 79. Лікування апластичної анемії повинно призначатись залежно від ступеню тяжкості процесу і тільки після здійснення повного обсягу
- 80. При тяжкій / дуже тяжкій формі АА пацієнти, які мають HLA-ідентичного сімейного донора повинні отримати трансплантацію
- 81. За відсутності відповіді або при рецидиві захворювання у пацієнтів з тяжкою АА призначається повторний курс імуносупресивної
- 82. Клінічний приклад Дитина Владислав, 9 років, знаходиться з 20.02.2012 р. на лікуванні в онкогематологічному відділенні. Дитина
- 83. Анемії ІВХДВ Важка анемія Важка анемія – стан, що вимагає госпіталізації та переливань компонентів крові. Характеризується
- 84. Анемії ІВХДВ У наступних ситуаціях потрібне переливання крові : • Hb • Hb 4-6 г/ дл
- 85. Література: Бережной В.В., Корнева В.В., Унич Н.К. Железодефицитные анемии в детском возрасте // Журнал практичного лікаря.
- 87. Скачать презентацию





























































 Основы сердечно-легочной реанимации
Основы сердечно-легочной реанимации Ящур. Пути передачи
Ящур. Пути передачи Кожные проявления при ВИЧ-инфекции коинфекции ВИЧ/ВГ
Кожные проявления при ВИЧ-инфекции коинфекции ВИЧ/ВГ Психологическое консультирование клиентов, имеющих специфические проявления личности
Психологическое консультирование клиентов, имеющих специфические проявления личности Импетиго стрептококковое, простой лишай, вульгарная эктима
Импетиго стрептококковое, простой лишай, вульгарная эктима Оценка функции почек с помощью биохимических маркеров
Оценка функции почек с помощью биохимических маркеров Возбудитель чумы
Возбудитель чумы Определение ПСА в диагностике рака предстательной железы. Индекс здоровья простаты
Определение ПСА в диагностике рака предстательной железы. Индекс здоровья простаты Оказание первой помощи при отсутствии сознания, остановке дыхания и кровообращения
Оказание первой помощи при отсутствии сознания, остановке дыхания и кровообращения Планирование семьи. Контрацепция
Планирование семьи. Контрацепция Суға бату кезіндегі көмек
Суға бату кезіндегі көмек Оперативный доступ к шее при флегмонах и абсцессах
Оперативный доступ к шее при флегмонах и абсцессах Болезни почек и мочевыводящих путей у пациентов пожилого и старческого возраста
Болезни почек и мочевыводящих путей у пациентов пожилого и старческого возраста Вакцинопрофилактика гриппа и пневмококковой инфекции
Вакцинопрофилактика гриппа и пневмококковой инфекции Үшкіл нерв. Бет нерві
Үшкіл нерв. Бет нерві Здоровье и болезнь. Факторы, определяющие здоровье. Методика сбора анамнеза. Периоды детского возраста. Оценка здоровья
Здоровье и болезнь. Факторы, определяющие здоровье. Методика сбора анамнеза. Периоды детского возраста. Оценка здоровья Клиническая анатомия слабых мест передней брюшной стенки и диафрагмы
Клиническая анатомия слабых мест передней брюшной стенки и диафрагмы Синдром менингита, отек-набухание головного мозга
Синдром менингита, отек-набухание головного мозга Противоэпидемические мероприятия
Противоэпидемические мероприятия Наркоз (общее обезболивание)
Наркоз (общее обезболивание) Мотивация выбора врачебной деятельности
Мотивация выбора врачебной деятельности Реабилитация при динамической афазии
Реабилитация при динамической афазии Наложение и снятие швов
Наложение и снятие швов Балалар мен жасөспірімдерге арналған бөлмелердің ауа температурасын анықтау әдістері
Балалар мен жасөспірімдерге арналған бөлмелердің ауа температурасын анықтау әдістері Диссеминированное внутрисосудистое свертывание крови
Диссеминированное внутрисосудистое свертывание крови Проблема вкусовой привлекательности рациона при ХБП и способы ее повышения
Проблема вкусовой привлекательности рациона при ХБП и способы ее повышения Глiкозиди. Глiкозиди кардiотонiчної дiї (серцевi глiкозиди). Лікарські рослини
Глiкозиди. Глiкозиди кардiотонiчної дiї (серцевi глiкозиди). Лікарські рослини Что нужно изменить в казахстанском протоколе?
Что нужно изменить в казахстанском протоколе?