Содержание
- 2. Нормативная документация Закон РФ № 52 «О санитарно-эпидемиологическом благополучии населения»1999г.,доп.2001,2004гг. СанПиН 2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям,
- 3. МУ 3.1.2313-08 «Требования к обеззараживанию, уничтожению и утилизации шприцев инъекционных однократного применения» ОСТ 4221-2-85 «Стерилизация и
- 4. от 18.06.01 № 77-ФЗ «О предупреждении распространения туберкулеза в РФ» (с изменениями от 22.08.04 г.) СП
- 5. СП 3.1.1275-03 «Профилактика инфекционных заболеваний при эндоскопических манипуляциях» МУ 3.5.1937-04 «Очистка, дезинфекция и стерилизация эндоскопов и
- 6. Дезинфекция Дезинфекция - это уничтожение патогенных и условно-патогенных микроорганизмов в окружающей среде, на объектах оборудования и
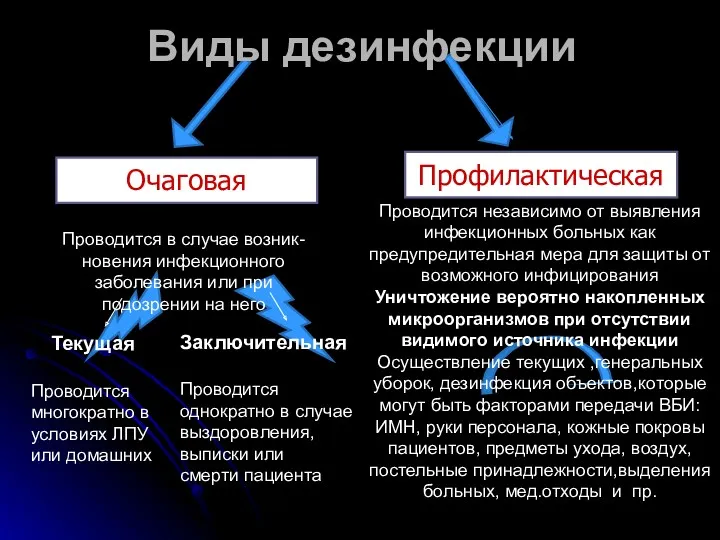
- 7. Проводится независимо от выявления инфекционных больных как предупредительная мера для защиты от возможного инфицирования Уничтожение вероятно
- 8. МЕТОДЫ ДЕЗИНФЕКЦИИ Механический – основан на удалении микроорганизмов(стирка, мытье, влажная уборка, проветривание, удаление пылесосом) Физический –
- 9. Изделия медицинского назначения (ИМН) после применения подлежат дезинфекции независимо от дальнейшего их использования ИМН однократного применения
- 12. Дезинфекцию можно проводить физическими и химическими методами. Выбор зависит от особенностей изделия и его назначения. Физический
- 13. Химический метод Для дезинфекции применяют ДС, обладающие широким спектром антимикробного действия, удобные в использование, малоопасные (4
- 14. Замачивание ИМН производится в емкости с крышками, погружение в рабочий раствор средства с заполнением каналов и
- 15. В ЛПУ должен быть не менее чем месячный запас разнообразных ДС различного химического состава и назначения
- 16. По химическому составу ДС распределяются по АДВ Хлорсодержащие /хлорамин, хлормикс,хлормисепт, жавель, деохлор, главхлор/ Кислородсодержащие /перекись водорода
- 17. 4.ЧАСы /четвертично-аммониевые соединения/ гуанидины, амины, ПАВы- Тетрамин, Авансепт, Диабак, Люмакс, Мистраль, Альфадез, Трилокс, Петролайт, Деобактер,Венделин,Бионса,Приоль,Стерибак. 5.
- 19. Новые препараты группы ЧАС+гуанидины : Авирайт, Десам Экстра, Бактол, Телесфор, Централь, Эквивалент, Эмиталь гарант, Амиксидин, Фрисепт-гамма,Анавидин-комплит
- 20. В целях предупреждения возможного формирования резистентных /устойчивых/ к ДС госпитальных штаммов микроорганизмов следует проводить мониторинг устойчивости
- 21. Выбор режимов дезинфекции ДС, применяемые в ЛПУ должны быть разрешены к применению в РФ и иметь
- 22. Режимы применения ДС Бактериальный ( кишечные, капельные, гнойно-септические ) Вирусный (гемоконтактные гепатиты, ВИЧ-инфекция) Туберкулез Кандидозы Дерматофитии
- 23. ДС для обработки эндоскопов и инструментов к ним Инструтон Е, Ника-дез, Ника-неодез, Абсолюцид форте, Тримицин-ЭМ, Мистраль,
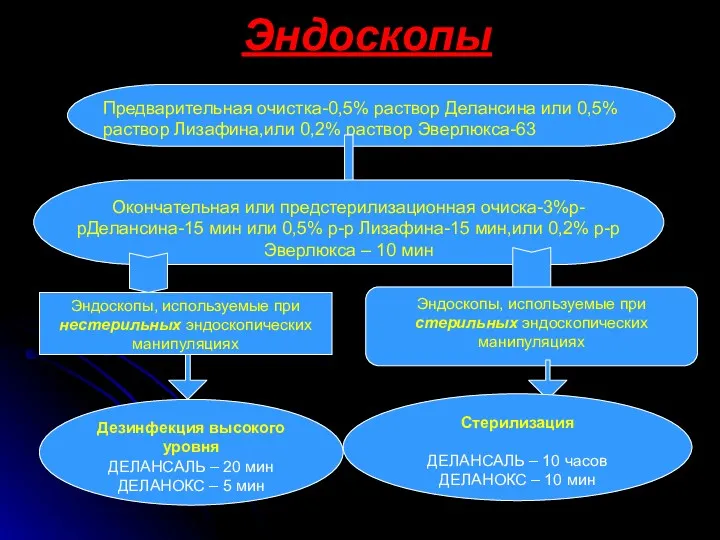
- 24. Эндоскопы Предварительная очистка-0,5% раствор Делансина или 0,5% раствор Лизафина,или 0,2% раствор Эверлюкса-63 Окончательная или предстерилизационная очиска-3%р-рДелансина-15
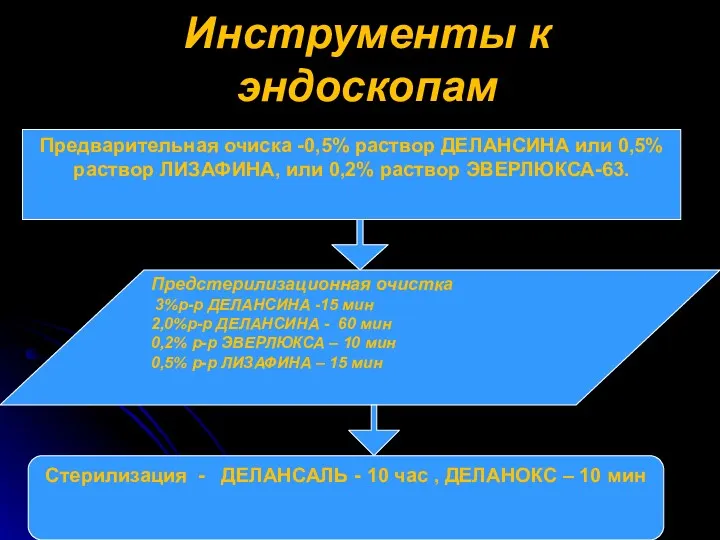
- 25. Инструменты к эндоскопам Предварительная очиска -0,5% раствор ДЕЛАНСИНА или 0,5% раствор ЛИЗАФИНА, или 0,2% раствор ЭВЕРЛЮКСА-63.
- 26. Выбор режимов для дезинфекции ИМН проводят по наиболее устойчивым микроорганизмам – между вирусами и грибами рода
- 27. Хранение ДС допускается только в специально отведенных местах, в оригинальной упаковке производителя, отдельно от лекарственных средств,
- 28. Классификация обеззараживаемых объектов предложена в 1968 г. в зависимости от риска передачи инфекции Э.Сполдингом
- 29. В целях более четкого определения рисков передачи инфекций при контакте с различными поверхностями оригинальная классификация Э.Сполдинга
- 30. Дезинфекция высокого уровня \ДВУ/ разрушает все микроорганизмы, за исключением бактериальных спор в большом количестве. Дезинфекция промежуточного(среднего)
- 31. Предстерилизационная очистка Цель – удаление с ИМН любых неорганических и органических загрязнений (включая белковые, жировые, механические
- 32. Предстерилизационная очистка осуществляется в качестве самостоятельного процесса после дезинфекции или при совмещении с ней в один
- 33. Условия проведения Централизованно / в ЦСО / Децентрализованно /при отсутствии ЦСО в ЛПУ) По способу проведения
- 34. Контроль ПСО Качество ПСО оценивают путем постановки азопирамовой или амидопириновой проб на наличие остаточных количеств крови
- 35. Контроль качества проводят ежедневно Контролю подлежит 1 % изделий каждой партии, но не менее 3 ед.
- 36. МУ 287-113 Приготовление реактива азопирам. Перед постановкой пробы готовят реактив азопирам, смешивая равные объемные количества исходного
- 37. Стерилизация Метод уничтожения всех форм патогенных и непатогенных микроорганизмов, включая споры Стерилизации подвергаются все ИМН, контактирующие
- 38. Методы стерилизации Радиационный – стерилизация в промышленных условиях Термический – с помощью высокой Т* Воздушный -
- 39. Химический метод стерилизации применяют для изделий, в конструкции которых использованы термолабильные материалы а.Газовым методом стерилизуют ИМН,
- 40. Сроки хранения стерильных изделий определяются видом упаковки: Двухслойная бязь, коробки стерилизационные без фильтра, пергамент, бумага упаковочная
- 41. К упаковочной бумаге для стерилизации ИМН должно быть регистрационное удостоверение, инструкция
- 42. проверка режимов, параметров аппаратуры, применение химических индикаторов и оценка эффективности Эффективность оценивают на основании результатов бактериологических
- 43. Стерилизаторы подлежат бактериологическому контролю после их установки (ремонта), а также в ходе эксплуатации не реже двух
- 44. Производственный контроль ПК проведения дезинфекционных и стерилизационных мероприятий осуществляется на основании Плана производственного контроля ЛПУ, включающего
- 45. ПК включает : Наличие официально изданных СП Наличие документов, подтверждающих безопасность продукции, работ, услуг Назначение лиц,
- 46. Оценка качества Критериями оценки качества проведения дезинфекционных и стерилизационных мероприятий в ЛПО являются: Отрицательные результаты посевов
- 48. Скачать презентацию










































 Експертиза стійкої втрати працездатності
Експертиза стійкої втрати працездатності Дистрофии. Классификация дистрофий
Дистрофии. Классификация дистрофий Қан кету және қан түкіру кезіндегі алғашқы көмек
Қан кету және қан түкіру кезіндегі алғашқы көмек Особенности размещения приемного отделения
Особенности размещения приемного отделения Кардиальная патология при сахарном диабете
Кардиальная патология при сахарном диабете Методы лечения аномалий прикуса в периоде смешанных зубах
Методы лечения аномалий прикуса в периоде смешанных зубах Мультикиназные ингибиторы - 2
Мультикиназные ингибиторы - 2 Средства, влияющие на систему крови
Средства, влияющие на систему крови Комплексные методы лечения зубочелюстных аномалий. Виды хирургических вмешательств в возрастном аспекте
Комплексные методы лечения зубочелюстных аномалий. Виды хирургических вмешательств в возрастном аспекте лфк-при-артрозе
лфк-при-артрозе Онкологія. Організація протиракової боротьби в Україні. Етіологія і патогенез злоякісних пухлин
Онкологія. Організація протиракової боротьби в Україні. Етіологія і патогенез злоякісних пухлин Апластикалық анемиялар
Апластикалық анемиялар Хронический гломерулонефрит
Хронический гломерулонефрит Бет-жақсүйек аймағының жараларын алғашқы хирургиялық өңдеу. Ерекшеліктері. Жүргізу техникасы
Бет-жақсүйек аймағының жараларын алғашқы хирургиялық өңдеу. Ерекшеліктері. Жүргізу техникасы Бронхиалдық астма-инфекциялық аллергиялық ауру
Бронхиалдық астма-инфекциялық аллергиялық ауру Домашний диетолог. 3-фазная программа управления весом. Тест-викторина
Домашний диетолог. 3-фазная программа управления весом. Тест-викторина Коррекция нарушений развития детей: особые образовательные потребности дошкольников с ОВЗ
Коррекция нарушений развития детей: особые образовательные потребности дошкольников с ОВЗ Спортивный травматизм
Спортивный травматизм Гравидограмманың интерпретациясы
Гравидограмманың интерпретациясы Балалардағы тыныс алу жүйесін зерттеу
Балалардағы тыныс алу жүйесін зерттеу Мініінвазивна хірургія в комплексному лікуванні кіст підшлункової залози
Мініінвазивна хірургія в комплексному лікуванні кіст підшлункової залози Комплексная оценка теплового состояния среды
Комплексная оценка теплового состояния среды Процессы адаптации. Регенерация, репарация и заживление ран
Процессы адаптации. Регенерация, репарация и заживление ран Особенности питания детей школьного возраста. 8 класс
Особенности питания детей школьного возраста. 8 класс Порядок оказания скорой, в том числе скорой специализированной, медицинской помощи
Порядок оказания скорой, в том числе скорой специализированной, медицинской помощи Жүрек-қантамыр аурулары. Гипертония .Стенокардия. Инсульт миокард. Инфарктісі
Жүрек-қантамыр аурулары. Гипертония .Стенокардия. Инсульт миокард. Инфарктісі Осложнения сахарного диабета
Осложнения сахарного диабета Основные психопатологические синдромы
Основные психопатологические синдромы