Содержание
- 2. ИСТОРИЯ 1948 г., Е.М. Тареев в монографии "Гипертоническая болезнь" писал: "Представление о гипертонике особенно часто ассоциируется
- 3. ИСТОРИЯ конец 1980-х годов несколько авторов (A.R Christlieb и др., М. Modan и др. в 1985
- 4. ИСТОРИЯ 1993 г, L.M. Resnick вводит понятие “генерализованной сердечно–сосудистой метаболической болезни”, которая проявляется АГ, инсулиннезависимым сахарным
- 5. РАСПРОСТРАНЕННОСТЬ Распространенность МС, по данным разных авторов, составляет от 5–20% (J.Desperes, 1994). В западных странах распространенность
- 6. Виды метаболического синдрома По критериям компонентов МС больные распределяются на группы: с полным МС (сочетание АГ,
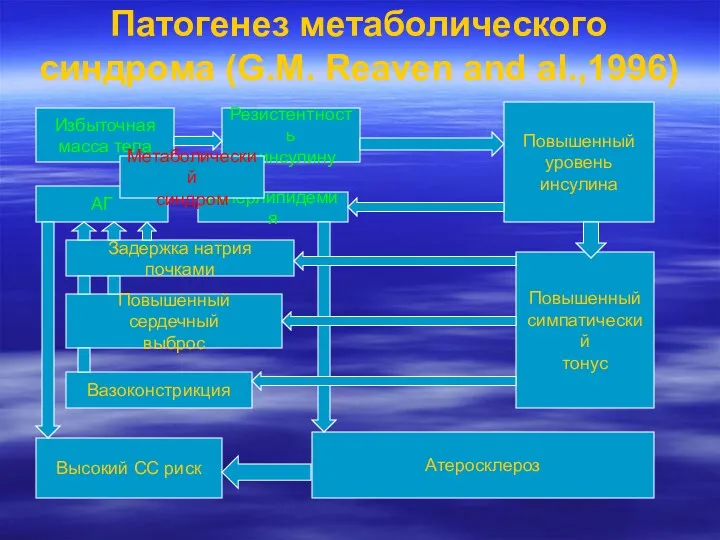
- 8. Патогенез метаболического синдрома (G.M. Reaven and al.,1996) Избыточная масса тела Резистентность к инсулину Повышенный уровень инсулина
- 9. ПАТОГЕНЕЗ ГИ сначала снижает чувствительность, а затем блокирует инсулиновые рецепторы, вследствие чего поступающие с пищей глюкоза
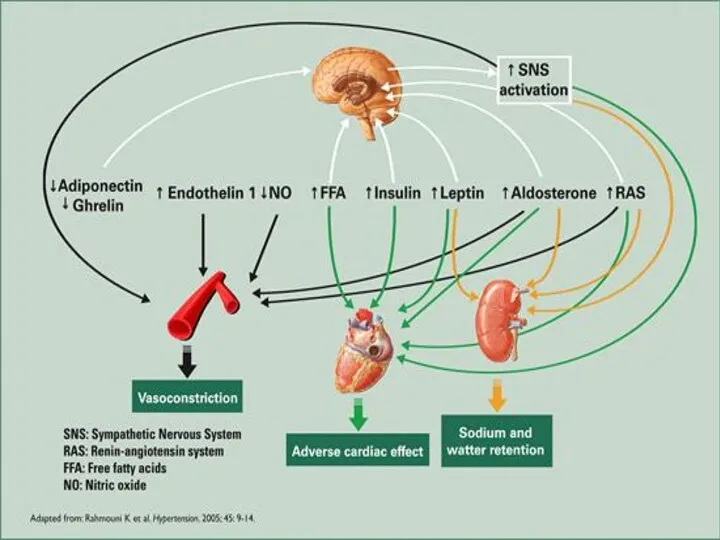
- 10. ПАТОГЕНЕЗ Центральный тип ожирения является причиной развития ИР, ГИ и других метаболических нарушений. Адипоциты висцеральной жировой
- 11. ПАТОГЕНЕЗ Интенсивный липолиз в висцеральных адипоцитах приводит к избыточному поступлению СЖК в портальную систему и печень,
- 12. Сосудистые эффекты инсулина Вазодилятация Истощение вазодилятации Антиатерогенные эффекты в результате увеличения высвобождения NO Снижение жесткости крупных
- 13. ГИПЕРИНСУЛИНЕМИЯ Инсулин повышает реабсорбцию натрия в проксимальных канальцах почек, что приводит к гиперволемии и повышению содержания
- 14. ГИПЕРИНСУЛИНЕМИЯ Инсулин является прямым вазодилатирующим агентом, поэтому ИР сама по себе способствует повышению ОПСС. Инсулининдуцируемая вазодилатация
- 15. ГИПЕРИНСУЛИНЕМИЯ В условиях ГИ происходит блокирование трансмембранных ионообменных механизмов (снижается активность трансмембранного фермента Na+, K+ и
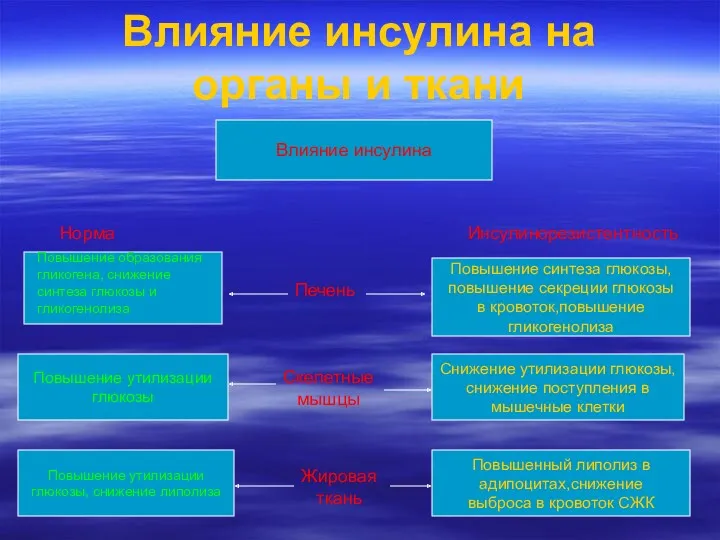
- 16. Влияние инсулина на органы и ткани Влияние инсулина Норма Инсулинорезистентность Повышение утилизации глюкозы Повышение утилизации глюкозы,
- 17. ГИПЕРСИМПАТИКОТОНИЯ Гиперсимпатикотония усиливает секрецию ренина в почках. Повышение ренина активизирует РААС. Увеличение концентрации AT–II воздействует на
- 18. ИНСУЛИНОРЕЗИСТЕНТНОСТЬ Инсулинорезистентность - снижение чувствительности инсулино-зависимых тканей к действию инсулина. Это состояние характеризуется недостаточным биологическим ответом
- 19. ПРИЧИНЫ ИНСУЛИНОРЕЗИСТЕНТНОСТИ гормональные и метаболические факторы, аутоиммунизация с выработкой антител к инсулину и инсулиновым рецепторам, изменение
- 20. ИНСУЛИНОРЕЗИСТЕНТНОСТЬ Выделяют периферическую и печеночную инсулинорезистентность. Причиной возникновения периферической инсулинорезистентности является уменьшение поглощения глюкозы поперечно-полосатыми мышцами
- 21. ИНСУЛИНОРЕЗИСТЕНТНОСТЬ По последним данным, ИР выявляется задолго (минимум за 15 лет) до появления клиники СД: гипергликемия
- 22. ИНСУЛИНОРЕЗИСТЕНТНОСТЬ При ИР подавление инсулином глюкозо–стимулируемой экспрессии гена AT в клетках проксимальных канальцев почек не происходит,
- 23. При синдроме “X” количество инсулина в крови больного ожирением может повышаться до 90–100 мкЕД/мл (при норме
- 24. МЕТОДЫ ОПРЕДЕЛЕНИЯ ИНСУЛИНОРЕЗИСТЕНТНОСТИ "Золотым" стандартом подтверждения наличия инсулинорезистентности является эугликемическая клэмп-методика с использованием биостатора. Суть ее
- 25. МЕТОДЫ ОПРЕДЕЛЕНИЯ ИНСУЛИНОРЕЗИСТЕНТНОСТИ Косвенными показателями инсулинорезистентности можно считать: уровень базальной инсулинемии индекс Саго - отношение глюкозы
- 26. ДИСФУНКЦИЯ ЭНДОТЕЛИЯ Определенный вклад в генез и становление АГ при МС вносит дисфункция эндотелия сосудов. Эндотелий
- 28. ЛЕПТИН В 1953 г. G.C. Kennedy предположил, что жировая ткань в организме, кроме роли энергетического депо,
- 29. ЛЕПТИН Лептин – гормон, синтезируемый адипоцитами висцеральной жировой ткани. Концентрация лептина в плазме прямо пропорциональна степени
- 30. ЛЕПТИН повышение АД на фоне роста массы тела более тесно коррелировало с повышением концентрации норадреналина, чем
- 31. ГЕМОРЕОЛОГИЯ Нарушение гемореологических свойств крови в сочетании с гиперлипидемией способствует тромбообразованию и нарушению в системе микроциркуляции.
- 32. ГЕМОРЕОЛОГИЯ ГИ приводит к нарушению фибринолитической активности крови, способствует отложению жировой ткани и обусловливает повышенный синтез
- 33. ГЕМОРЕОЛОГИЯ Изменения со стороны функциональной активности тромбоцитов крови у больных МС заключается прежде всего в повышении
- 34. ДИСЛИПИДЕМИЯ Высокий уровень триглицеридов. Увеличением содержания СЖК в крови, которые, в избытке поступая в печень, приводят
- 35. ДИСЛИПИДЕМИЯ Хроническая ГИ в ответ на систематически избыточное питание приводит к переполнению триглицеридами жировой ткани и
- 36. ГИПЕРУРИКЕМИЯ Гиперурикемия (ГУ) довольно часто ассоциирована с НТГ, дислипидемией и АГ у больных абдоминальным ожирением и
- 37. Схема обследования больных на стадии доклинических проявлений выявление наследственной предрасположенности к ожирению, СД, ИБС, АГ; социальный
- 39. Скачать презентацию
































 Профилактическая медицина
Профилактическая медицина Боль и обезболивание
Боль и обезболивание Егде жастағы және қарт адамдардың тамақтануы
Егде жастағы және қарт адамдардың тамақтануы Улучшение качества медицинской помощи на основе информационных технологий
Улучшение качества медицинской помощи на основе информационных технологий Жапонияның денсаулық сақтау жүйесі
Жапонияның денсаулық сақтау жүйесі Налоги и налогообложение в здравоохранении
Налоги и налогообложение в здравоохранении Гнойно-воспалительные заболевания мягких тканей у детей
Гнойно-воспалительные заболевания мягких тканей у детей Кариес зубов. Причины и механизм образования. Основные теории и гипотезы кариеса (Миллер, Лукомский, Энтин, Шарпенак, Боровский)
Кариес зубов. Причины и механизм образования. Основные теории и гипотезы кариеса (Миллер, Лукомский, Энтин, Шарпенак, Боровский) Дифференциальная диагностика при легочных инфильтратах. Принципы лечения
Дифференциальная диагностика при легочных инфильтратах. Принципы лечения Коронавирус 2019-nCoV
Коронавирус 2019-nCoV Металло керамикалық сауыт дайындаудың бірінші лабораториялық кезеңінде қолданылатын құрал саймандар мен апараттар
Металло керамикалық сауыт дайындаудың бірінші лабораториялық кезеңінде қолданылатын құрал саймандар мен апараттар Доброкачественные органоспецифические опухоли челюстей, лица, шеи
Доброкачественные органоспецифические опухоли челюстей, лица, шеи Fizika kafedrasi
Fizika kafedrasi Невроз. Психотравма высшей нервной деятельности с конфликтом в ценостеях, ориентации, отношениях
Невроз. Психотравма высшей нервной деятельности с конфликтом в ценостеях, ориентации, отношениях Қазіргі кездегі өнеркәсіптік қала тұрғындарының денсаулығы
Қазіргі кездегі өнеркәсіптік қала тұрғындарының денсаулығы Ішек өтімсіздігі (инвагинация)
Ішек өтімсіздігі (инвагинация) СПИД – что это такое?
СПИД – что это такое? Течение и ведение послеродового периода. Становление лактации. Послеродовая контрацепция
Течение и ведение послеродового периода. Становление лактации. Послеродовая контрацепция Oral cavity
Oral cavity Malignant Melanoma
Malignant Melanoma Вещества, влияющие на эфферентную иннервацию. Адренергические средства
Вещества, влияющие на эфферентную иннервацию. Адренергические средства Основы здорового образа жизни студентов
Основы здорового образа жизни студентов Болезни желчного пузыря и желчевыводящих путей. Желчно-каменная болезнь. Хронический панкреатит
Болезни желчного пузыря и желчевыводящих путей. Желчно-каменная болезнь. Хронический панкреатит Неоадъювантное лечение II-III стадии HER2-положительного рака молочной железы
Неоадъювантное лечение II-III стадии HER2-положительного рака молочной железы Туберкулинодиагностика
Туберкулинодиагностика Тромболитики. Механизм действия
Тромболитики. Механизм действия Стахиботриотоксикоз
Стахиботриотоксикоз Защита медицинского персонала от ВБИ
Защита медицинского персонала от ВБИ