Молекулярно-генетические методы, фармокогенетика, генетический паспорт, Основные предикторы генетической предрасположенности презентация
Содержание
- 2. Что же такое предиктивная медицина? Это одно из направлений современной медицины, которое направлено на прогнозирование заболеваний
- 3. Генетический анализ Молекулярно-генетический анализ - это современный, точный и единственный на сегодняшний день метод, позволяющий выявить
- 4. Кому целесообразно проводить генетический анализ? здоровым людям, ведущим интенсивный образ жизни и желающим защитить свой организм
- 5. здоровым людям, которые хотят оставаться здоровыми и дееспособными до самых преклонных лет, и не тратить своё
- 6. будущим мамам и папам, планирующим рождение ребенка и стремящимся оптимальным образом подготовить свой организм к зачатию
- 7. людям с отягощенной наследственностью по сердечно-сосудистым, эндокринным, онкологическим, и другим заболеваниям, желающим заблаговременно принять меры по
- 8. Когда надо проводить молекулярно-генетический анализ? Генетическое исследование – это возможность прогнозирования заболеваний и чем раньше его
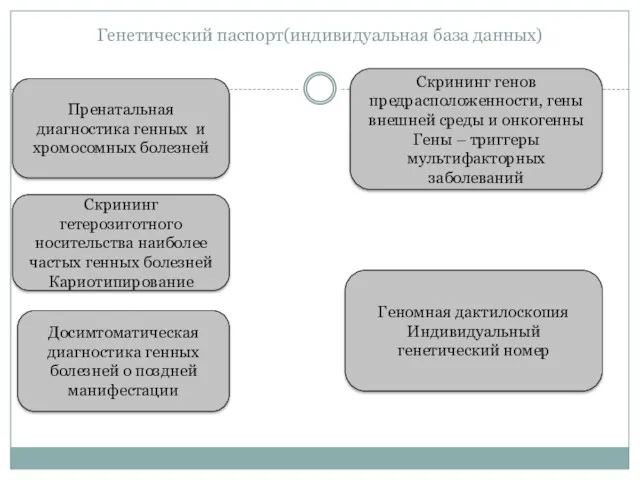
- 9. Генетический паспорт – документ, содержащий информацию о генетическом коде человека. Эта информация может быть получена в
- 10. Для составления генетического паспорта исследуется кровь – процедура получения образцов для исследования не сложнее, чем для
- 11. Использовать полученную информацию можно по-разному, поэтому существует две разновидности генетических паспортов. ДНК-профиль, или идентификационный генетический паспорт,
- 12. Скрининг гетерозиготного носительства наиболее частых генных болезней Кариотипирование Досимтоматическая диагностика генных болезней о поздней манифестации Пренатальная
- 14. ДНК-профиль ДНК-профиль, или идентификационный генетический паспорт – это аналог отпечатков пальцев человека. В ДНК-профиле заключена информация
- 15. Генетический паспорт здоровья дает всю необходимую информацию о наиболее вероятных заболевания конкретного человека, и врач сможет
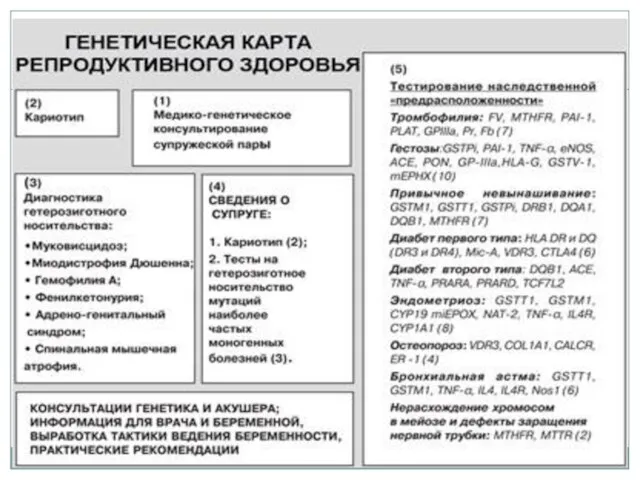
- 16. Неинвазивная пренатальная диагностика резус фактора плода молекулярно-генетическим методом Для чего нужен анализ? Одним из основных направлений
- 17. Несовместимость по резус-фактору- одна из самых частых причин ГБПиН. Когда отец гетерозиготен по гену RHD, а
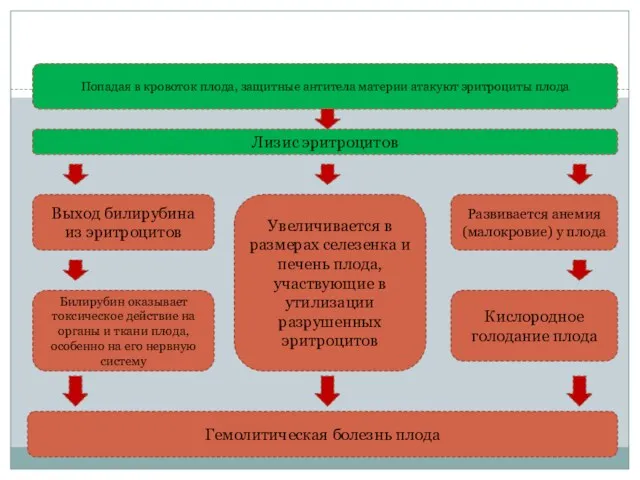
- 18. Попадая в кровоток плода, защитные антитела материи атакуют эритроциты плода Лизис эритроцитов Выход билирубина из эритроцитов
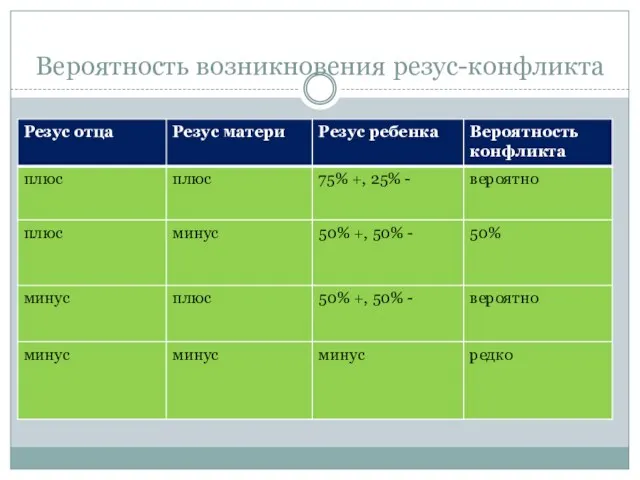
- 19. Вероятность возникновения резус-конфликта
- 20. О методе Анализируется венозная кровь беременной женщины, содержащая небольшие количества внеклеточной ДНК плода. Циркулирующие внеклеточные плодные
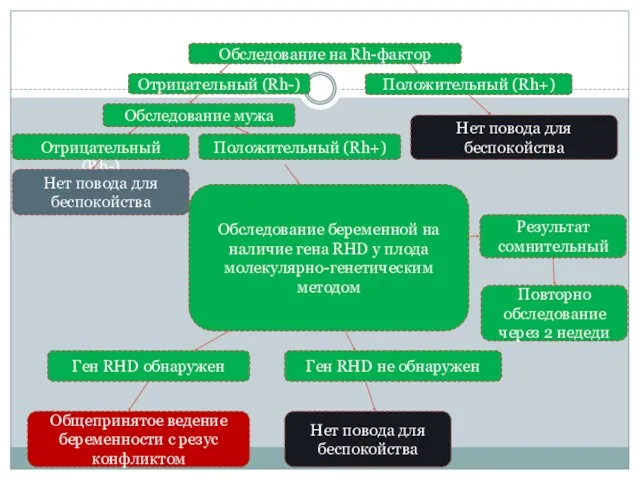
- 21. Обследование на Rh-фактор Отрицательный (Rh-) Положительный (Rh+) Обследование мужа Отрицательный (Rh-) Положительный (Rh+) Нет повода для
- 22. Материал венозная кровь матери (с ЭДТА) сроки 3-5 рабочих дней
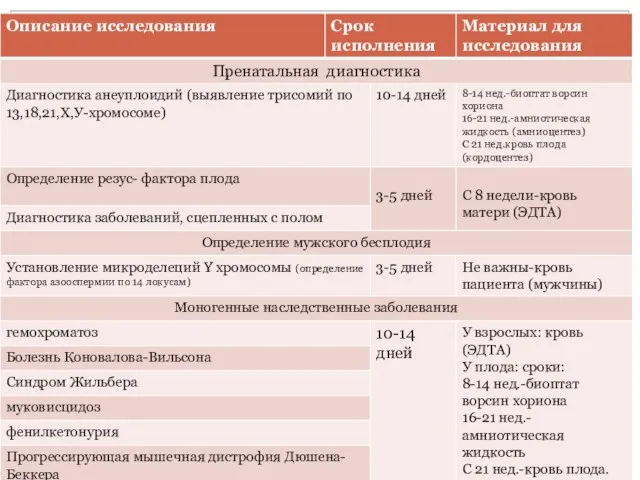
- 23. Пренатальная диагностика анеуплоидий (выявление трисомии по 13,18,21, Х,У-хромосоме У человека в норме 46 хромосом или 23
- 24. Для чего нужен анализ? Анеуплойдии-это изменение числа хромосом, которые могут привести к возникновению хромосомных заболеваний (синдром
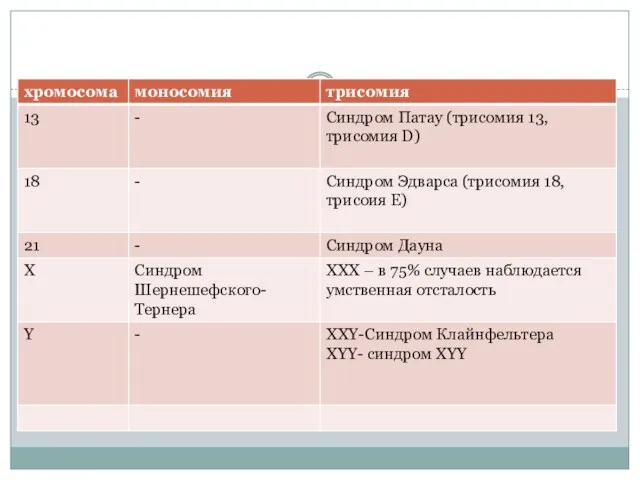
- 26. Пренатальная диагностика анеуплоидий (выявление трисомии по 13,18,21, Х,У-хромосоме) 13- Cиндром Патау (трисомия 13, трисомия D) 18-
- 27. Материал для исследования в качестве плодного материала для проведения пренатальной диагностики анеуплоидий используют либо биоптат ворсин
- 28. Данный анализ рекомендуется при следующих показателях. -возраст матери от 30 лет -семейным парам, имеющим детей с
- 29. Все мы похожи, но благодаря разнообразию хромосомного набора каждый из нас уникален. Малейшие изменения в хромосомах
- 30. Золотой стандарт ДНК-диагностики на сегодняшний день - комплексное использование и прямых и косвенных методов в каждом
- 31. Прямые методы ДНК-диагностики используются в тех случаях, когда известен ген, ответственный за возникновение наследственного заболевания и
- 32. Косвенные методы ДНК-диагностики применяют в том случае, если ген, повреждение в котором приводит к заболеванию, не
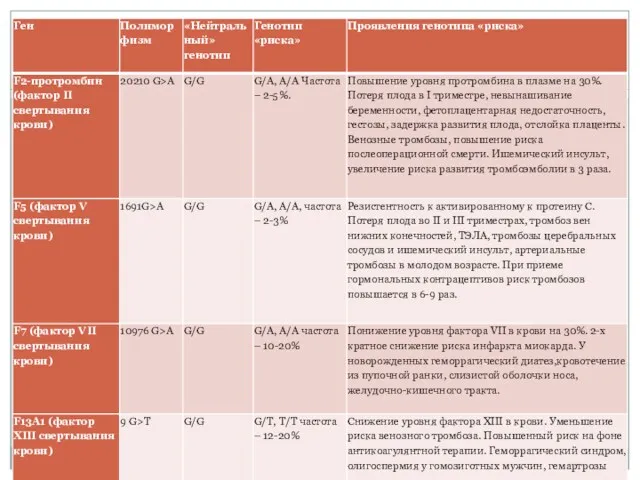
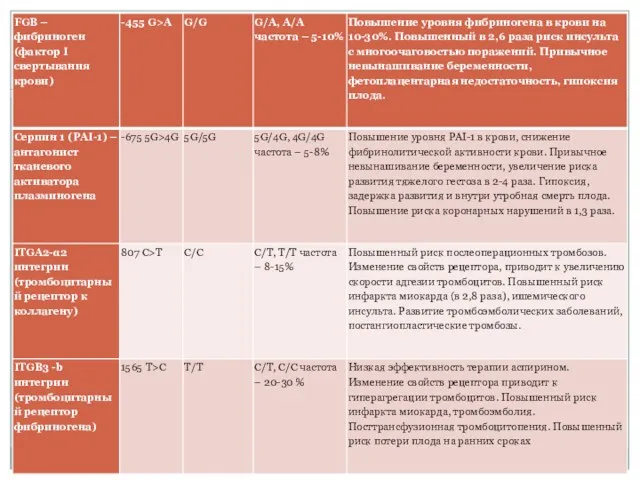
- 33. Тромбофилия – заболевание системы крови, проявляющееся в нарушении гемостаза и склонности к развитию рецидивирующих сосудистых тромбозов
- 34. Дополнительные факторы риска развития тромбофилических состояний: Приобретенные заболевания крови (тромбоцитозы, этитремия, антифосфолипидный синдром) Атеросклероз Мерцательная аритмия
- 35. Показания к генетическому анализу: Случаи наследственной тромбоэмболии в семье Случаи тромбоза в анамнезе единичный тромбоз до
- 38. Для верификации диагноза и разработки тактики лечения необходимы дополнительные исследования: АЧТВ Протромбиновое время в секундах Фибриноген
- 39. Крупнейшим достижением науки, ознаменовавшим переход в III тысячелетие, явилась расшифровка генома человека. Это открытие определяет новый
- 40. Научная, медицинская и экономическая целесообразность фармакогенетических разработок сегодня не вызывает сомнений, поскольку их итогом является повышение
- 41. Фармакогеномика — новая наука о том, как генетика влияет на индивидуальную реакцию на конкретное лекарство. Она
- 42. Новейшим направлением фармакогенетики является изыскание оригинальных фармакологических средств, направленных на определенные фенотипы патологических состояний и чувствительность
- 43. В настоящее время у врачей имеется ложное предубеждение о фармакогенетическом тестировании как об очень сложном, дорогом
- 44. Кроме того, в настоящее время активно разрабатываются так называемые ДНК-чипы, с помощью которых у одного больного
- 48. Скачать презентацию



































 Алғашқы көмек түрлері
Алғашқы көмек түрлері Ошибки диагностики и лечения внебольничных пневмоний
Ошибки диагностики и лечения внебольничных пневмоний Переход к системе непрерывного медицинского (фармацевтического) образования
Переход к системе непрерывного медицинского (фармацевтического) образования Первая медицинская помощь при острой сердечной недостаточности и инсульте
Первая медицинская помощь при острой сердечной недостаточности и инсульте Острый и хронический пиелонефрит
Острый и хронический пиелонефрит Мал шаруашылығы өнiмдерiн консервiлеу технологиясының негiздерi мен гигиенасы және оларды ветеринариялық-санитариялық сараптау
Мал шаруашылығы өнiмдерiн консервiлеу технологиясының негiздерi мен гигиенасы және оларды ветеринариялық-санитариялық сараптау Общие принципы проведения инфузионной терапиии при критических состояних. Общие принципы диагностики и ИТ эндо- и экзотоксикозов
Общие принципы проведения инфузионной терапиии при критических состояних. Общие принципы диагностики и ИТ эндо- и экзотоксикозов КОГБУЗ Яранская центральная районная больница
КОГБУЗ Яранская центральная районная больница Обезболивание на догоспитальном этапе оказания медицинской помощи
Обезболивание на догоспитальном этапе оказания медицинской помощи Принципы гигиенического нормирования вредных веществ
Принципы гигиенического нормирования вредных веществ Острая сердечная недостаточность
Острая сердечная недостаточность Лекция Медицинское обеспечение ликвидации ЧС
Лекция Медицинское обеспечение ликвидации ЧС Перинатальные инфекции новорожденных
Перинатальные инфекции новорожденных Служение больницы и учреждения
Служение больницы и учреждения Шоки-1. Патогенез шоку
Шоки-1. Патогенез шоку Қызықты клиникалық жағдай
Қызықты клиникалық жағдай Заболевания почек у детей
Заболевания почек у детей Основы трансплантологии
Основы трансплантологии Лазеры в медицине
Лазеры в медицине Отруйність спиртів та їх згубна дія на організм людини
Отруйність спиртів та їх згубна дія на організм людини Энтеробиоз. Трихинеллез
Энтеробиоз. Трихинеллез Сестринский уход при различных заболеваниях и состояниях. Лечение пациентов терапевтического профиля
Сестринский уход при различных заболеваниях и состояниях. Лечение пациентов терапевтического профиля Патофизиологический эксперимент
Патофизиологический эксперимент Рак поджелудочной железы
Рак поджелудочной железы Ситуационные задачи для проведения занятий с ординаторами. Подготовка и организация работы больницы при чрезвычайных ситуациях
Ситуационные задачи для проведения занятий с ординаторами. Подготовка и организация работы больницы при чрезвычайных ситуациях ABCDE / Einführung. Cardio-pulmonale Reanimation
ABCDE / Einführung. Cardio-pulmonale Reanimation Оказание первой помощи при несчастных случаях на производстве
Оказание первой помощи при несчастных случаях на производстве Синдром легочного инфильтрата
Синдром легочного инфильтрата