Слайд 17

PLoS One. 2013 Sep 17;8(9):e75171. doi: 10.1371/journal.pone.0075171.
Epidemiology and Outcome of Pneumonia
Caused by Methicillin-Resistant Staphylococcus aureus (MRSA) in Canadian Hospitals.
Tadros MTadros M, Williams VTadros M, Williams V, Coleman BLTadros M, Williams V, Coleman BL, McGeer AJTadros M, Williams V, Coleman BL, McGeer AJ, Haider STadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee CTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides HTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein ETadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John MTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston LTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil STadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz KTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin NTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin N, Suh KNTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin N, Suh KN, Powis JTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin N, Suh KN, Powis J, Smith STadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin N, Suh KN, Powis J, Smith S, Taylor GTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin N, Suh KN, Powis J, Smith S, Taylor G, Watt CTadros M, Williams V, Coleman BL, McGeer AJ, Haider S, Lee C, Iacovides H, Rubinstein E, John M, Johnston L, McNeil S, Katz K, Laffin N, Suh KN, Powis J, Smith S, Taylor G, Watt C, Simor AE.
Source
University of Toronto, Toronto, Ontario, Canada.
Abstract
BACKGROUND:
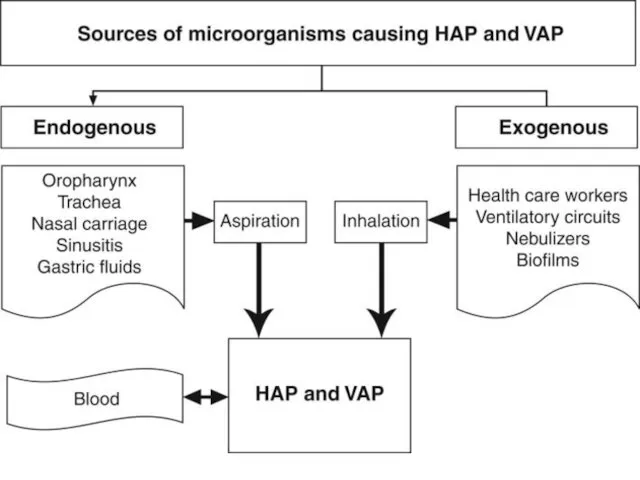
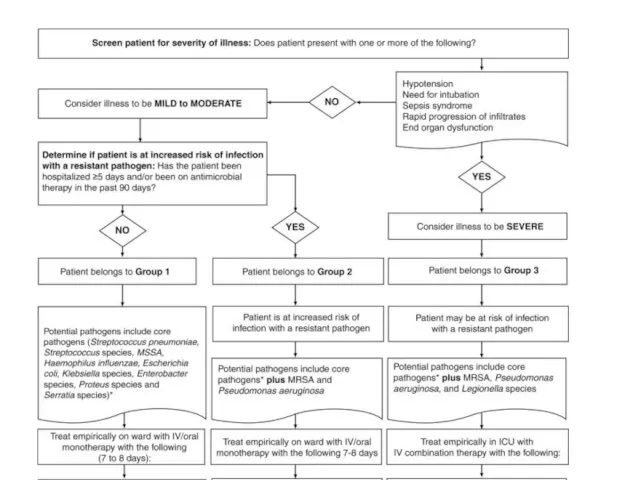
MRSA remains a leading cause of hospital-acquired (HAP) and healthcare-associated pneumonia (HCAP). We describe the epidemiology and outcome of MRSA pneumonia in Canadian hospitals, and identify factors contributing to mortality.
METHODS:
Prospective surveillance for MRSA pneumonia in adults was done for one year (2011) in 11 Canadian hospitals. Standard criteria for MRSA HAP, HCAP, ventilator-associated pneumonia (VAP), and community-acquired pneumonia (CAP) were used to identify cases. MRSA isolates underwent antimicrobial susceptibility testing, and were characterized by pulsed-field gel electrophoresis (PFGE) and Panton-Valentine leukocidin (PVL) gene detection. The primary outcome was all-cause mortality at 30 days. A multivariable analysis was done to examine the association between various host and microbial factors and mortality.
RESULTS:
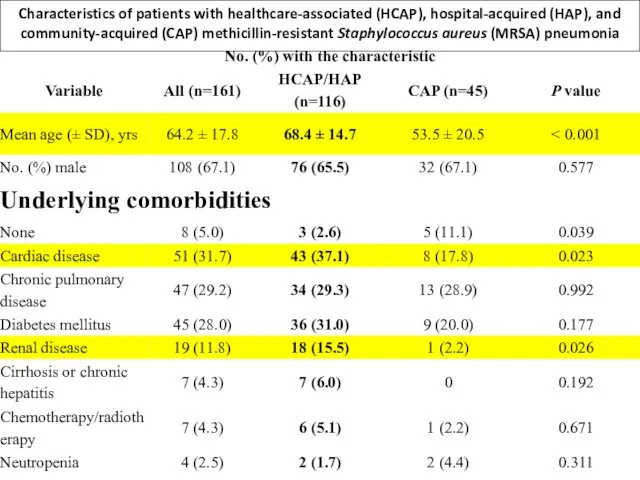
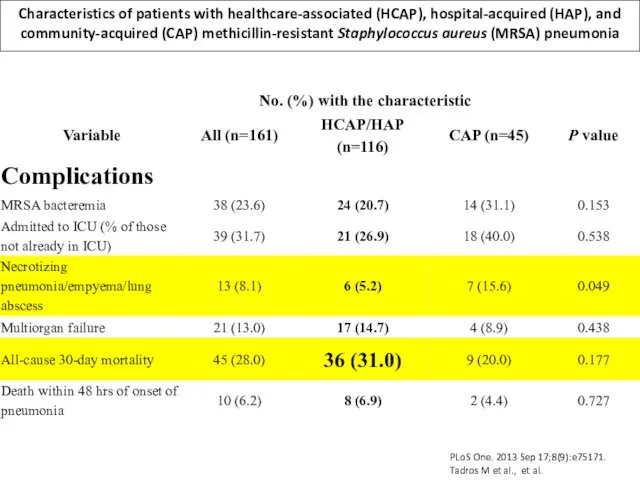
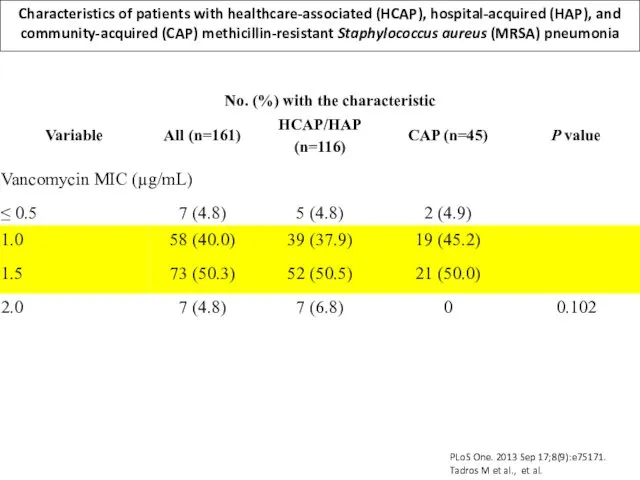
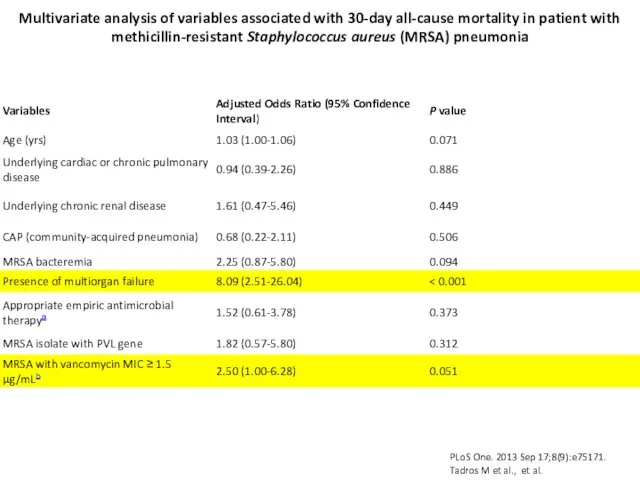
A total of 161 patients with MRSA pneumonia were identified: 90 (56%) with HAP, 26 (16%) HCAP, and 45 (28%) CAP; 23 (14%) patients had VAP. The mean (± SD) incidence of MRSA HAP was 0.32 (± 0.26) per 10,000 patient-days, and of MRSA VAP was 0.30 (± 0.5) per 1,000 ventilator-days. The 30-day all-cause mortality was 28.0%. In multivariable analysis, variables associated with mortality were the presence of multiorgan failure (OR 8.1; 95% CI 2.5-26.0), and infection with an isolate with reduced susceptibility to vancomycin (OR 2.5, 95% CI 1.0-6.3).
CONCLUSIONS:
MRSA pneumonia is associated with significant mortality. Severity of disease at presentation, and infection caused by an isolate with elevated MIC to vancomcyin are associated with increased mortality. Additional studies are required to better understand the impact of host and microbial variables on outcome.
















![Род Stenotrophomonas включает 5 видов [25], из которых клинически значимым](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/104775/slide-29.jpg)















 Инфекционный мононуклеоз
Инфекционный мононуклеоз Методы исследования сердечно-сосудистой системы
Методы исследования сердечно-сосудистой системы Проведение операции тонзилэктомии при применении холодноплазменного хирургического метода
Проведение операции тонзилэктомии при применении холодноплазменного хирургического метода Снотворные средства. Психотропные средства
Снотворные средства. Психотропные средства Фармакологічні засоби відновлення працездатності
Фармакологічні засоби відновлення працездатності Антитела: строение, функции
Антитела: строение, функции ВИЧ инфекция. Клиника, лечение, профилактика
ВИЧ инфекция. Клиника, лечение, профилактика Инфекционный контроль и профилактика ВБИ
Инфекционный контроль и профилактика ВБИ Методы вправления вывихов
Методы вправления вывихов Введение в акушерство
Введение в акушерство Қазақстан Қарулы Күштерінің медицина қызметінің міндеттері мен ұйымдастырылуы
Қазақстан Қарулы Күштерінің медицина қызметінің міндеттері мен ұйымдастырылуы Проведение процедуры ЭКО и перенос криоконсервированных эмбрионов
Проведение процедуры ЭКО и перенос криоконсервированных эмбрионов Нейролептические экстрапирамидные расстройства
Нейролептические экстрапирамидные расстройства Безопасность регионарной анестезии с точки зрения доказательной медицины
Безопасность регионарной анестезии с точки зрения доказательной медицины Жүре пайда болған (ЖИТС, СПИД ағылш. AIDS) иммундық дефицитiнiң синдромы
Жүре пайда болған (ЖИТС, СПИД ағылш. AIDS) иммундық дефицитiнiң синдромы Причины кардиогенного шока
Причины кардиогенного шока Пациент. Подпись врача
Пациент. Подпись врача Ажгереева А
Ажгереева А Строения генетического аппарата митохондрий. Особенности митохондриальной наследственности
Строения генетического аппарата митохондрий. Особенности митохондриальной наследственности Использование 3D печати в медицине
Использование 3D печати в медицине Профилактика и коррекция нарушений осанки
Профилактика и коррекция нарушений осанки Острые лейкозы
Острые лейкозы Розвиток урології як клінічної дисципліни. Неспецифічні запальні захворювання органів сечової системи
Розвиток урології як клінічної дисципліни. Неспецифічні запальні захворювання органів сечової системи Клинические разновидности аномалий зубов и зубных рядов. (Часть 1)
Клинические разновидности аномалий зубов и зубных рядов. (Часть 1) Биологиялық текті айғақты заттарға сот медициналық сараптама талдау
Биологиялық текті айғақты заттарға сот медициналық сараптама талдау Инвазия. Формы инвазии
Инвазия. Формы инвазии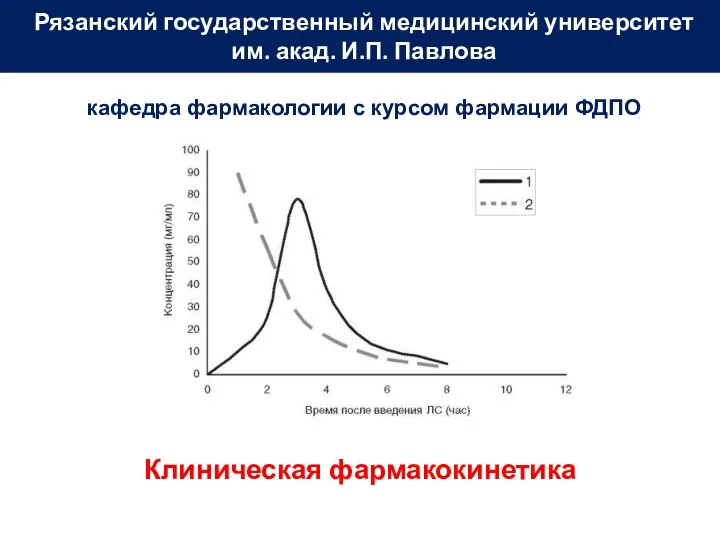 Клиническая фармакокинетика
Клиническая фармакокинетика Синдром (болезнь) Бернара-Сулье
Синдром (болезнь) Бернара-Сулье