Организация работы с непригодными для медицинского использования лекарственными средствами презентация
Содержание
- 2. Министерство здравоохранения Республики Беларусь, управление фармацевтической инспекции и организации лекарственного обеспечения, УО «Витебский государственный медицинский университет»
- 3. Содержание: Подготовительный этап Цель Область применения Используемые сокращения Нормативные ссылки Порядок работы Ответственность Связь с другими
- 4. Цель: Минимизация рисков попадания в гражданский оборот недоброкачественных, фальсифицированных, контрафактных товаров аптечного ассортимента. 4
- 5. Обоснование: В действующих нормативных правовых актах отсутствует понятие «непригодные для медицинского использования лекарственные средства», однако приведены
- 6. К непригодным для медицинского использования лекарственным средствам ОТНОСЯТСЯ: Фальсифицированные ЛС Недоброкачественные ЛС Контрафактные ЛС ЛС с
- 7. Область применения: Организация работы с непригодными для медицинского использования лекарственными средствами с момента поступления в аптечную
- 8. Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 № 323-ФЗ; Федеральный закон
- 9. Федеральный закон от 31 декабря 2014 г. №532-ФЗ «О внесении изменений в отдельные законодательные акты Российской
- 10. Приемка товаров и проведение приемочного контроля; Хранение лекарственных средств для медицинского применения; Связь с другими стандартными
- 11. Используемые сокращения: ★АО – аптечная организация; ★ЛП - лекарственный препарат (ы); ★МОЛ - материально-ответственное лицо; ★НПА
- 12. Квалификация исполнителей: наличие документа, подтверждающее высшее или среднее фармацевтическое образование; сертификат специалиста/свидетельство об аккредитации; уверенное пользование
- 13. Ответственность: Персонал аптечной организации несет ответственность в пределах своей компетенции: ?доведение до сведения работников СОП; ?назначение
- 14. Уполномоченный по качеству аптечной организации: ?контроль соблюдения СОП (не реже 1 раза в месяц; создание журнала
- 15. ?обеспечение передачи отчетов по результатам проведенной работы в ТО Росздравнадзора (форма свободная); ?организация и контроль учета
- 16. ?личное выполнение требований СОП; ?соблюдение персоналом аптечной организации СОП; ?назначение ответственного за организацию работы с непригодными
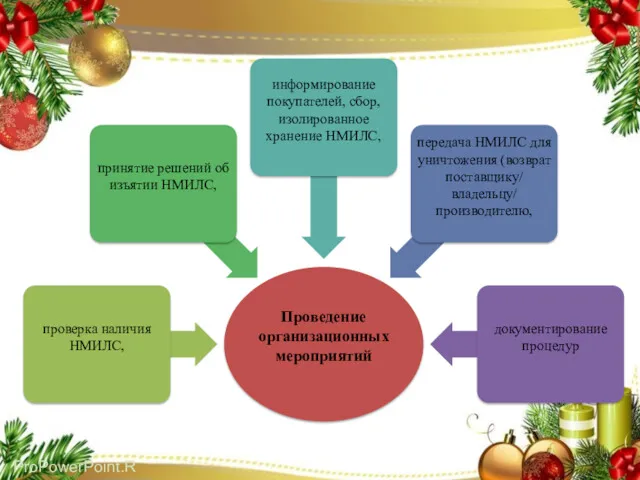
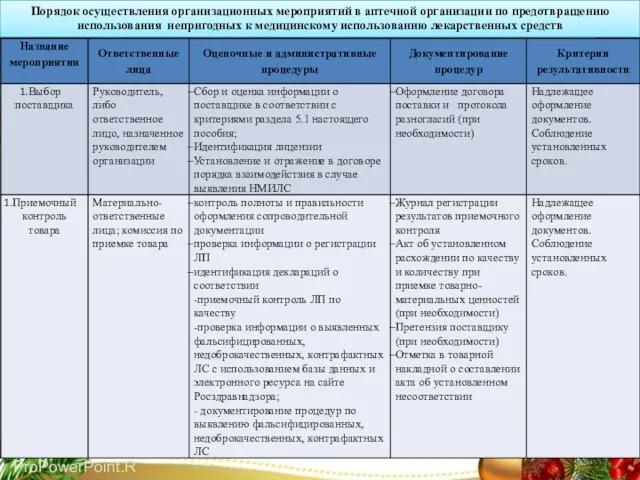
- 17. ПОРЯДОК ОСУЩЕСТВЛЕНИЯ ОРГАНИЗАЦИОННЫХ МЕРОПРИЯТИЙ В АПТЕЧНОЙ ОРГАНИЗАЦИИ ПО ПРЕДОТВРАЩЕНИЮ ИСПОЛЬЗОВАНИЯ НЕПРИГОДНЫХ ДЛЯ МЕДИЦИНСКОГО ИСПОЛЬЗОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
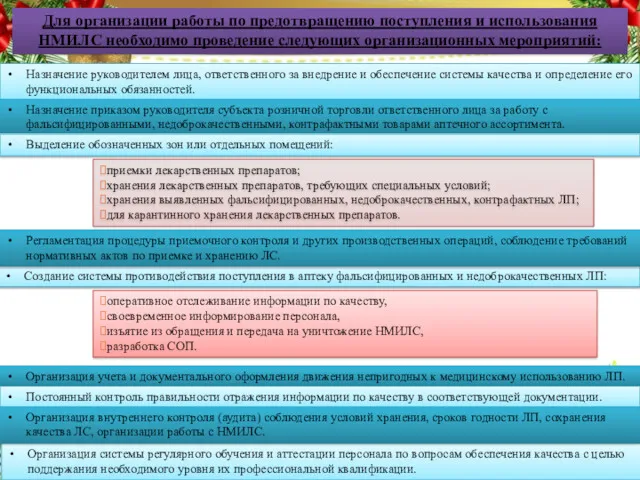
- 18. Создание системы противодействия поступления в аптеку фальсифицированных и недоброкачественных ЛП: Для организации работы по предотвращению поступления
- 19. В процессе регулирования предупреждения и выявления в аптеке НМИЛС можно выделить несколько этапов:
- 20. а) соответствие поставщика требованиям действующего законодательства Российской Федерации о лицензировании отдельных видов деятельности; б) деловая репутация
- 21. Мероприятия на стадии выбора поставщика ✔Идентификация лицензии поставщика на фармацевтическую деятельность (на официальном сайте http://www.roszdravnadzor.ru/services/licenses); ✔При
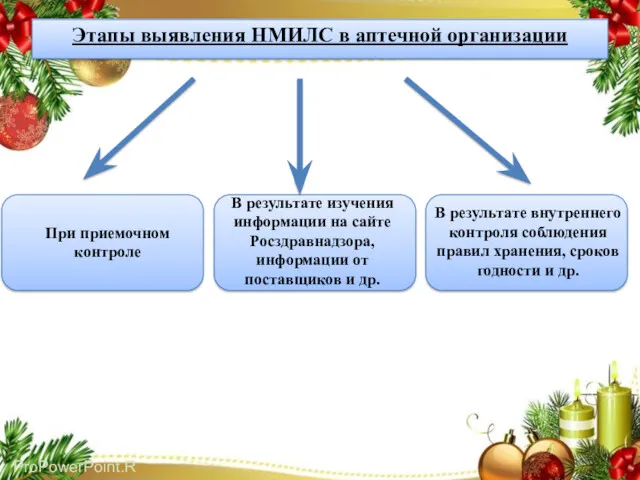
- 22. Этапы выявления НМИЛС в аптечной организации При приемочном контроле В результате изучения информации на сайте Росздравнадзора,
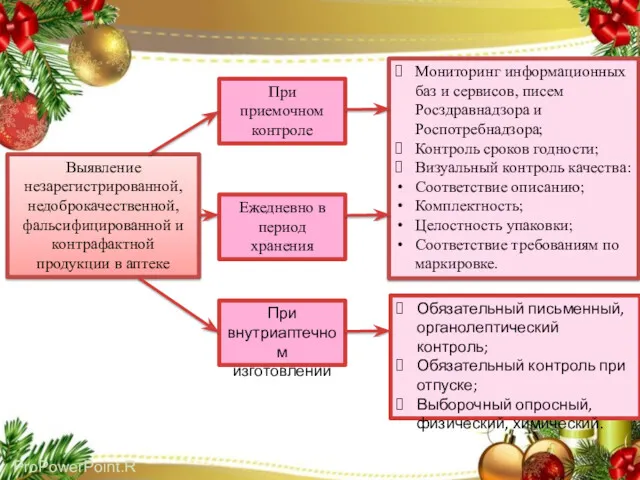
- 23. Выявление незарегистрированной, недоброкачественной, фальсифицированной и контрафактной продукции в аптеке При приемочном контроле Ежедневно в период хранения
- 24. Мероприятия по предотвращению поступления в аптечную организацию фальсифицированных, недоброкачественных, контрафактных ЛП при приемке товаров ?Контроль документации:
- 26. В помещениях и (или) зонах должны поддерживаться температурные режимы хранения и влажность, соответствующие условиям хранения, указанным
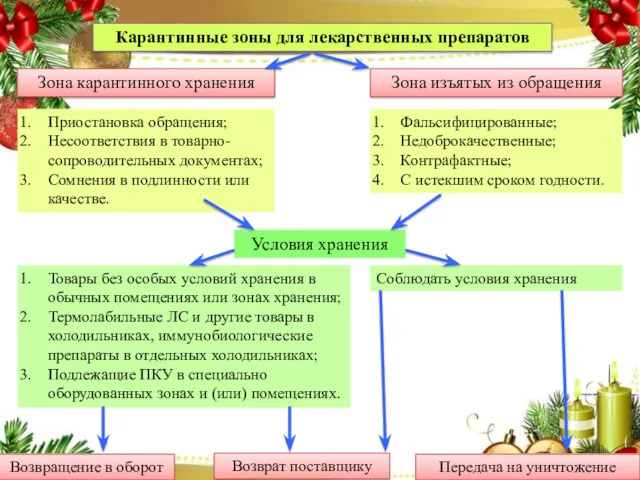
- 27. Карантинные зоны для лекарственных препаратов Зона карантинного хранения Зона изъятых из обращения Приостановка обращения; Несоответствия в
- 28. Перемещение ЛП Из карантинной зоны препарат может быть перемещен: в зону хранения фальсифицированных, недоброкачественных, контрафактных, с
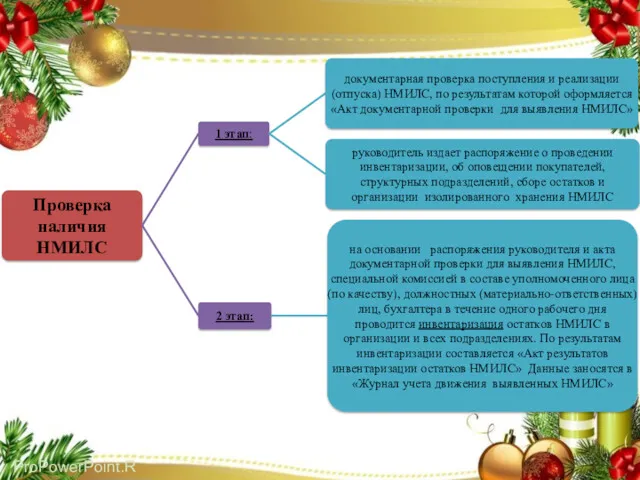
- 30. Анализ информации о выявленных НМИЛС руководителем организации из числа сотрудников организации назначается уполномоченное лицо, в обязанности
- 32. Сбор, изолированное хранение НМИЛС На основании распоряжения руководителя должностным лицом организации незамедлительно осуществляется оповещение покупателей, структурных
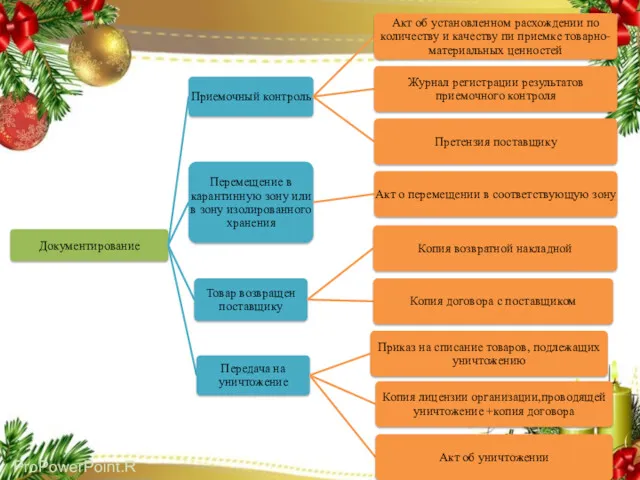
- 33. Передача НМИЛС для уничтожения (возврат поставщику/ владельцу/производителю Размещенные в помещении (зоне) изолированного хранения НМИЛС упаковываются, маркируются
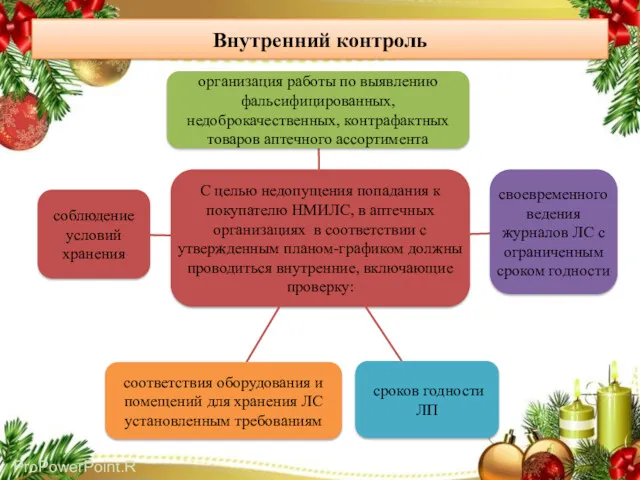
- 34. Выявление иных НМИЛС в результате внутреннего контроля Для выявления ЛС с истекшим сроком годности, а также
- 35. Документирование выявленных несоответствий при приемке товаров В случае несоответствия товаров аптечного ассортимента условиям договора, данным сопроводительных
- 36. При выявлении фактов наличия НМИЛС (в т.ч. с истекшим сроком годности), приостанавливается их реализация, проводится инвентаризация
- 37. Целесообразно информационные письма распечатывать и хранить в отдельной папке. Информационно-аналитический мониторинг и скрининг качества ЛП с
- 38. Внутренний контроль
- 40. 1. Ответственный уполномоченный по качеству в аптечной организации ежедневно в начале рабочего дня просматривает письма для
- 41. 2. При наличии лекарственного препарата обозначенного в письме как фальсифицированное лекарственное средство уполномоченный по качеству сравнивает
- 42. 3.При наличии лекарственного препарата, указанного в письме как фальсифицированное лекарственное средство, но с другими сериями, которые
- 43. 4. Лекарственные препараты, указанные в п.1,2, и 3 cдаются в аккредитованную организацию для проведения мероприятий по
- 44. 5. При наличии лекарственного препарата обозначенного в письме недоброкачественные лекарственные препараты уполномоченный по качеству сравнивает его
- 45. 6. При наличии лекарственного препарата обозначенного в письме недоброкачественные лекарственные препараты, вся серия которого подлежит изъятию
- 46. 7. При наличии лекарственного препарата обозначенного в письме недоброкачественные лекарственные препараты, партия которого подлежит изъятию из
- 47. 4. Лекарственные препараты, указанные в п.5,6, и 7 при подтверждении Росздравнадзором несоответствия качества лекарственных препаратов требованиям
- 48. Порядок работы по выявлению недоброкачественных лекарственных средств, не обозначенных письмами Росздравнадзора: 1. При выявлении лекарственных препаратов,
- 49. 2. Лекарственные препараты, вызывающие сомнение в их качестве, перемещают в зону карантинного хранения (статус которых не
- 50. 3. При отсутствии полного комплекта сопроводительных документов лекарственные препараты перемещаем в зону карантинного хранения лекарственных препаратов
- 51. 28 Порядок работы по выявлению лекарственных средств с истекающим сроком годности: 1. Уполномоченные по качеству и
- 52. 3. При наличии нескольких серий одного наименования лекарственного препарата в первую очередь используется лекарственный препарат, срок
- 53. Документальное оформление: 1. Комиссией в течение двух рабочих дней составляется «Акт о перемещении фальсифицированных, забракованных и
- 54. 2.При отзыве лекарственного препарата и возврата поставщику оформляют возвратную накладную в трех экземплярах: -первый экземпляр с
- 55. 3.При уничтожении лекарственных препаратов и возврата поставщику оформляют возвратную накладную в трех экземплярах: -первый экземпляр с
- 56. Порядок осуществления организационных мероприятий в аптечной организации по предотвращению использования непригодных к медицинскому использованию лекарственных средств
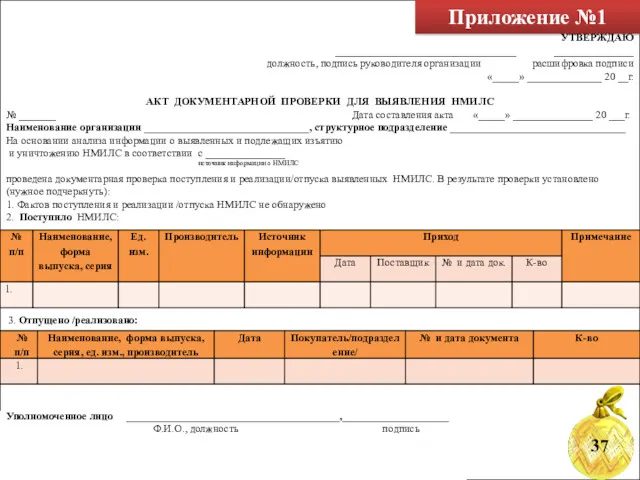
- 60. Приложение №1 УТВЕРЖДАЮ __________________________________ _______________ должность, подпись руководителя организации расшифровка подписи «_____» ______________ 20 __г. АКТ
- 61. УТВЕРЖДАЮ __________________________________ _______________ должность, подпись руководителя организации расшифровка подписи «_____» ______________ 20 __г. АКТ РЕЗУЛЬТАТОВ ИНВЕНТАРИЗАЦИИ
- 62. УТВЕРЖДАЮ __________________________________ _______________ должность, подпись руководителя организации расшифровка подписи «_____» ______________ 20 __г. АКТ ОБСЛЕДОВАНИЯ ДЛЯ
- 63. Приложение №4 НАИМЕНОВАНИЕ ОРГАНИЗАЦИИ__________________________________________ СТРУКТУРНОЕ ПОДРАЗДЕЛЕНИЕ___________________________________________ ЖУРНАЛ регистрации результатов приемочного контроля Начат_________________20__г. Окончен_______________20__г. ООО «Витамин»
- 64. 8.1. Сверить соответствие наименования поступивших детских товаров, наименования производителей, сроки годности, номер партии (если есть) в
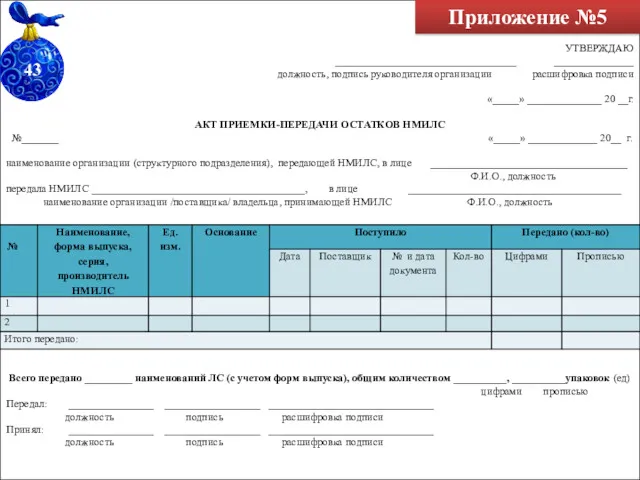
- 65. Приложение №5 УТВЕРЖДАЮ __________________________________ _______________ должность, подпись руководителя организации расшифровка подписи «_____» ______________ 20 __г. АКТ
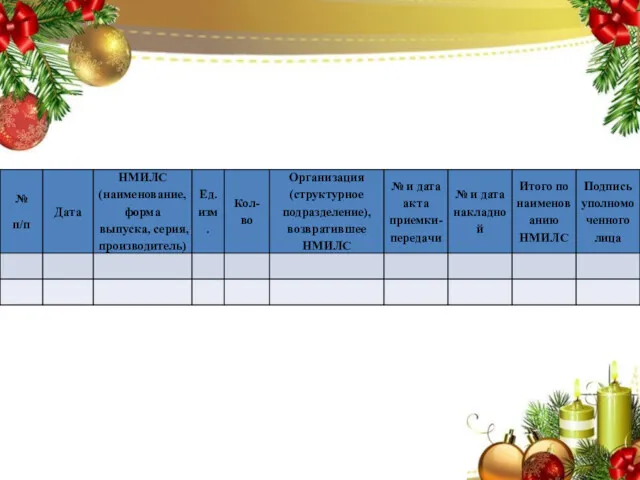
- 66. Приложение №6 НАИМЕНОВАНИЕ ОРГАНИЗАЦИИ__________________________________________ СТРУКТУРНОЕ ПОДРАЗДЕЛЕНИЕ___________________________________________ ЖУРНАЛ УЧЕТА РЕГИСТРАЦИИ ОПЕРАЦИЙ ПО СБОРУ ОСТАТКОВ НМИЛС Начат_________________20__г. Окончен_______________20__г.
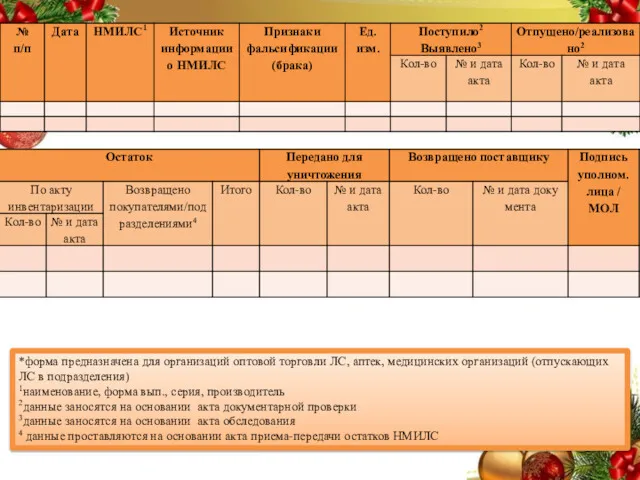
- 68. Приложение №7 НАИМЕНОВАНИЕ ОРГАНИЗАЦИИ__________________________________________ СТРУКТУРНОЕ ПОДРАЗДЕЛЕНИЕ___________________________________________ ЖУРНАЛ УЧЕТА ВЫЯВЛЕННЫХ НЕПРИГОДНЫХ ДЛЯ МЕДИЦИНСКОГО ИСОЛЬЗОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ Начат_________________20__г.
- 69. *форма предназначена для организаций оптовой торговли ЛС, аптек, медицинских организаций (отпускающих ЛС в подразделения) 1наименование, форма
- 70. Приложение №8 НАИМЕНОВАНИЕ ОРГАНИЗАЦИИ__________________________________________ СТРУКТУРНОЕ ПОДРАЗДЕЛЕНИЕ___________________________________________ ЖУРНАЛ УЧЕТА ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ С ОГРАНИЧЕННЫМ СРОКОМ ГОДНОСТИ Начат_________________20__г. Окончен_______________20__г.
- 72. Скачать презентацию





















































 Микозы стоп
Микозы стоп Воспалительные заболевания женских половых органов
Воспалительные заболевания женских половых органов Обновленные практические рекомендации EHRA по применению новых оральных антикоагулянтов
Обновленные практические рекомендации EHRA по применению новых оральных антикоагулянтов Фармакокинетика и фармакодинамика
Фармакокинетика и фармакодинамика Нежелательные явления вакцинации
Нежелательные явления вакцинации Нарушения сердечного ритма и проводимости
Нарушения сердечного ритма и проводимости Мастер-класс. Травматологический конкурс
Мастер-класс. Травматологический конкурс Пародонтальные индексы
Пародонтальные индексы Пищевые отравления немикробной этиологии
Пищевые отравления немикробной этиологии Selenium. Минерал красоты и молодости
Selenium. Минерал красоты и молодости Развитие НЭК у новорожденных на ИВЛ
Развитие НЭК у новорожденных на ИВЛ Здоровье и здоровый образ жизни
Здоровье и здоровый образ жизни Физиологические роды. Обезболивание родов
Физиологические роды. Обезболивание родов Дені сау бала кабинетінде жұмыс істеп, есепке жазу
Дені сау бала кабинетінде жұмыс істеп, есепке жазу Уборка помещений в больнице (для санитаров)
Уборка помещений в больнице (для санитаров) Қан және лимфа айналымының бұзылуы
Қан және лимфа айналымының бұзылуы Multiple Sclerois
Multiple Sclerois Хроническая сердечна недостаточность
Хроническая сердечна недостаточность Заворот толстого отдела кишечника у лошади
Заворот толстого отдела кишечника у лошади Полиомиелит. Симптомы и формы полиомиелита
Полиомиелит. Симптомы и формы полиомиелита Побочные эффекты, возрастные особенности применения лекарственных средств
Побочные эффекты, возрастные особенности применения лекарственных средств Экология микроорганизмов. Микрофлора почвы, воды, воздуха. Роль внешней среды в распространении и передаче патогенных микробов
Экология микроорганизмов. Микрофлора почвы, воды, воздуха. Роль внешней среды в распространении и передаче патогенных микробов Исследование сердечной деятельности
Исследование сердечной деятельности Последствия нейротравмы
Последствия нейротравмы Сколиоз. Симптомы и причины
Сколиоз. Симптомы и причины Виды рентгенологической диагностики заболеваний мочеполовой системы
Виды рентгенологической диагностики заболеваний мочеполовой системы Строение и функции нервной системы человека
Строение и функции нервной системы человека Цитологическая диагностика опухолей кожи. Строение кожи
Цитологическая диагностика опухолей кожи. Строение кожи