Содержание
- 2. Особо опасные (трансграничные) болезни Часть III 8. ЧУМА КРУПНОГО РОГАТОГО СКОТА 9. ЧУМА МЕЛКИХ ЖВАЧНЫХ 10.
- 3. ЧУМА КРУПНОГО РОГАТОГО СКОТА (лат. — Pestis bovum)
- 4. Чума крупного рогатого скота (лат. — Pestis bovum) — остро протекающая контагиозная септицемическая болезнь домашних и
- 6. Распространение чумы в мире было отмечено уже в IV в. Заразный характер её установил Д. Раммазини
- 7. Возбудитель — РНК-содержащий вирус, относящийся к роду Morbillivirus семейства Paramixaviridae. По своей вирулентности штаммы вируса чумы
- 8. Эпизоотология К чуме восприимчивы животные всех видов из отряда парнокопытных. В естественных условиях из сельскохозяйственных животных
- 9. Чума отличается высокой контагиозностью. В свежих очагах эпизоотии носят взрывоподобный опустошительный характер с 90-100%-ной летальностью животных
- 10. Вирус передается в контактной форме через мочу, кал, слюну и истечения из глаз и носа больных
- 11. Патогенез Вскоре после заражения вирус проникает в кровь, разносится по всему организму и размножается преимущественно в
- 12. В некротизированных участках и по краям эрозий откладывается фибрин и образуются псевдомембраны, в результате чего возникают
- 13. Инкубационный период длится 4-5, реже 9 дней и более. Симптомы болезни разнообразны и зависят от штамма
- 14. Температура тела повышается до 41-42°С, снижается удой, животное угнетено, аппетит отсутствует. Со второго дня болезни развиваются
- 15. Нарушения деятельности желудочно-кишечного тракта проявляются запором, затем профузным поносом с примесью крови на последней стадии. Животные
- 16. С самого основания в 1945 году ФАО признала, что борьба с чумой крупного рогатого скота необходима
- 17. GREP (Глобальная программа ликвидации чумы крупного рогатого скота), была создана ФАО в 1994 году для закрытия
- 18. Посредством GREP ФАО в тесном сотрудничестве с Всемирной организацией охраны здоровья животных (МЭБ) координировала усилия такого
- 19. Ликвидация чумы крупного рогатого скота в глобальном масштабе требовала научного подтверждения о том, что болезнь больше
- 20. Ликвидация чумы крупного рогатого скота стала возможной благодаря передовой науке, тесному международному сотрудничеству и самоотверженной работе
- 21. Уолтер Плоурайт (Walter Plowright) – лидер в идеологии, научном и технологическом обеспечении глобальной эрадикации* ЧКРС, широко
- 22. Вакцина использовалась для защиты поголовья скота во время вспышек болезни. После того, как удалось взять её
- 23. В истории человечества это вторая победа в борьбе со смертельными микробами!!! Первой стала ликвидация оспы людей,
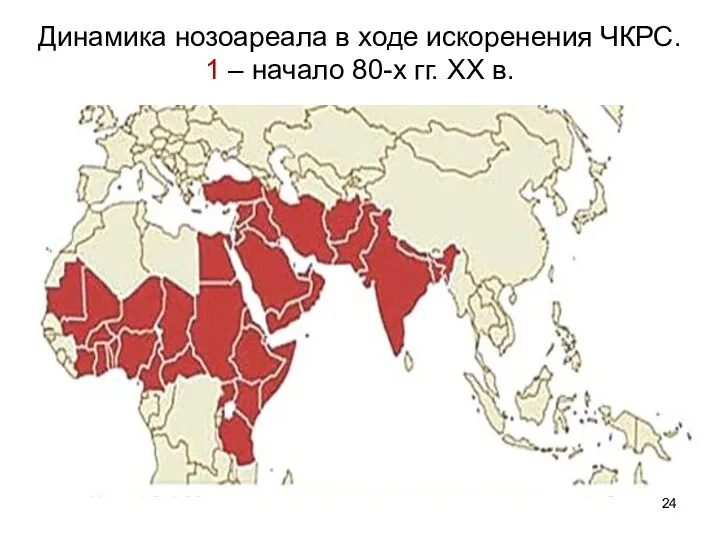
- 24. Динамика нозоареала в ходе искоренения ЧКРС. 1 – начало 80-х гг. XX в.
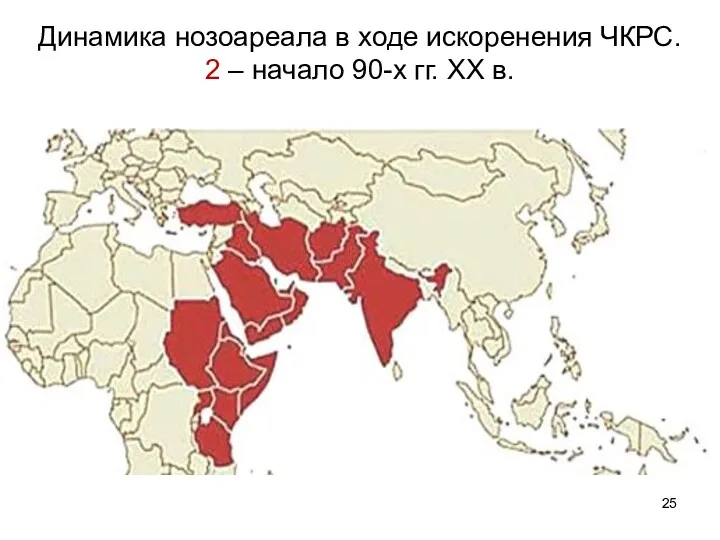
- 25. Динамика нозоареала в ходе искоренения ЧКРС. 2 – начало 90-х гг. XX в.
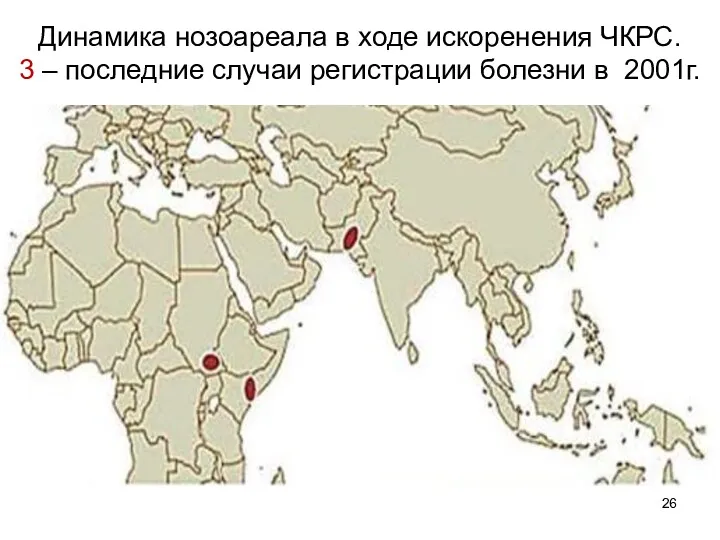
- 26. Динамика нозоареала в ходе искоренения ЧКРС. 3 – последние случаи регистрации болезни в 2001г.
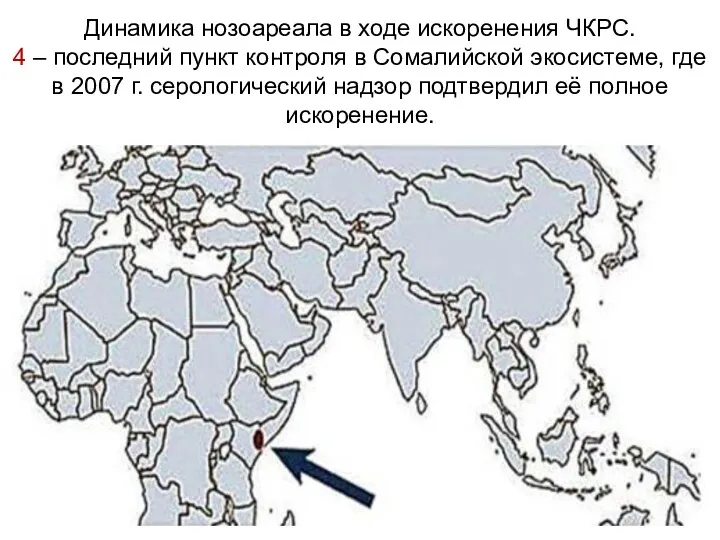
- 27. Динамика нозоареала в ходе искоренения ЧКРС. 4 – последний пункт контроля в Сомалийской экосистеме, где в
- 28. Судя по всем имеющимся научным данным, чума крупного рогатого скота была полностью ликвидирована, и её возбудитель
- 29. ЧУМА МЕЛКИХ ЖВАЧНЫХ (pestis ovium et caprarum)
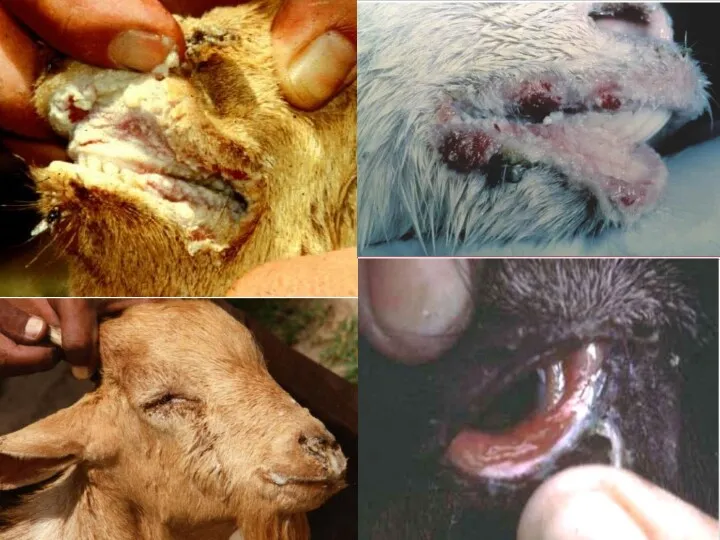
- 30. Чума мелких жвачных — это трансграничная, эмерджентная, контагиозная вирусная болезнь овец и коз, характеризующаяся лихорадкой (40,0
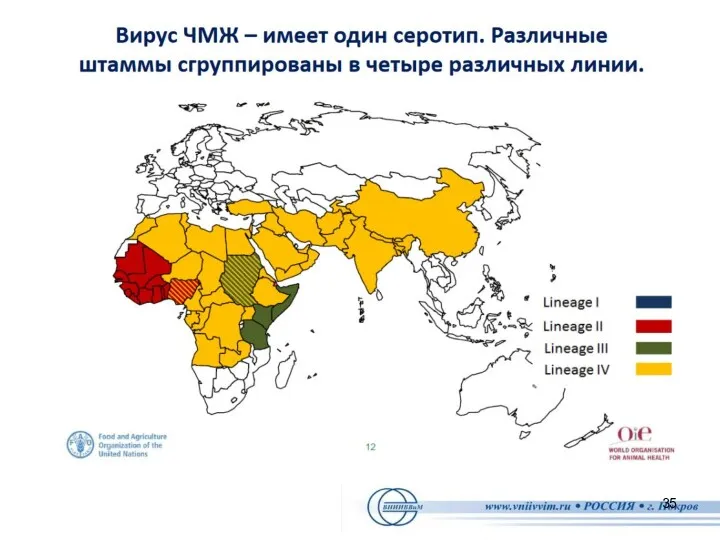
- 32. Этиология Возбудитель болезни – РНК-геномный вирус, относящийся к семейству Paramixoviridae, подсемейству Morbillivirus, имеет слегка овальную форму,
- 33. Эпизоотологические данные В естественных условиях болезнь поражает коз и овец всех возрастов, но тяжелее протекает у
- 34. Вирус передается аэрогенным и алиментарным путем, при прямом контакте овец и коз с больными животными, а
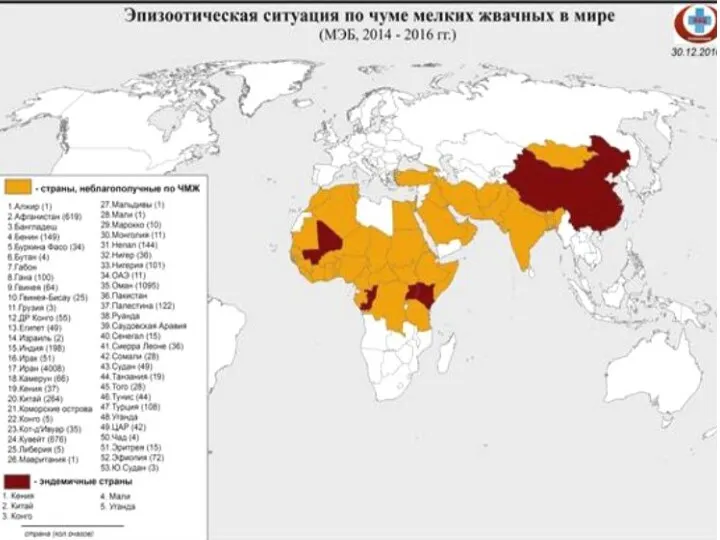
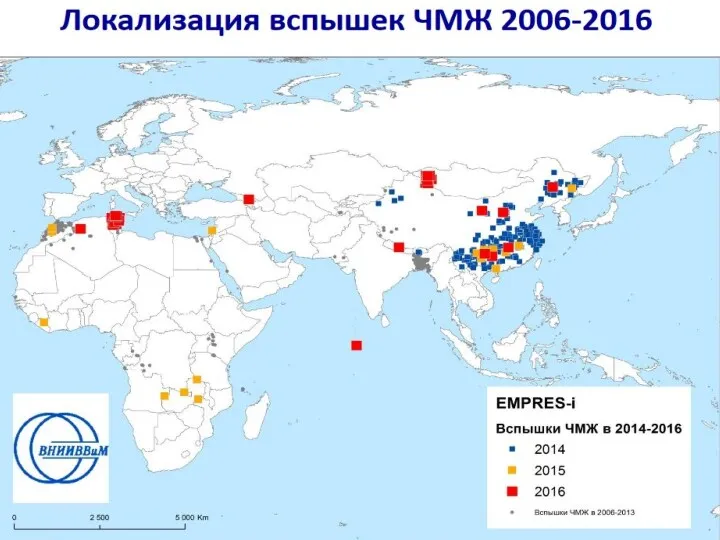
- 36. Распространение ЧМЖ в мире. Современный нозоареал ЧМЖ (в период 2001 – 2011 гг.) охватывал страны Африки
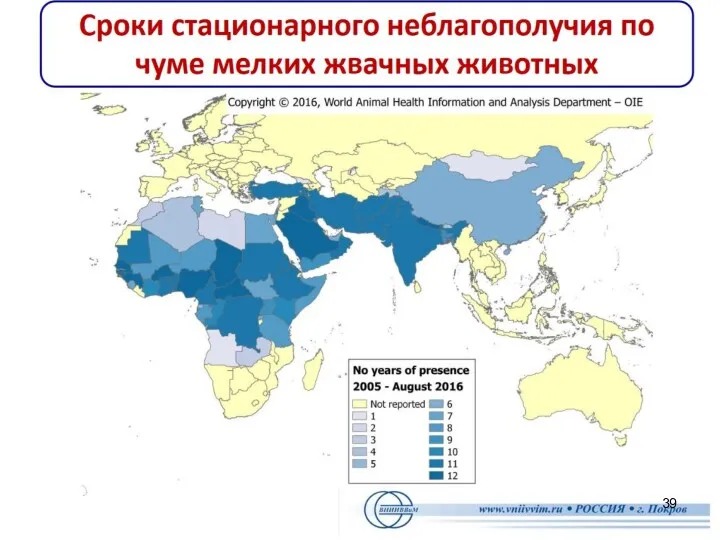
- 38. Болезнь имеет тенденцию к территориальному распространению в пределах вышеназванных континентов. По данным МЭБ за период 2001-2011
- 40. Болезнь регистрируется в Турции, Китае установлена в Таджикистане и Казахстане. По сообщению департамента ветеринарии Республики Таджикистан
- 41. В 2003 г. в южной части территории Республики Казахстан произошла вспышка неизвестной инфекции среди овец и
- 43. При проведении клинических, эпизоотологических и серологических исследований установлено, что причиной заболевания и падежа животных на территории
- 44. Уровень летальности в Азии у овец колебался от 7,5 до 66%, у коз от 16,6 до
- 45. При этом сезонность болезни была выражена слабо, подъемы регистрации вспышек и заболеваемости наблюдали в периоды (годы),
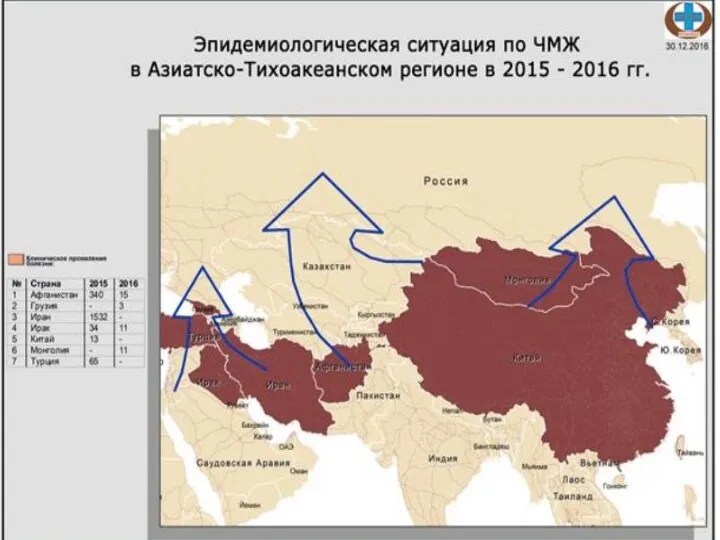
- 46. Напряженная эпизоотическая ситуация по ЧМЖ сохраняется и в настоящее время, зарегистрированы в 2012 г. новые очаги
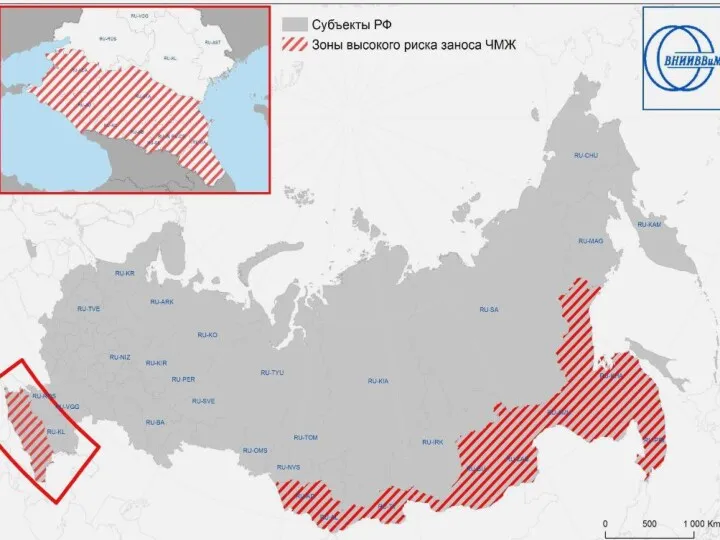
- 49. В результате исследований и математико-картографического моделирования потенциального нозоареала на территорию Закавказья, Средней и Центральной Азии установлен
- 51. Эпизоотические риски Основной путь заноса в незаражённые регионы – ввоз/перемещение заражённых животных (в т.ч. при незаконном
- 53. АФРИКАНСКАЯ ЧУМА ЛОШАДЕЙ (лат. — Pestis africana equorum; англ. — African Horse Sickness; африканская чума однокопытных,
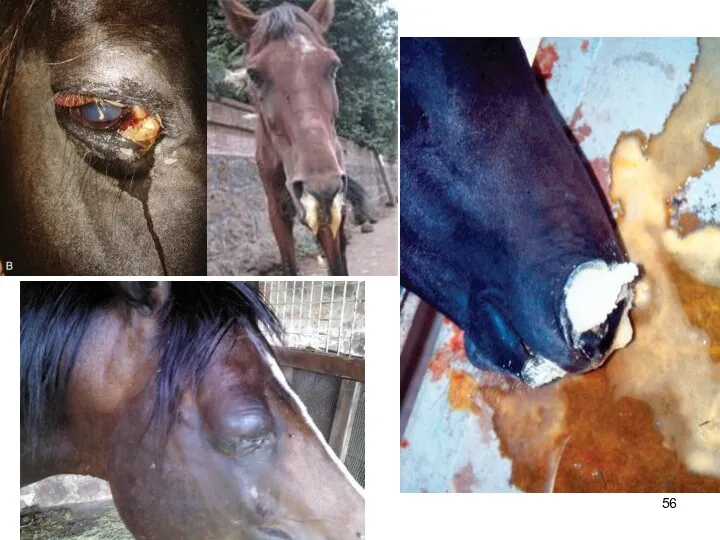
- 54. Африканская чума лошадей — вирусная трансмиссивная болезнь, характеризующаяся лихорадкой, отеками, геморрагическими явлениями, поражением органов дыхания, высокой
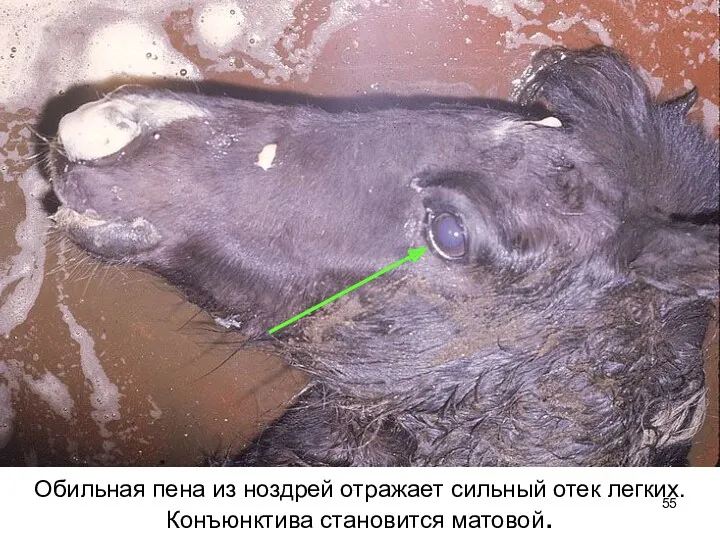
- 55. Обильная пена из ноздрей отражает сильный отек легких. Конъюнктива становится матовой.
- 57. Возбудитель - РНК-содержащий вирус, относящийся к роду Orbovirus семейства Reoviridae. Его находят в крови, внутренних органах,
- 58. В естественных условиях к болезни наиболее восприимчивы однокопытные животные: лошади, мулы, лошаки, ослы и зебры. Могут
- 59. Животные заражаются обычно при выпасе в ночное время. Пастьба на этих участках днем не представляет опасности.
- 60. Болезнь впервые обнаружена в Южной Африке в 1919 г. Вирусная природа установлена R. Alexander (1943). До
- 61. Распро-странение Африканс-кой чумы лошадей на Африкан-ском континенте.
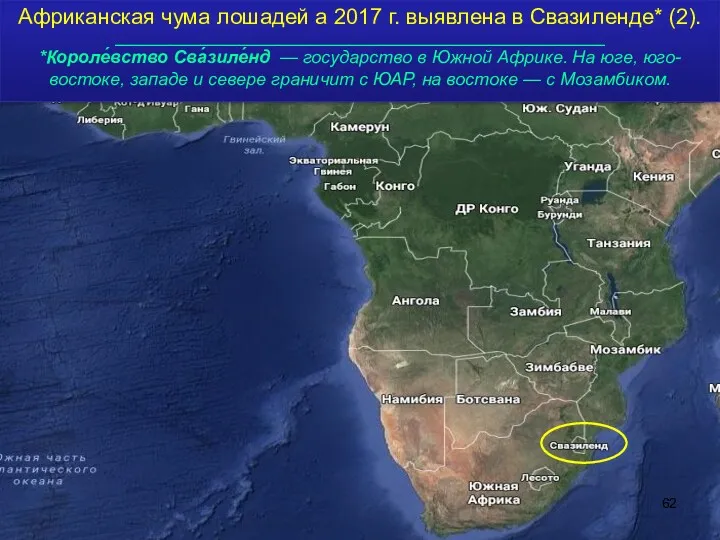
- 62. Африканская чума лошадей а 2017 г. выявлена в Свазиленде* (2). _______________________________________________________________ *Короле́вство Сва́зиле́нд — государство в
- 63. ГУБКООБРАЗНАЯ ЭНЦЕФАЛОПАТИЯ КРУПНОГО РОГАТОГО СКОТА (ГЭ КРС) (англ. — Bovine Spongiforme Encephalopatie — BSE; болезнь бешеной/сумасшедшей
- 64. Губкообразная энцефалопатия крупного рогатого скота (ГЭ КРС) -медленно развивающаяся инфекционная прионная трансмиссивная болезнь взрослого крупного рогатого
- 65. Расстройство координации движений (Атаксия задних конечностей)
- 66. Распространение Губкообразная энцефалопатия впервые была зарегистрирована в 1985—1986 годах в Великобритании под названием «болезнь бешеной коровы».
- 67. В последующие 10 лет произошло распространение ГЭ КРС на другие страны — Франция, Португалия, Швейцария, Германия,
- 68. Неблагополучными по ГЭ КРС за 7 лет (с 2002 до 2009 г.) являлись Англия, Ирландия, Португалия,
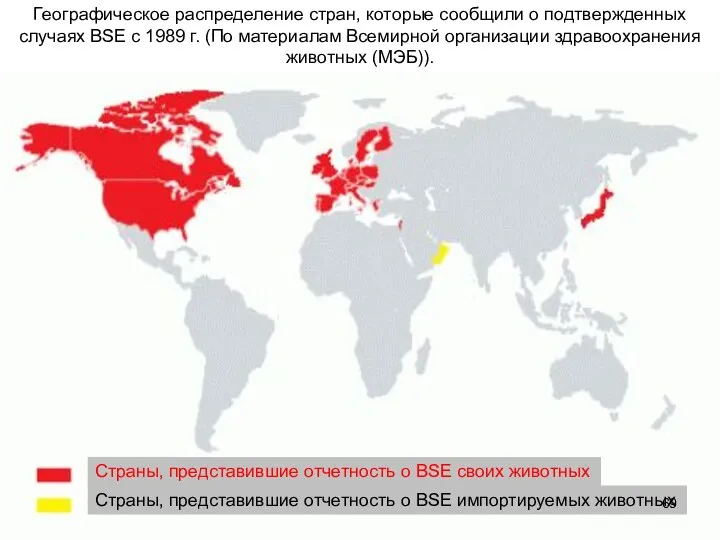
- 69. Страны, представившие отчетность о BSE импортируемых животных Страны, представившие отчетность о BSE своих животных Географическое распределение
- 70. Экономический ущерб ГЭ КРС нанесла европейским странам громадный экономический ущерб, ввиду того, что было уничтожено около
- 71. Было уничтожено около 4 миллионов голов крупного рогатого скота.
- 72. Этиология. К настоящему времени в мире принята прионная концепция ГЭ КРС. Прион — в переводе означает
- 73. Сам возбудитель представлен только белком без нуклеиновой кислоты и поэтому выдерживает кипячение, многократное замораживание и оттаивание,
- 74. В качестве дезинфицирующего средства используют 8%-й раствор гидрооксида натрия, с воздействием на возбудителя в течении 1
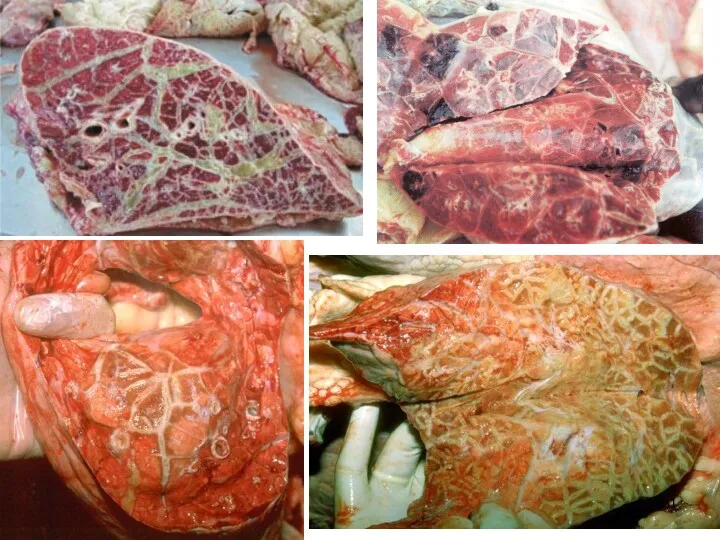
- 75. КОНТАГИОЗНАЯ ПЛЕВРОПНЕВМОНИЯ КРУПНОГО РОГАТОГО СКОТА (повальное воспаление лёгких крупного рогатого скота)
- 76. Контагиозная плевропневмония крупного рогатого скота (лат. — Pleuropneumonia contagiosa bovum; англ. — Bovine contagious pleuropneumoniae; повальное
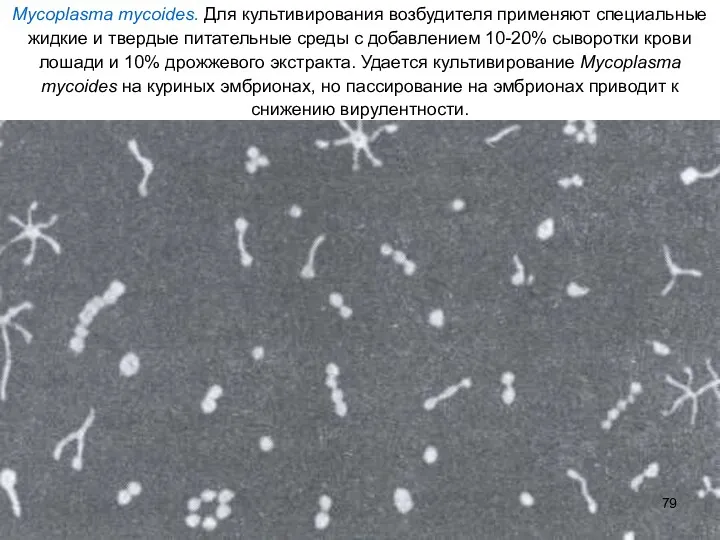
- 78. Возбудитель болезни Mycoplasma mycoides в мазках из экссудата, а также из культур, как и другие микоплазмы,
- 79. Mycoplasma mycoides. Для культивирования возбудителя применяют специальные жидкие и твердые питательные среды с добавлением 10-20% сыворотки
- 80. Источник возбудителя инфекции — больные и переболевшие КПП животные, у которых до наступления полной инкапсуляции пораженных
- 82. Первое сообщение о повальном воспалении легких (ПВЛ) крупного рогатого скота (1696) принадлежит Валентини. Инфекционную природу контагиозной
- 83. КПП крупного рогатого скота в европейской части России впервые была установлена в 1824-1825 гг. Иенсеном и
- 84. В странах мира к настоящему времени ареал КПП также сократился. Однако она все ещё регистрируется в
- 86. ЛИХОРАДКА ДОЛИНЫ РИФТ (rift vallei fever)
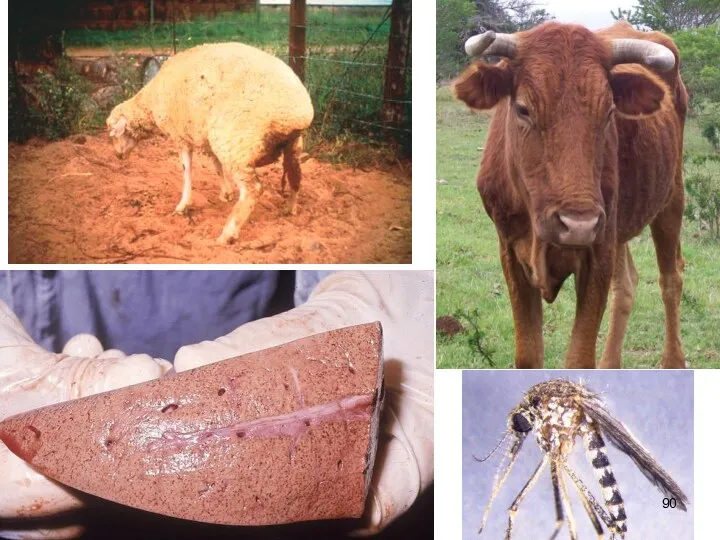
- 87. Лихорадка долины Рифт (энзоотический гепатит рогатого скота; Febris vallis Rift, Hepatitis enzootica — лат., Rift valley
- 88. Возбудитель Болезнь вызывается мелким РНК-содержащим вирусом, отнесённым к семейству Phenuiviridae рода Phlebovirus вида Rift Valley fever
- 89. Эпизоотологические данные. Болезнь носит сезонный характер. В дождливый период количество больных животных увеличивается. От больного животного
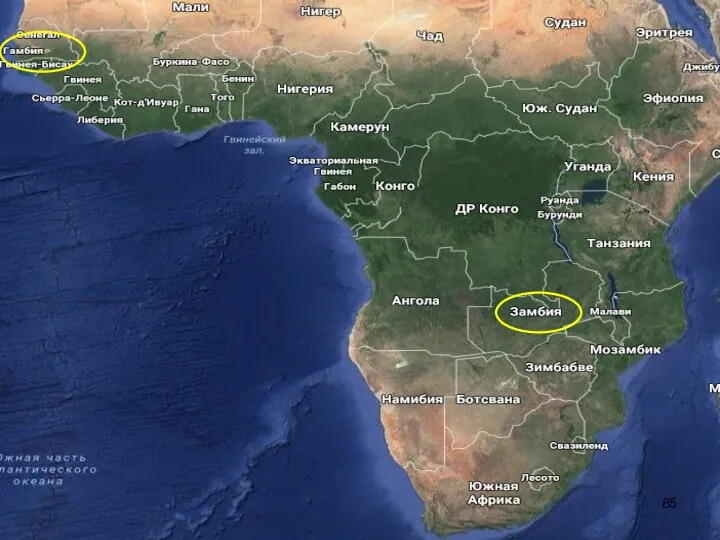
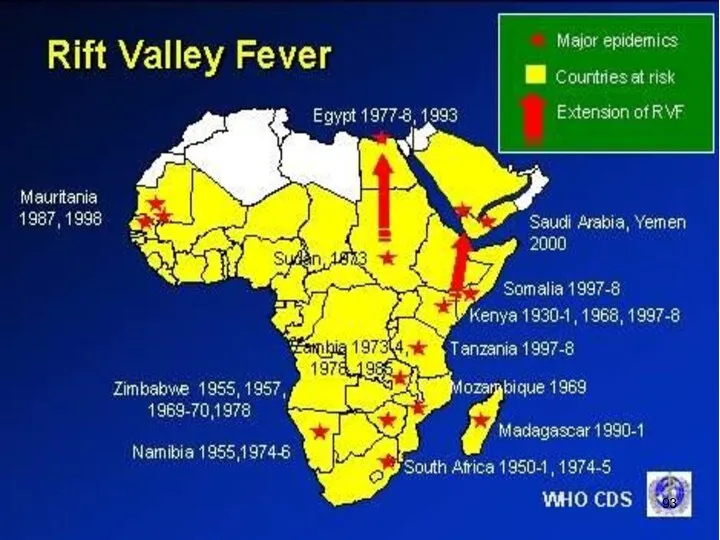
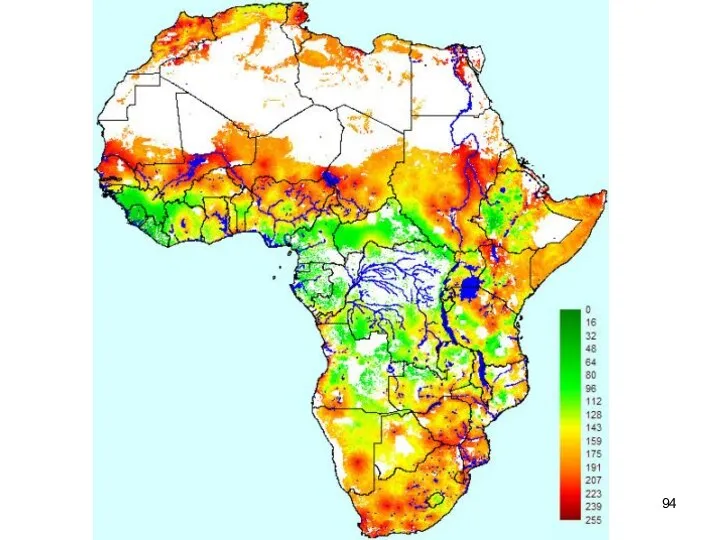
- 91. Эпизоотии ЛДР на африканском континенте весьма часты и наносят большой экономический ущерб, поскольку вызывают практически поголовную
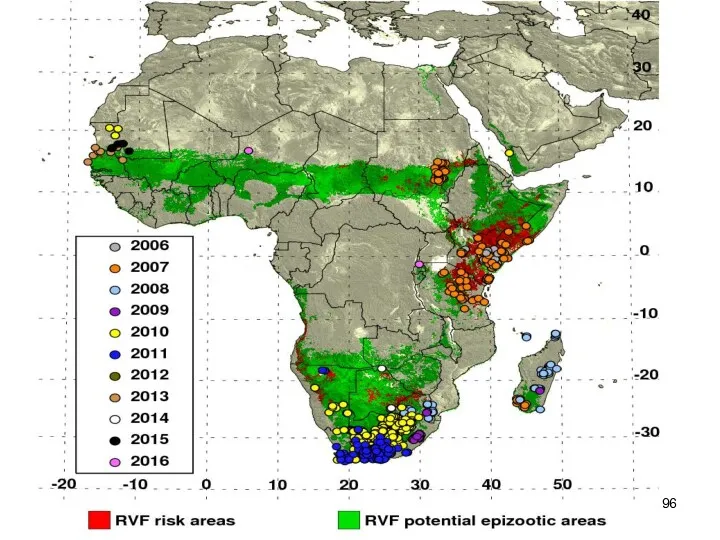
- 92. За последние два десятилетия этот возбудитель, циркулировавший ранее лишь в восточной и южной частях Африки, появился
- 95. В 2007 г. Международное эпизоотическое бюро отнесло к числу особо опасных и экономически значимых болезней животных,
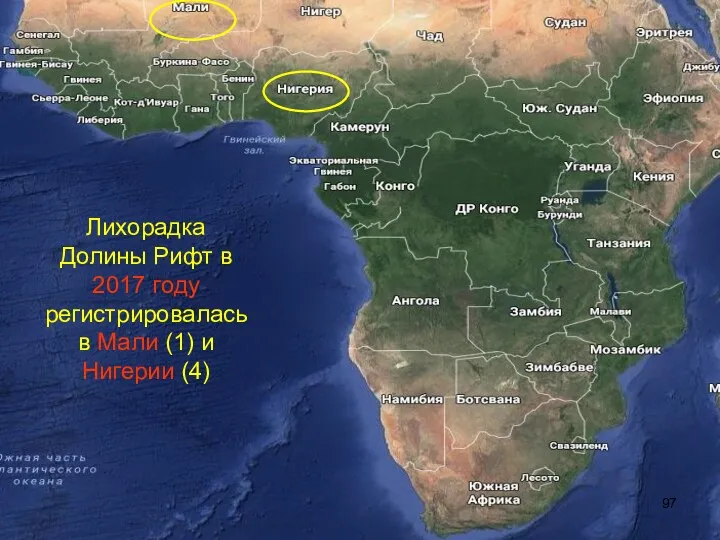
- 96. Мали Нигерия
- 97. Лихорадка Долины Рифт в 2017 году регистрировалась в Мали (1) и Нигерии (4)
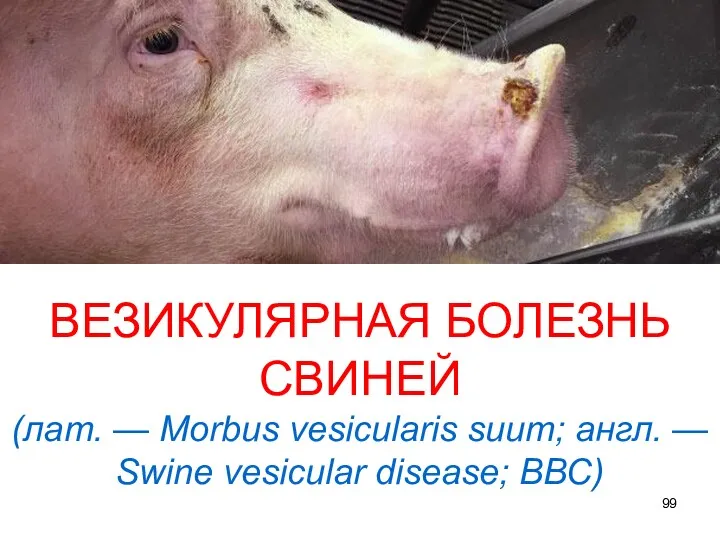
- 99. ВЕЗИКУЛЯРНАЯ БОЛЕЗНЬ СВИНЕЙ (лат. — Morbus vesicularis suum; англ. — Swine vesicular disease; ВВС)
- 100. Везикулярная болезнь свиней — контагиозная болезнь, характеризующаяся лихорадкой и образованием везикул и язв на коже хоботка,
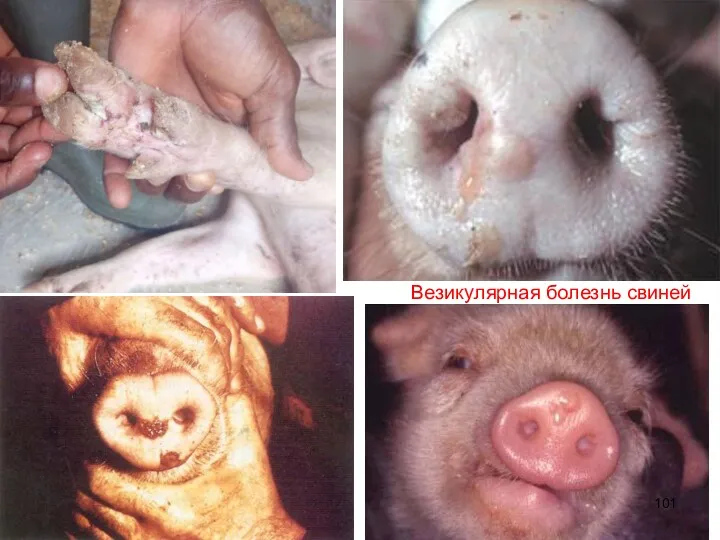
- 101. Везикулярная болезнь свиней
- 102. Впервые болезнь, клинически напоминающая ящур, была зарегистрирована и описана в Италии в 1966 г. Вирус, выделенный
- 103. Возбудитель болезни Болезнь вызывает РНК-содержащий, сферической формы вирус диаметром З0-32нм из рода Enterovirus семейства Picornaviridae. Между
- 104. Возбудитель в высоких концентрациях накапливается в эпителии пораженных участков кожи, выявляется также в лимфатических узлах и
- 105. Эпизоотология Болеют только свиньи независимо от породы, пола и возраста и кабаны. Возможно инфицирование человека. Источник
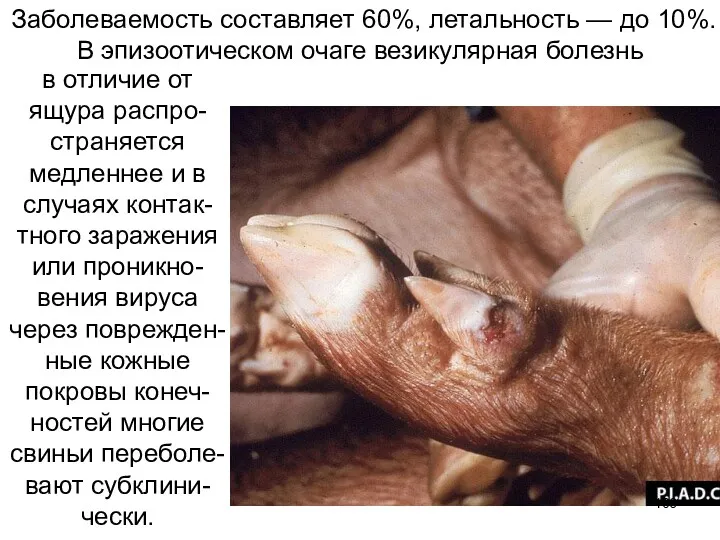
- 106. Заболеваемость составляет 60%, летальность — до 10%. В эпизоотическом очаге везикулярная болезнь в отличие от ящура
- 107. ВЕЗИКУЛЯРНЫЙ СТОМАТИТ (Stomatitis vesicularis — лат., Vesicular stomatitis — англ.)
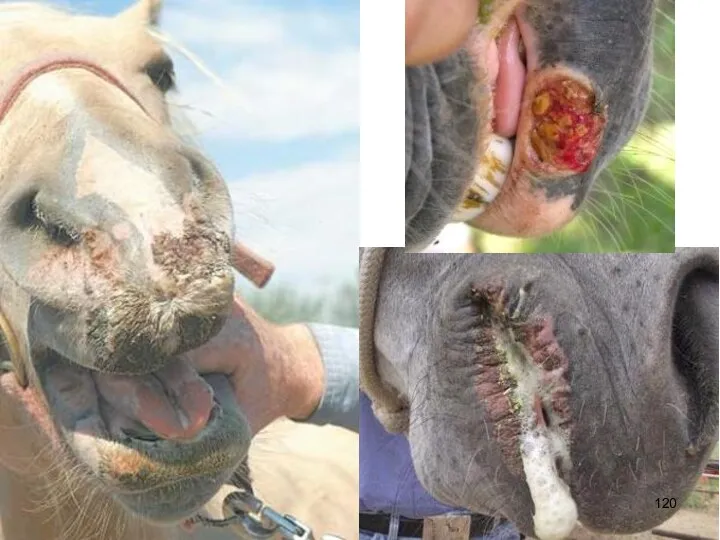
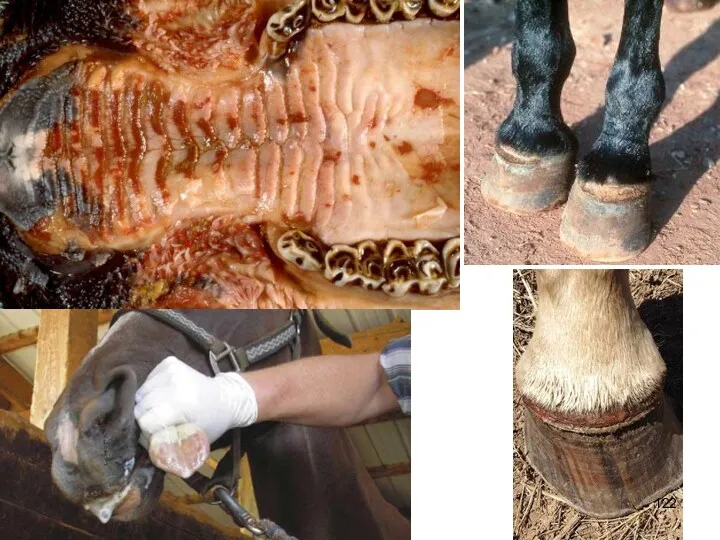
- 108. Везикулярный стоматит - остропротекающая вирусная болезнь крупного рогатого скота, лошадей и свиней, проявляющаяся лихорадкой, образованием везикул
- 109. Везикулярный стоматит впервые зарегистрирован у лошадей в 1862 г. в США, затем в 1884 и в
- 110. Первая эпизоотия везикулярного стоматита у свиней зарегистрирована в 1941 г. в Венесуэле, одновременно заболевали как скот,
- 111. В 1950 г. инфекция распространилась в Мексике. В Китае болезнь с везикулярным синдромом у скота и
- 112. В конце 1979 г. и начале 1980 г. болезнь диагностировали в странах Америки: Колумбии 22 случая,
- 113. Возбудитель везикулярного стоматита — РНК-содержащий вирус. Впервые его природу описал в 1926—1927 гг. W. Cotton. Возбудитель
- 114. Геном вируса — односпиральная молекула РНК (около 2%), выделенная из вирионов неинфекционна. При размножении вируса образуются
- 115. Эпизоотологические данные В естественных условиях болезнь протекает в виде энзоотии, реже эпизоотии, поражает от 5 до
- 116. Болезнь обычно наблюдают в летний влажный пастбищный период, который совпадает с периодом активности насекомых. С переходом
- 117. Клинические признаки Инкубационный период болезни — от 1 до 12 суток, чаще равен 2—5 суткам. Начальный
- 119. Эрозии при доброкачественном исходе болезни эпителизируются в течение 3—10 дней. Болезнь протекает от 1 до 3
- 121. Часто у коров поражаются соски, иногда развивается мастит. Везикулы могут встречаться также на слизистой оболочке носовой
- 123. БОЛЕЗНЬ НЬЮКАСЛА (псевдочума, азиатская чума, атипичная чума, пневмоэнцефалит)
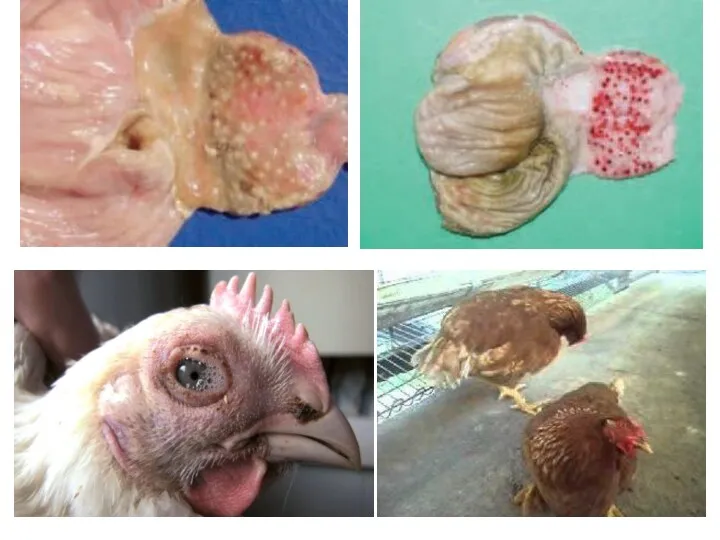
- 124. Болезнь Ньюкасла (псевдочума птиц) - высококонтагиозная болезнь птиц из отряда куриных, проявляющаяся поражением органов дыхания, желудочно-кишечного
- 125. Клинические признаки б. Ньюкасла во многом зависят от того, какой тип вируса вызвал заболевание и от
- 126. При подостром течении, которое характерно для вакцинированных цыплят, болезнь может протекать с преобладанием симптомов поражения нервной,
- 127. При респираторной форме отмечается нарушение дыхания, вдох затруднен, в птичнике слышны хрипы и карканье. Веки опухают,
- 128. Скручивание шеи, отвисание крыльев, хвоста, поражение ног
- 130. Возбудитель - РНК-содержащий вирус, размером 120-180 нм из рода парамиксвирусов, семейства Paramyxoviridae. Он обладает гемагглютинирующими свойствами
- 131. Вирус болезни Ньюкасла птиц находится во всех органах и тканях больных, в содержимом кишечника, помете, слюне,
- 132. Выделение вируса из организма начинается за 20-24 ч. до появления клинических симптомов, и продолжается весь период
- 133. Болезнь, отличающаяся от классической чумы (гриппа) птиц, была впервые зарегистрирована на острове Ява Краневельдом в 1926
- 134. В период Второй мировой войны болезнь широко распространилась в европейских странах и была занесена на территорию
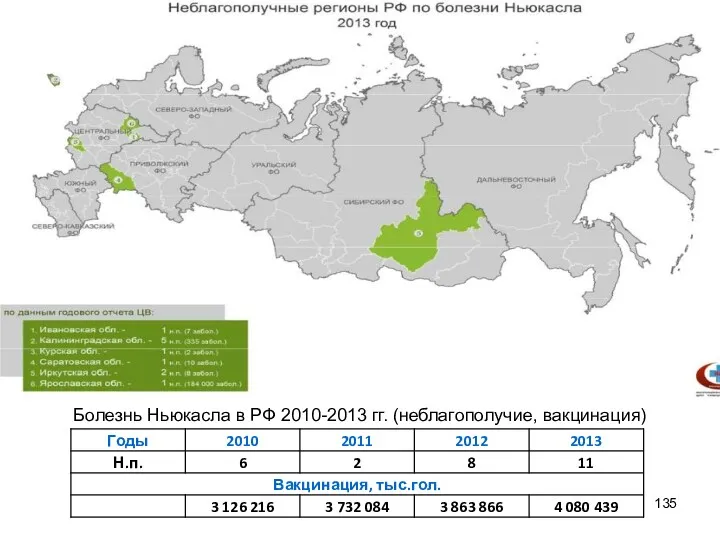
- 135. Болезнь Ньюкасла в РФ 2010-2013 гг. (неблагополучие, вакцинация)
- 136. Очень высокая эпизоотологическая опасность болезни связана с разносом возбудителя на различные континенты с птицеводческой продукцией. В
- 137. БЛАГОДАРЮ ЗА ВНИМАНИЕ! 5.02.2018 г.
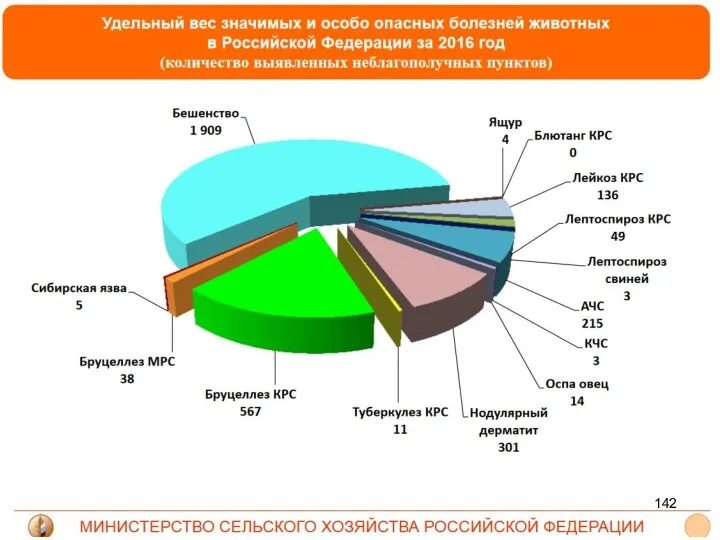
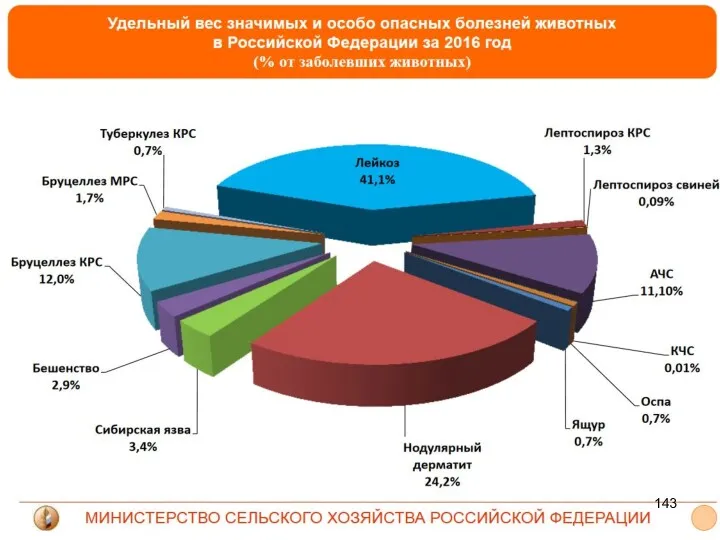
- 138. Список В Эта категория, по определению ВОЗЖ (МЭБ), включает "заразные (трансмиссивные) болезни, которые имеют существенное значение
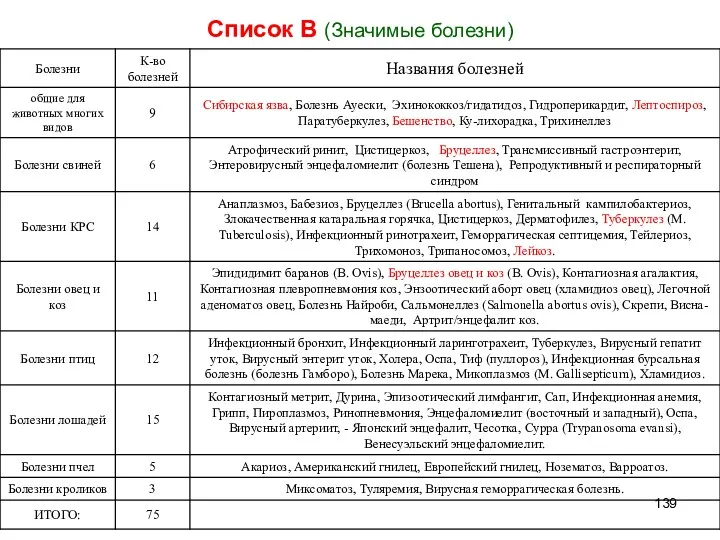
- 139. Список В (Значимые болезни)
- 140. Из болезней Списка В в России ФГБУ «ВНИИЗЖ», являющийся Центром МЭБ по сотрудничеству в области диагностики
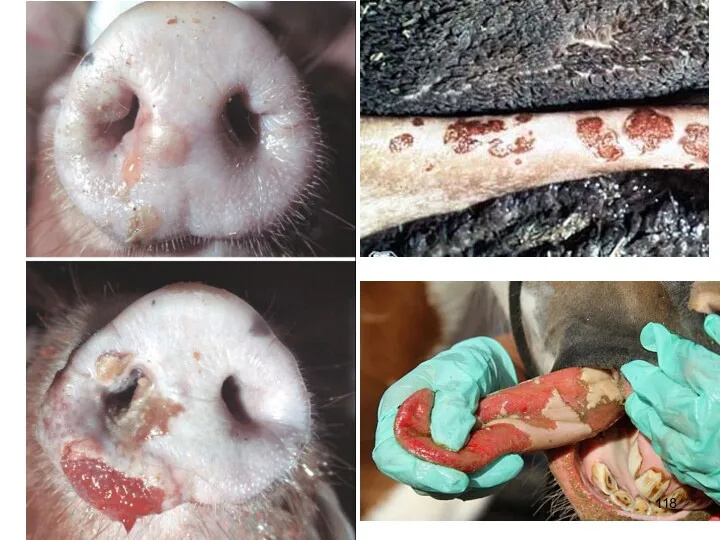
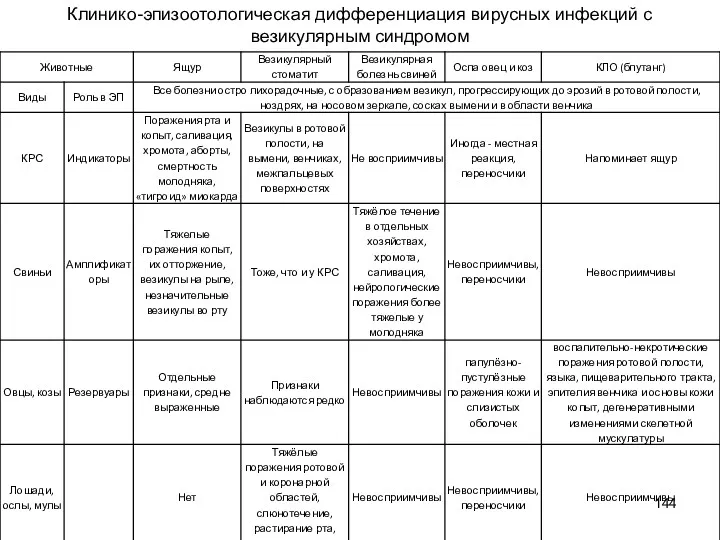
- 144. Клинико-эпизоотологическая дифференциация вирусных инфекций с везикулярным синдромом
- 145. Индикаторы – клинические признаки, позволяющие заподозрить болезнь. Амплификатор – то же, что и резервуар, но его
- 147. Скачать презентацию












































































































 Диссеминированные заболевания легких
Диссеминированные заболевания легких Под знаком красного креста
Под знаком красного креста Миокард инфаркты
Миокард инфаркты Жіночий таз і тазове дно
Жіночий таз і тазове дно Теміртапшылықты анемия
Теміртапшылықты анемия Методичні рекомендації з організації інтернатури для керівників лікарів – інтернів за фахом „педіатрія”
Методичні рекомендації з організації інтернатури для керівників лікарів – інтернів за фахом „педіатрія” Закрытая (тупая) травма живота. Перитонит. Часть I
Закрытая (тупая) травма живота. Перитонит. Часть I Полиомиелит. Протекание болезни полиомиелита
Полиомиелит. Протекание болезни полиомиелита Стандартные меры предосторожности (СМП). Основная концепция СМП. Транзиторная и резидентная микрофлора
Стандартные меры предосторожности (СМП). Основная концепция СМП. Транзиторная и резидентная микрофлора Синдром Бругада
Синдром Бругада Экстрапирамидная система
Экстрапирамидная система Гипертонический криз
Гипертонический криз Иммуногенездегі жасушааралық кооперация туралы түсінік. Антигендердің жалпы сипаттамасы
Иммуногенездегі жасушааралық кооперация туралы түсінік. Антигендердің жалпы сипаттамасы Lung abscess
Lung abscess Қан арнасының сыйымдылығы мен циркуляциядағы қан көлемінің сәйкес келмеуіне байланысты гемодинамиканың
Қан арнасының сыйымдылығы мен циркуляциядағы қан көлемінің сәйкес келмеуіне байланысты гемодинамиканың Основные виды шока
Основные виды шока Водные растворы в условиях промышленного производства и их стандартизация
Водные растворы в условиях промышленного производства и их стандартизация Острая ревматическая лихорадка у детей
Острая ревматическая лихорадка у детей Сау және науқас адамдарға терең веналарының өткізгіштігін тексеру әдістерін жүргізу
Сау және науқас адамдарға терең веналарының өткізгіштігін тексеру әдістерін жүргізу Синтетические каннабиоиды. Дорога, ведущая к шизофрении
Синтетические каннабиоиды. Дорога, ведущая к шизофрении Лихорадка Денге
Лихорадка Денге Острая ревматическая лихорадка
Острая ревматическая лихорадка Растительные антисептики и противовоспалительные средства
Растительные антисептики и противовоспалительные средства Методы исследования врожденных пороков развития
Методы исследования врожденных пороков развития Особливості формування серця і стимуляція регенерації серцевої м'язової тканини в умовах сучасної медицини
Особливості формування серця і стимуляція регенерації серцевої м'язової тканини в умовах сучасної медицини Дифференциальная диагностика аллергического,вазомоторного,медикаментозного,атрофического ринита
Дифференциальная диагностика аллергического,вазомоторного,медикаментозного,атрофического ринита Иммунокомпетентные клетки. Т- и В-лимфоциты, макрофаги, их кооперация
Иммунокомпетентные клетки. Т- и В-лимфоциты, макрофаги, их кооперация Лечение заболеваний пародонта. Значение гигиены полости рта в комплексном лечении заболеваний пародонта
Лечение заболеваний пародонта. Значение гигиены полости рта в комплексном лечении заболеваний пародонта