Содержание
- 2. Острый лимфобластный лейкоз (ОЛЛ) – гетерогенная группа злокачественных клональных заболеваний системы крови, происходящих из клеток-предшественниц гемопоэза
- 3. История Alfred-Armand-Louis-Marie Velpeau (1795 – 1867) Французский анатом и хирург 1827 - Предоставление первого точного описания
- 4. История Он сообщил о случае 63-летней женщины, которая умерла от лихорадки, опухшего желудка и общей слабости.
- 5. История Virchow, Rudolf. Weißes Blut , 1845 Рудольф Людвиг Карл Вирхов (1821 - 1902) 1845 –
- 6. История 1877 Описал нормальные и изменённые лейкоциты Пауль Эрлих (1854 – 1915) Вильгельм Эбштейн (1836 –
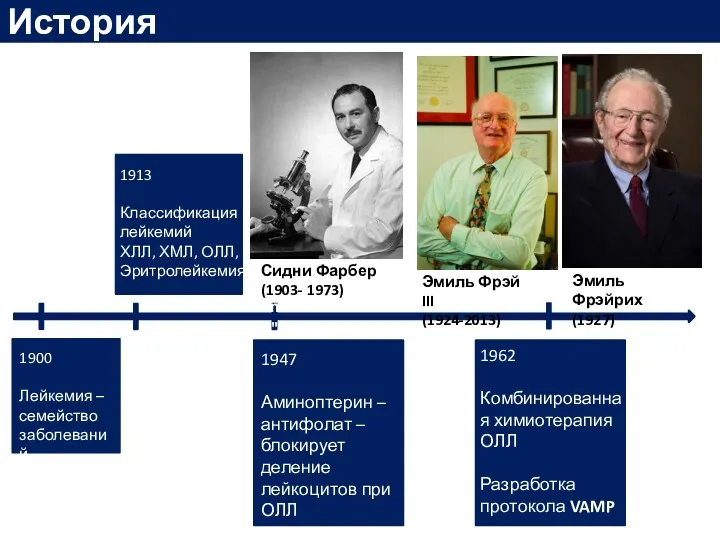
- 7. История Emil "Tom" Frei III 1900 Лейкемия – семейство заболеваний 1913 Классификация лейкемий ХЛЛ, ХМЛ, ОЛЛ,
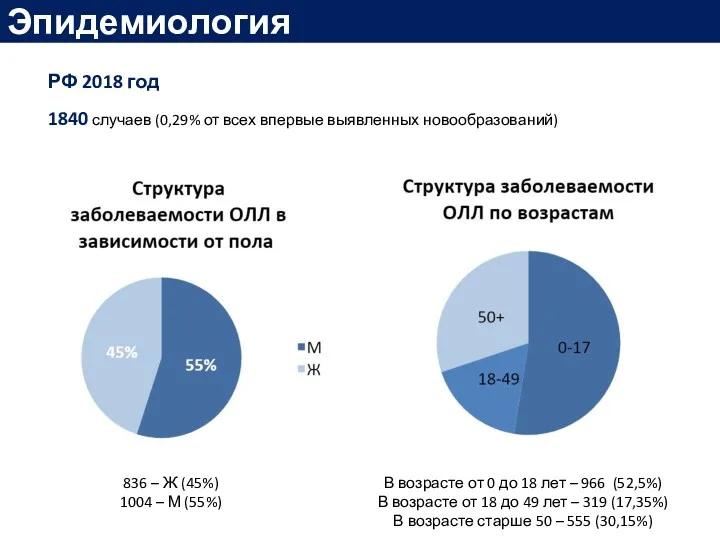
- 8. РФ 2018 год 1840 случаев (0,29% от всех впервые выявленных новообразований) 836 – Ж (45%) 1004
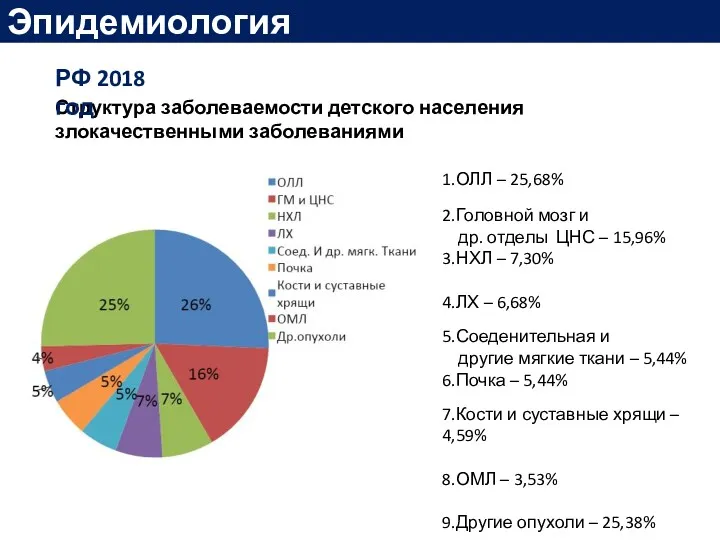
- 9. Структура заболеваемости детского населения злокачественными заболеваниями РФ 2018 год 1.ОЛЛ – 25,68% 2.Головной мозг и др.
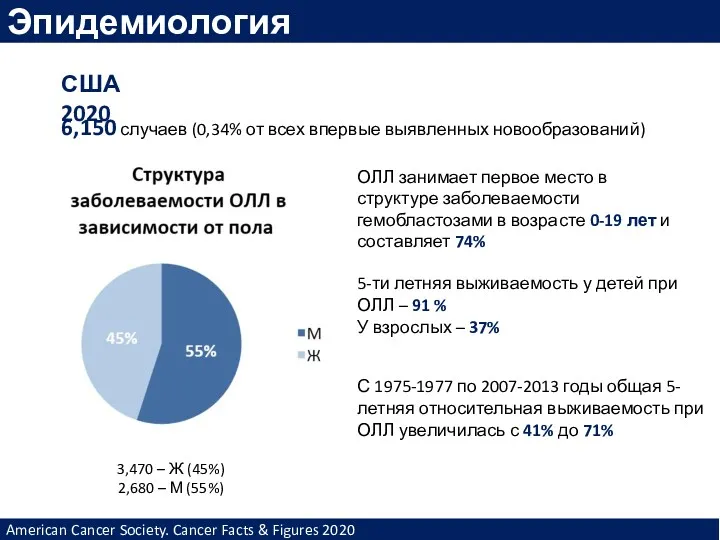
- 10. США 2020 6,150 случаев (0,34% от всех впервые выявленных новообразований) 3,470 – Ж (45%) 2,680 –
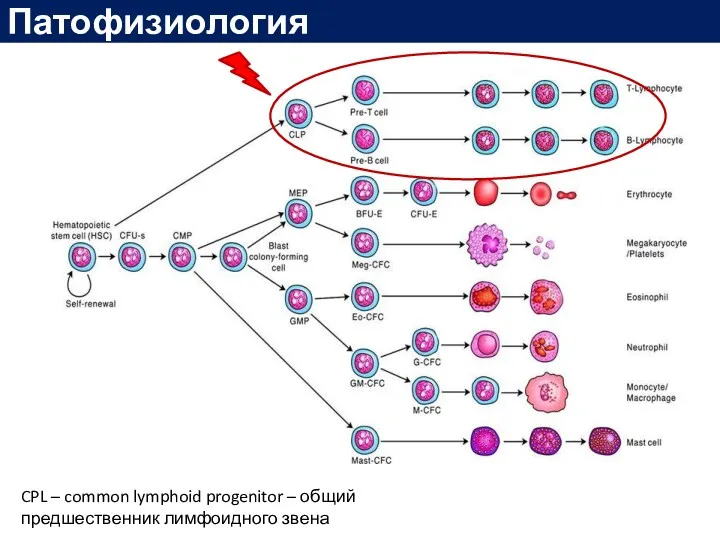
- 11. Патофизиология CPL – common lymphoid progenitor – общий предшественник лимфоидного звена
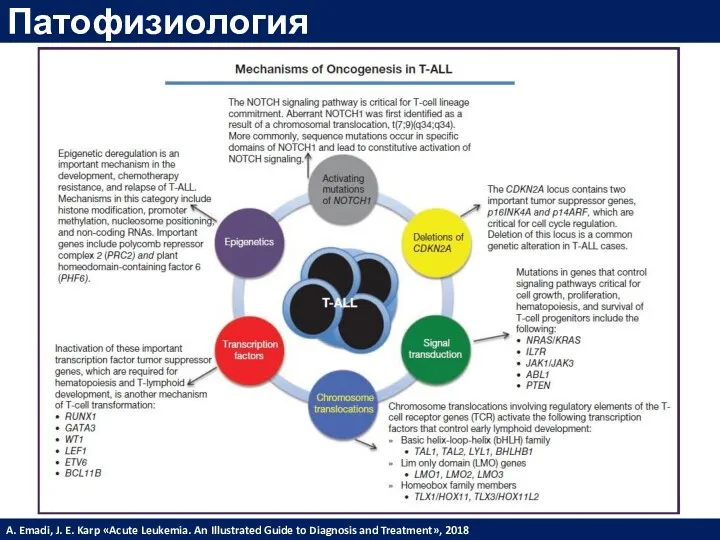
- 12. Патофизиология A. Emadi, J. E. Karp «Acute Leukemia. An Illustrated Guide to Diagnosis and Treatment», 2018
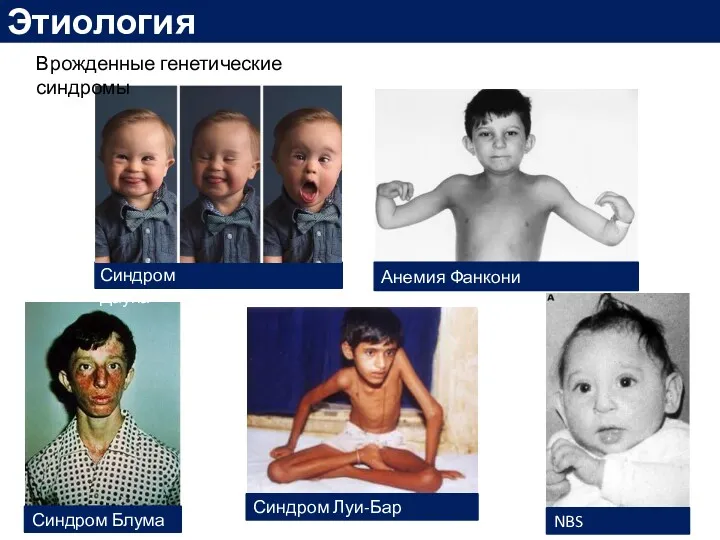
- 13. Синдром Дауна Этиология Врожденные генетические синдромы Анемия Фанкони Синдром Блума Синдром Луи-Бар NBS
- 14. Этиология • Воздействие ионизирующего излучения • Вирусы (EBV, HTLV-1) • Пестициды, химиотерапия и другие токсичные химические
- 15. Клинические проявления 1. НЕЙТРОПЕНИЯ •Повышение температуры •Тяжелые, затяжные инфекции 2. АНЕМИЯ •Тахикардия • Бледность кожных покровов
- 16. Классификация ВОЗ 2016 Arber, D. A., Orazi, A., Hasserjian, R., Thiele, J., Borowitz, M. J., Le
- 17. Диагностика Морфология Иммунофенотипировение Цитогенетика/ молекулярная генетика
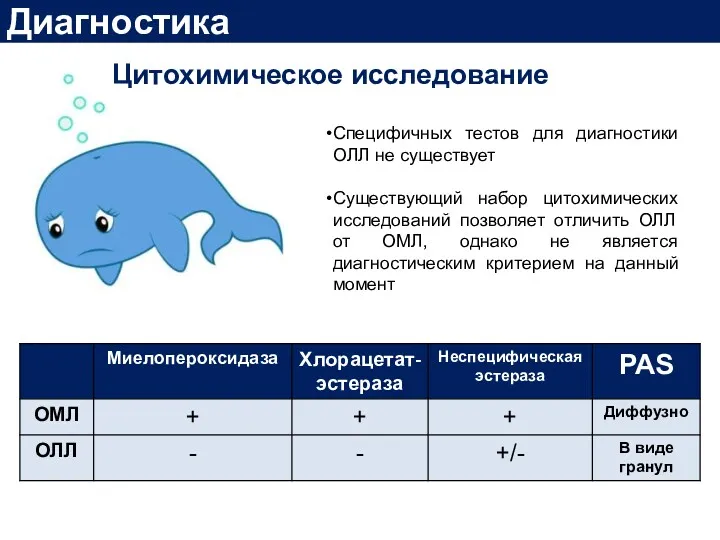
- 18. Диагностика Цитохимическое исследование Cпецифичных тестов для диагностики ОЛЛ не существует Существующий набор цитохимических исследований позволяет отличить
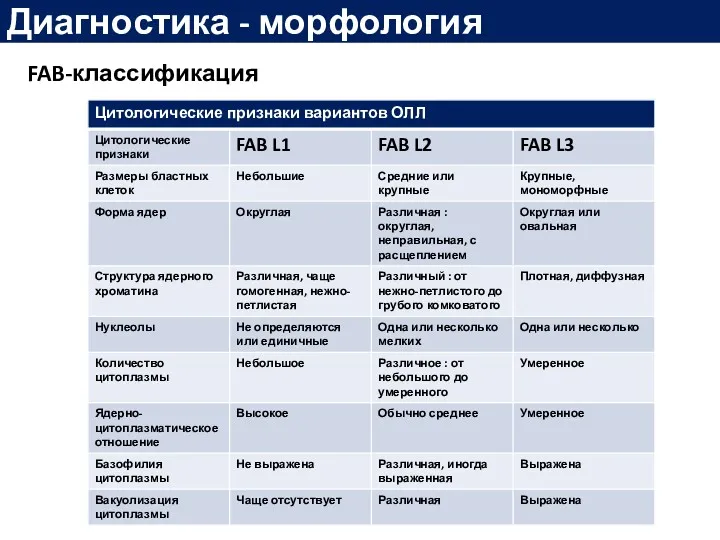
- 19. Диагностика - морфология FAB-классификация
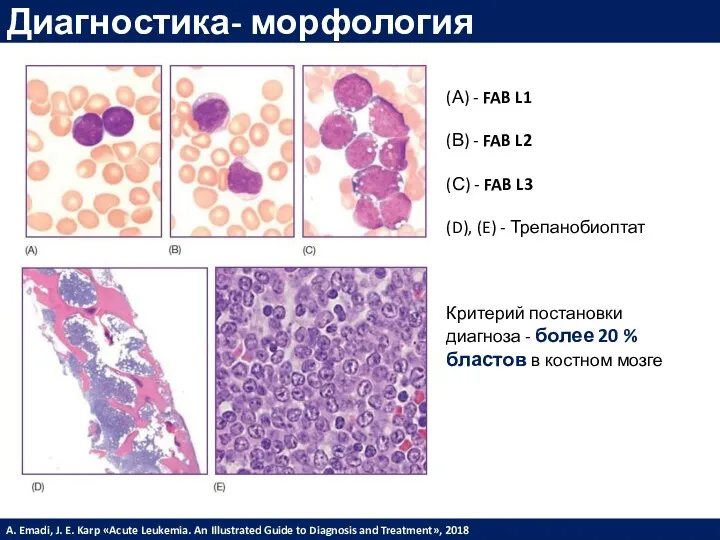
- 20. Диагностика- морфология (А) - FAB L1 (В) - FAB L2 (С) - FAB L3 (D), (E)
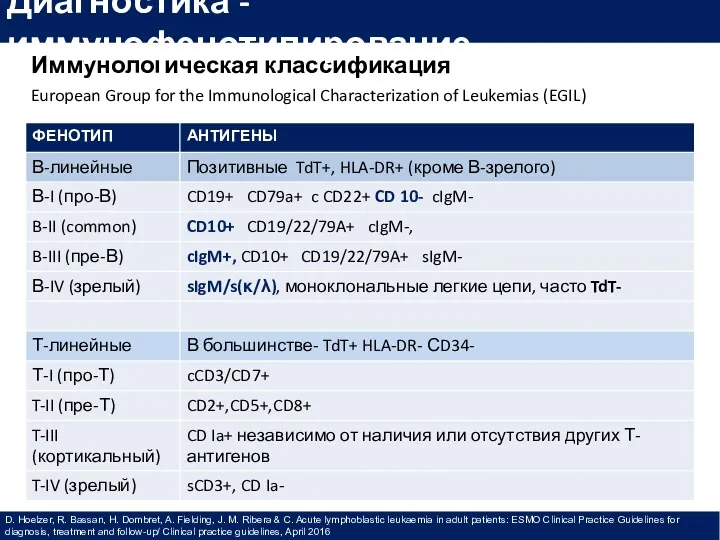
- 21. Иммунологическая классификация European Group for the Immunological Characterization of Leukemias (EGIL) Диагностика - иммунофенотипирование D. Hoelzer,
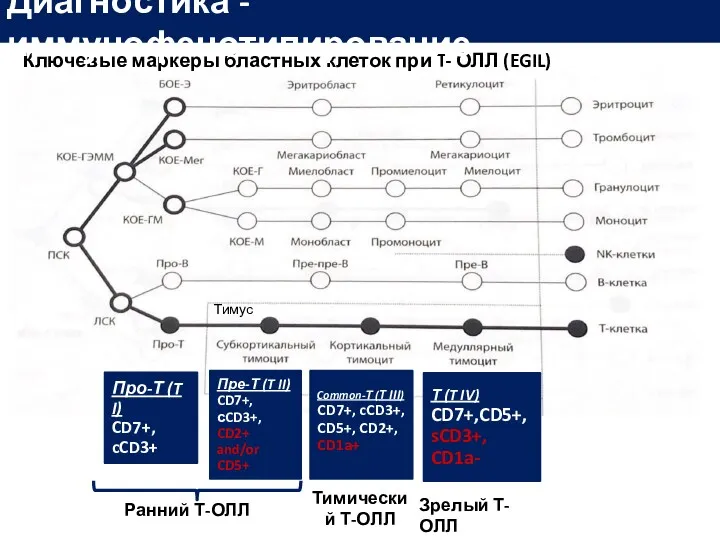
- 22. Ключевые маркеры бластных клеток при T- ОЛЛ (EGIL) Диагностика - иммунофенотипирование Про-Т (T I) CD7+, cCD3+
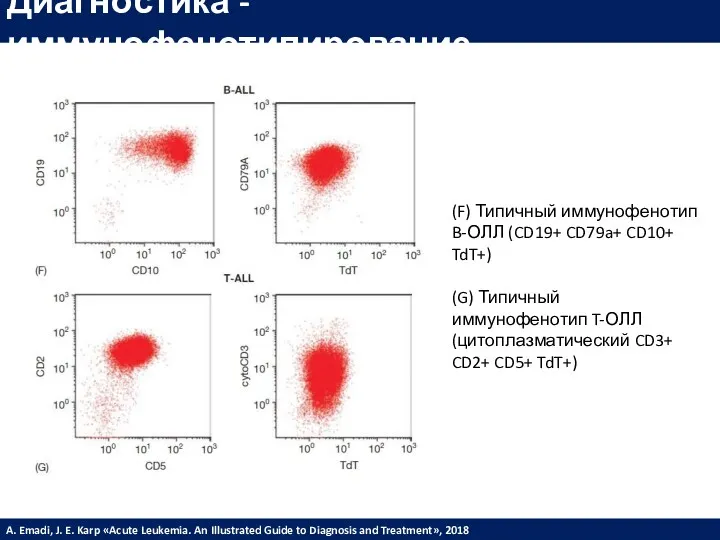
- 23. Диагностика - иммунофенотипирование (F) Типичный иммунофенотип B-ОЛЛ (CD19+ CD79a+ CD10+ TdT+) (G) Типичный иммунофенотип T-ОЛЛ (цитоплазматический
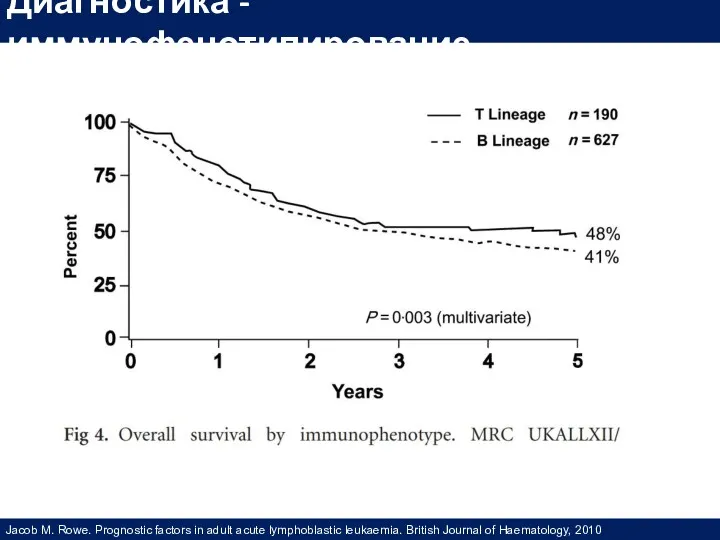
- 24. Jacob M. Rowe. Prognostic factors in adult acute lymphoblastic leukaemia. British Journal of Haematology, 2010 Диагностика
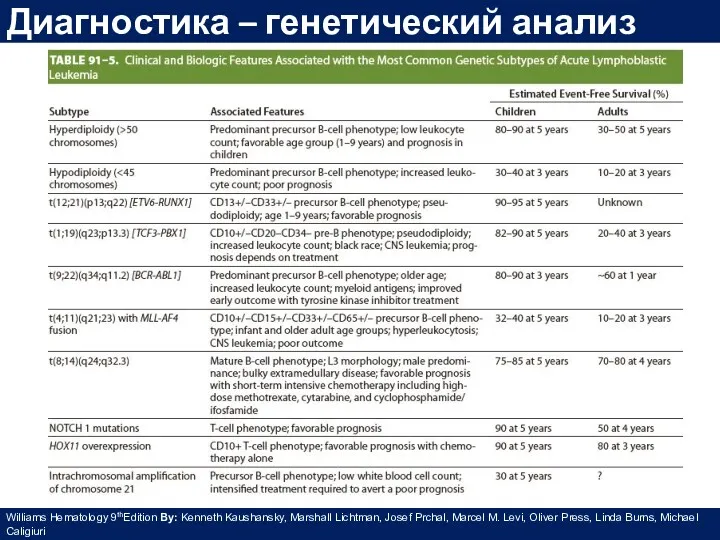
- 25. Диагностика – генетический анализ Williams Hematology 9thEdition By: Kenneth Kaushansky, Marshall Lichtman, Josef Prchal, Marcel M.
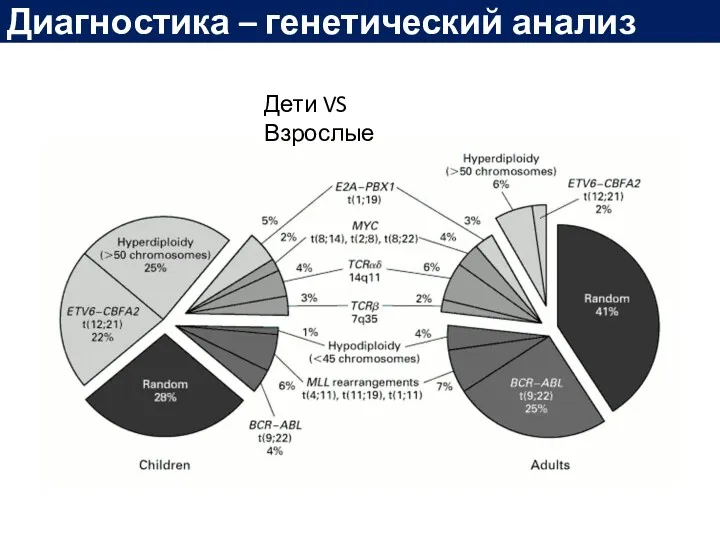
- 26. Диагностика – генетический анализ Дети VS Взрослые
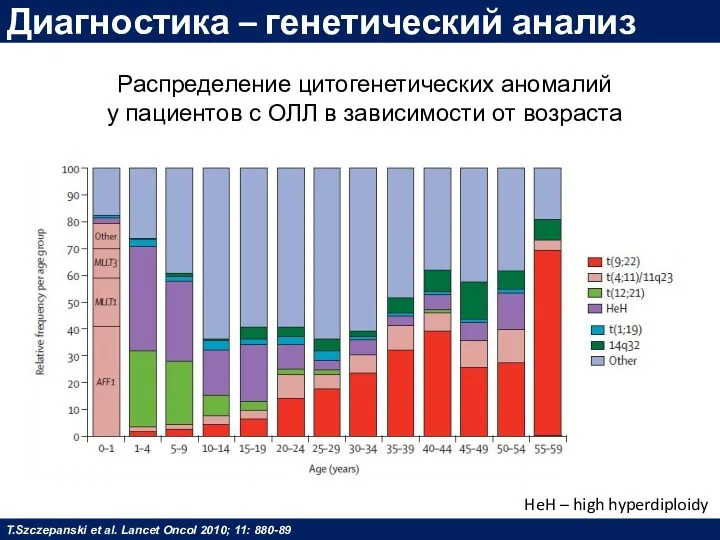
- 27. Диагностика – генетический анализ Распределение цитогенетических аномалий у пациентов с ОЛЛ в зависимости от возраста T.Szczepanski
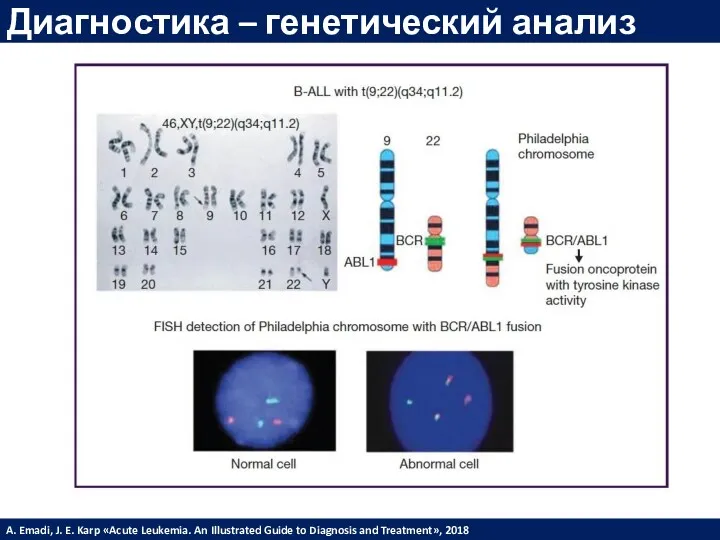
- 28. Диагностика – генетический анализ A. Emadi, J. E. Karp «Acute Leukemia. An Illustrated Guide to Diagnosis
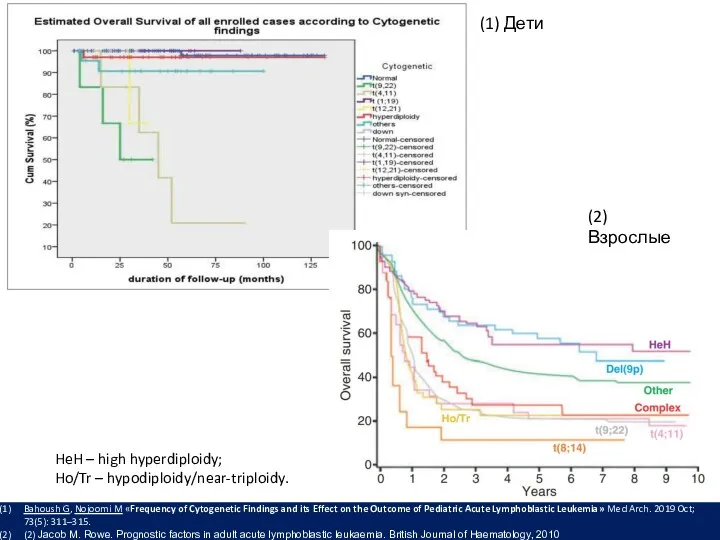
- 29. (1) Дети (2) Взрослые Bahoush G, Nojoomi M «Frequency of Cytogenetic Findings and its Effect on
- 30. Диагностика Проведение СМ-пункции В результате анализа ликвора возможны следующие варианты: • CNS1 – пункция не травматичная
- 31. Диагностика • Клинический анализ крови • Биохимический анализ крови • Коагулограмма • HLA типирование + Определение
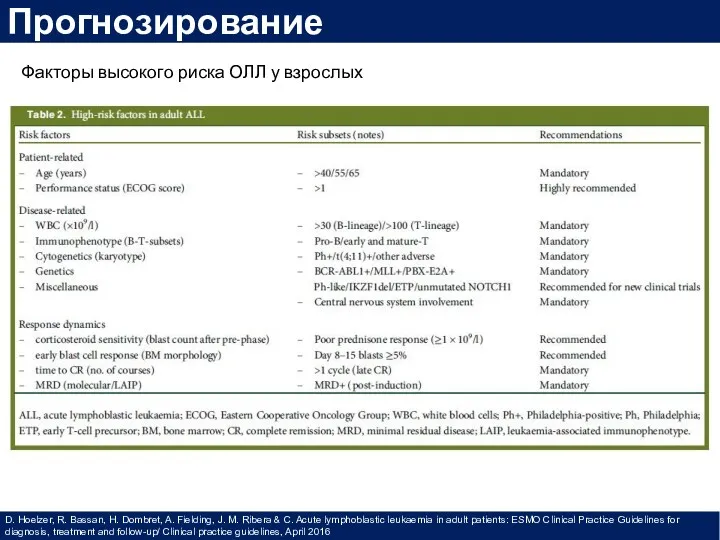
- 32. Прогнозирование D. Hoelzer, R. Bassan, H. Dombret, A. Fielding, J. M. Ribera & C. Acute lymphoblastic
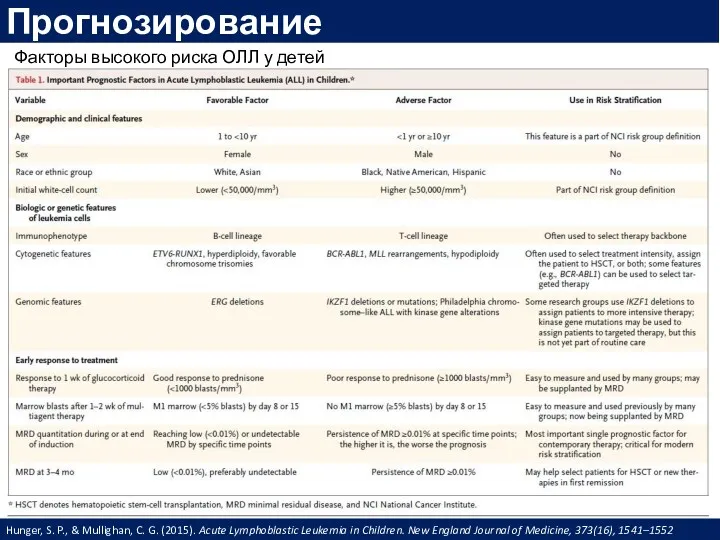
- 33. Факторы высокого риска ОЛЛ у детей Hunger, S. P., & Mullighan, C. G. (2015). Acute Lymphoblastic
- 34. Лечение Цели лечения: • Эрадикация лейкемического клона • Восстановление нормального кроветворения • Достижение длительной бессобытийной выживаемости
- 35. Критерии ответа на терапию у пациентов с ОЛЛ Лечение Полная ремиссия • Отсутствие экстрамедуллярных очагов ОЛЛ
- 36. Минимальная остаточная болезнь (МОБ; minimal residual disease – MRD) – наличие остаточных лейкемических клеток у пациента
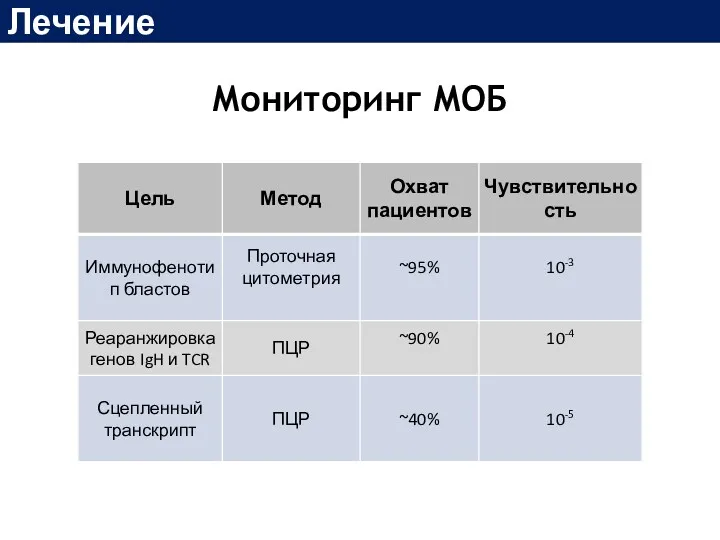
- 37. Мониторинг МОБ Лечение
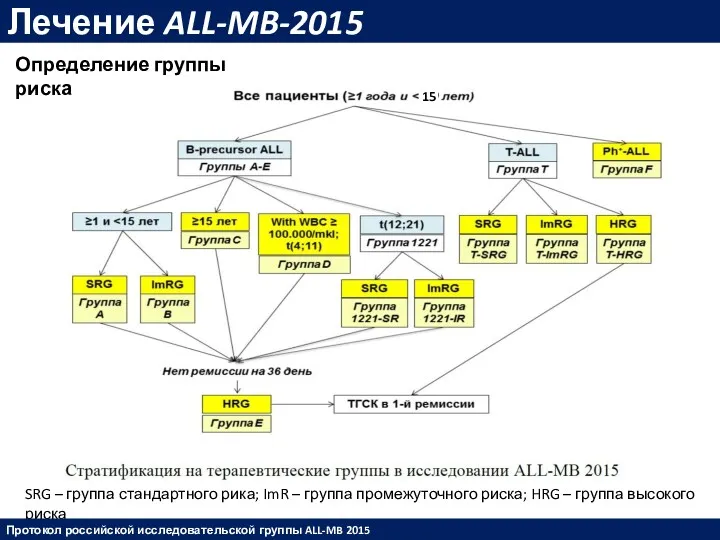
- 38. Лечение ALL-MB-2015 SRG – группа стандартного рика; ImR – группа промежуточного риска; HRG – группа высокого
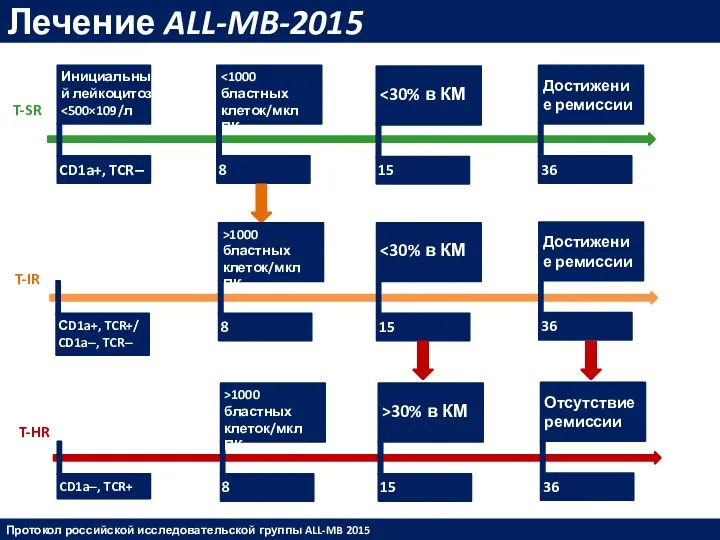
- 39. Лечение ALL-MB-2015 T-SR T-IR T-HR CD1a+, TCR‒ Инициальный лейкоцитоз 8 сутки 15 сутки 36 сутки Достижение
- 40. Лечение ALL-MB-2015 Этапы лечения острого лейкоза 1. Индукция ремиссии - это период начального лечения, целью которого
- 41. 29 3 8 15 22 1 36 Дэкс ПЭГ-АСП ВКР ДРЦ ТРИПЛЕТ ИТБ* Дэкс – дексаметазон;
- 42. Лечение ALL-MB-2015 Консолидация – 1 7 8 9 10 11 12 13 14 15 16 17
- 43. Лечение ALL-MB-2015 Вторая фаза индукции (для группы T-IR) Сутки 37 43 71 45 46 47 48
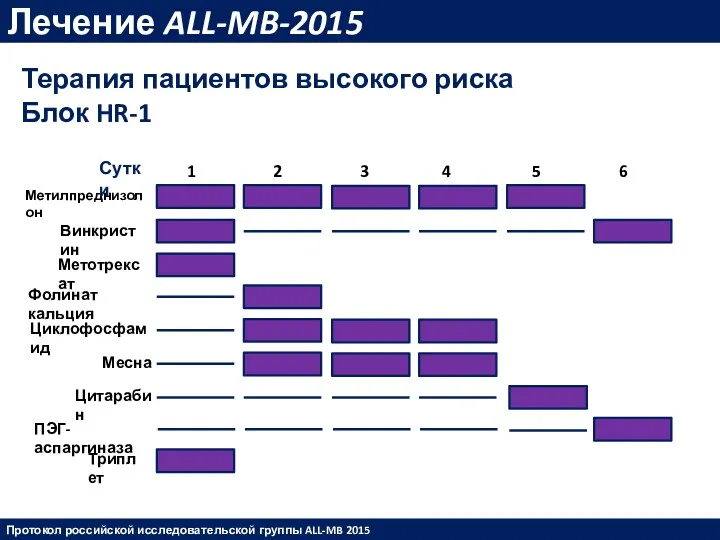
- 44. Лечение ALL-MB-2015 Терапия пациентов высокого риска Блок HR-1 Протокол российской исследовательской группы ALL-MB 2015 Метилпреднизолон Винкристин
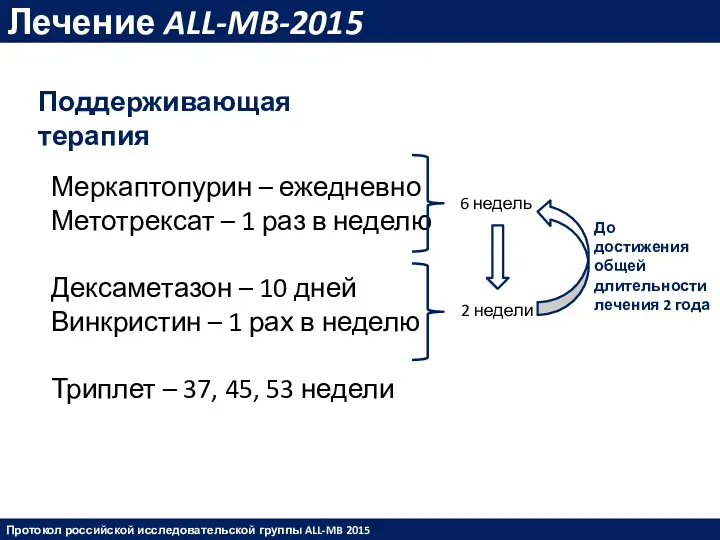
- 45. Лечение ALL-MB-2015 Меркаптопурин – ежедневно Метотрексат – 1 раз в неделю Дексаметазон – 10 дней Винкристин
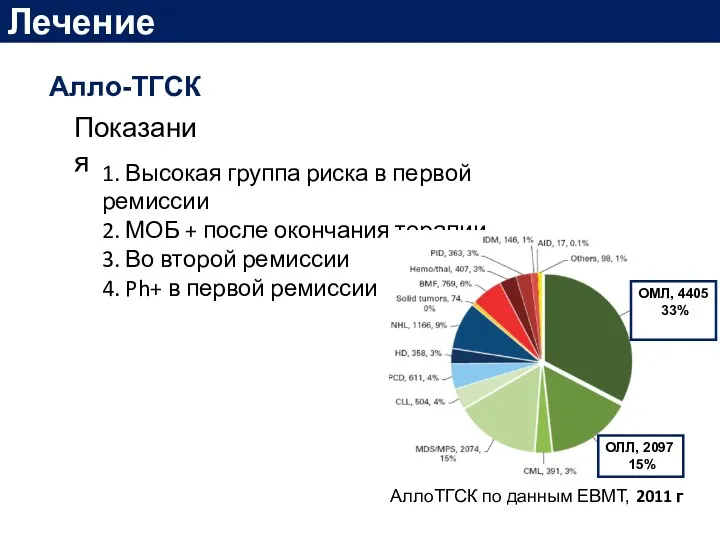
- 46. Лечение Алло-ТГСК 1. Высокая группа риска в первой ремиссии 2. МОБ + после окончания терапии 3.
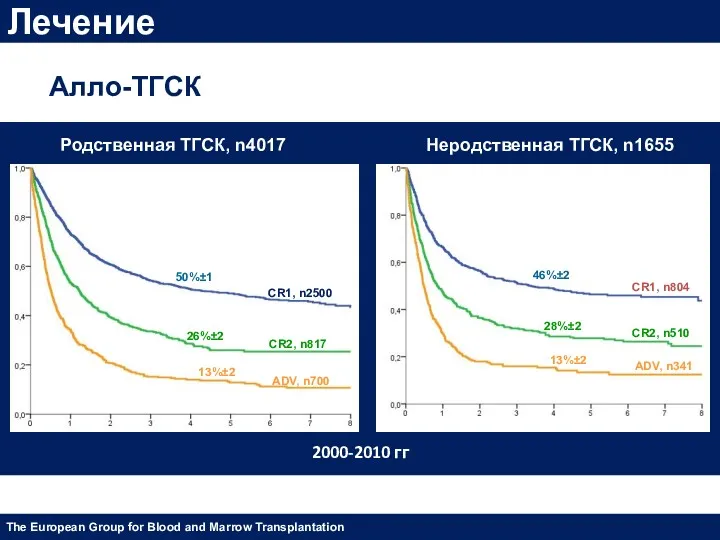
- 47. Лечение Сергей Н. Бондаренко, Иван С. Моисеев, Ольга А. Слесарчук, et al. «Аллогенная трансплантация гемопоэтических стволовых
- 48. Лечение CR1, n2500 CR1, n804 CR2, n817 CR2, n510 ADV, n700 ADV, n341 Неродственная ТГСК, n1655
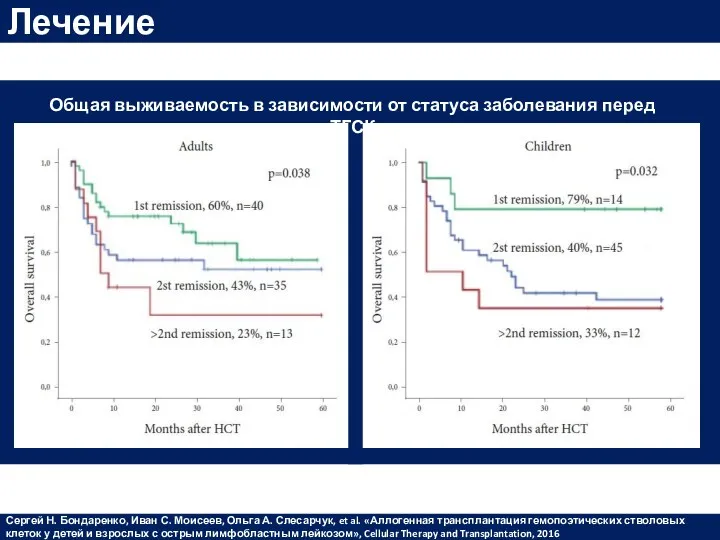
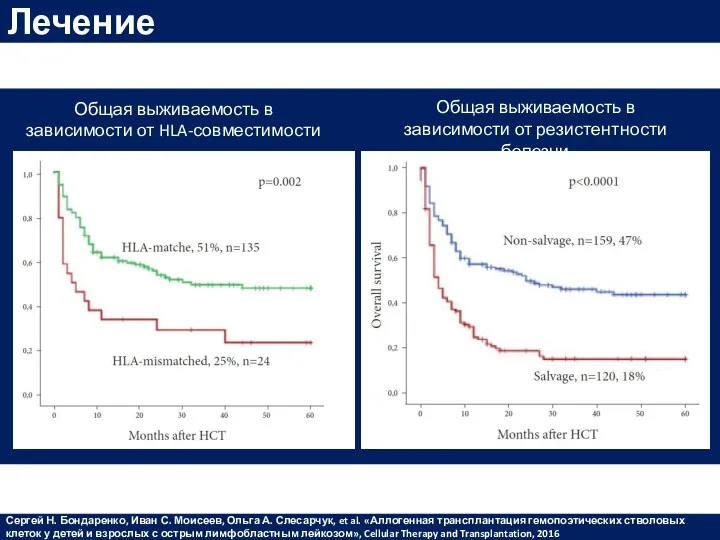
- 49. Лечение Сергей Н. Бондаренко, Иван С. Моисеев, Ольга А. Слесарчук, et al. «Аллогенная трансплантация гемопоэтических стволовых
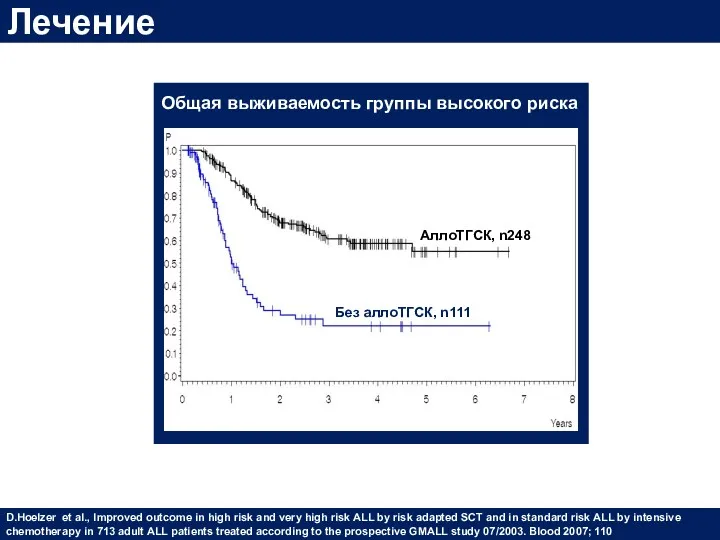
- 50. Общая выживаемость группы высокого риска АллоТГСК, n248 Без аллоТГСК, n111 Лечение D.Hoelzer et al., Improved outcome
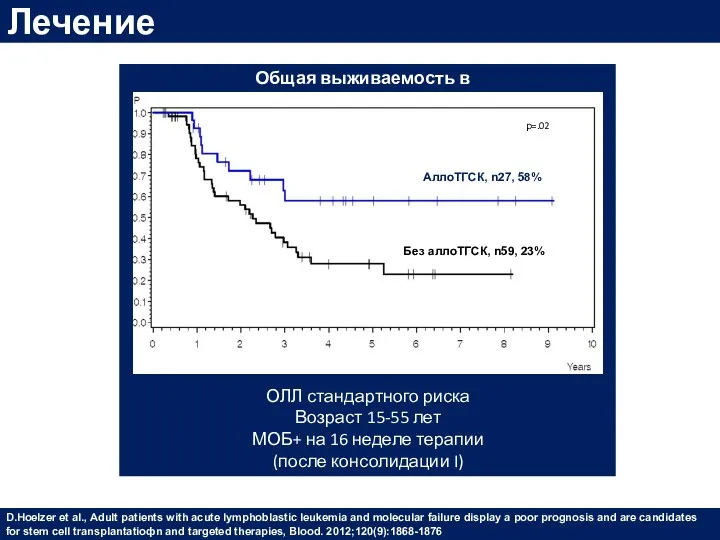
- 51. ОЛЛ стандартного риска Возраст 15-55 лет МОБ+ на 16 неделе терапии (после консолидации I) Без аллоТГСК,
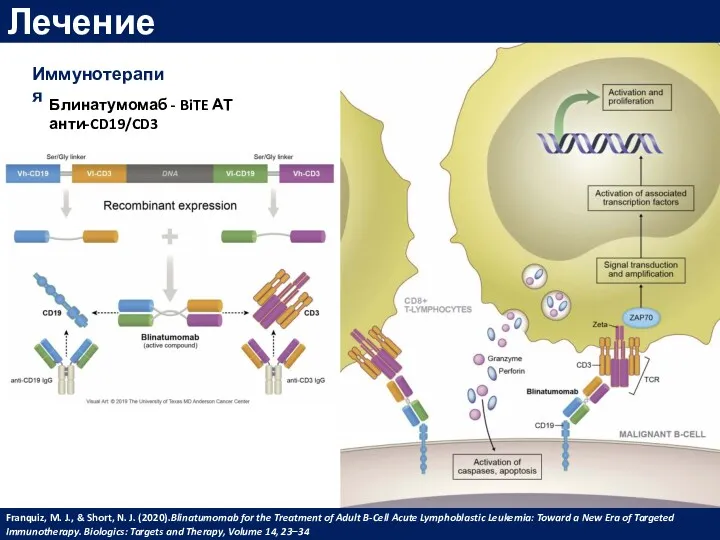
- 52. Лечение Иммунотерапия Блинатумомаб - BiTE АТ анти-CD19/CD3 Franquiz, M. J., & Short, N. J. (2020).Blinatumomab for
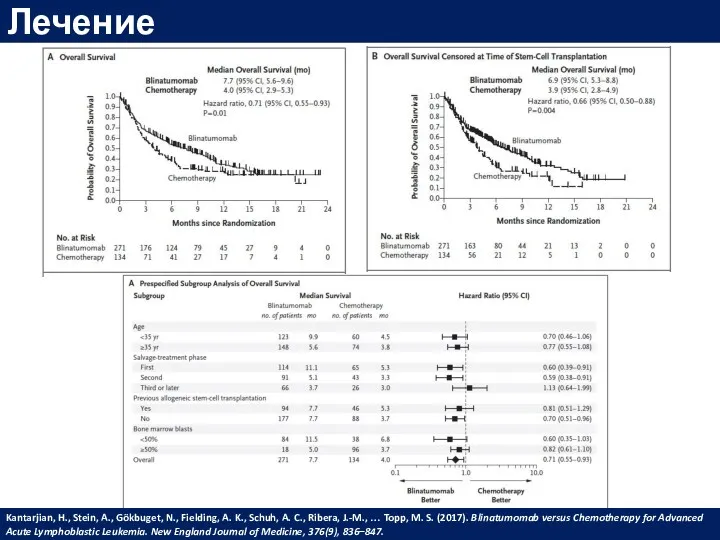
- 53. Лечение Kantarjian, H., Stein, A., Gökbuget, N., Fielding, A. K., Schuh, A. C., Ribera, J.-M., …
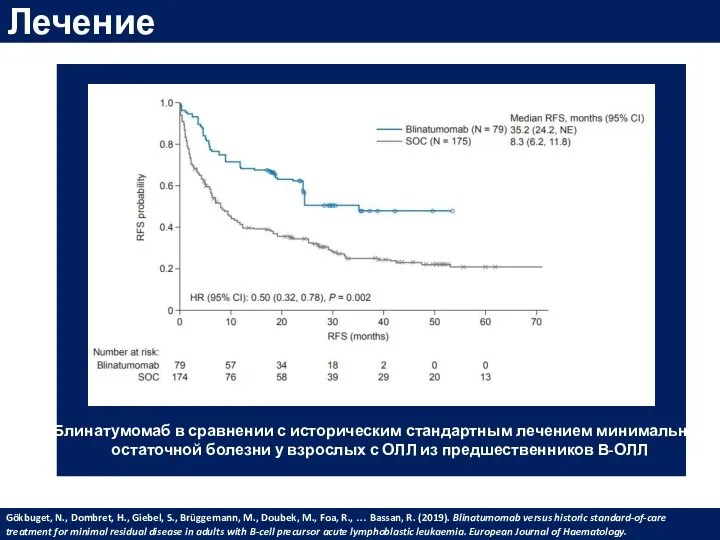
- 54. Лечение Блинатумомаб в сравнении с историческим стандартным лечением минимальной остаточной болезни у взрослых с ОЛЛ из
- 55. ОВ, 53% (95% CI 36-70%) БРВ, 38% (95% CI 21-55%) Общая и безрецидивная выживаемость пациентов ОЛЛ
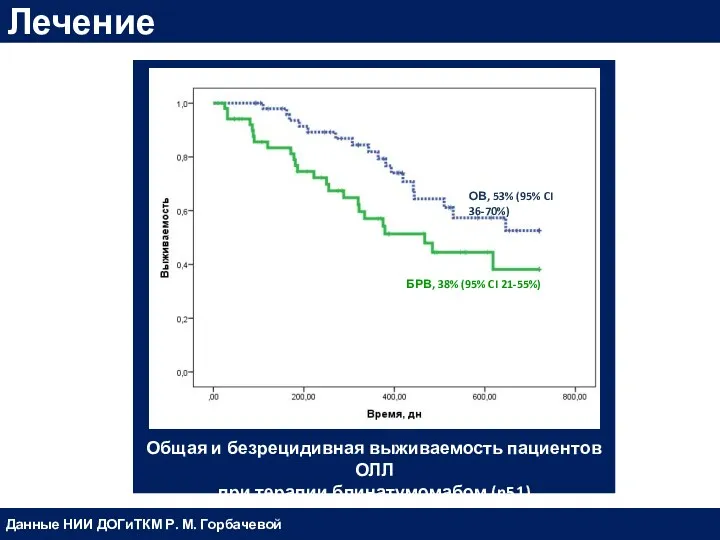
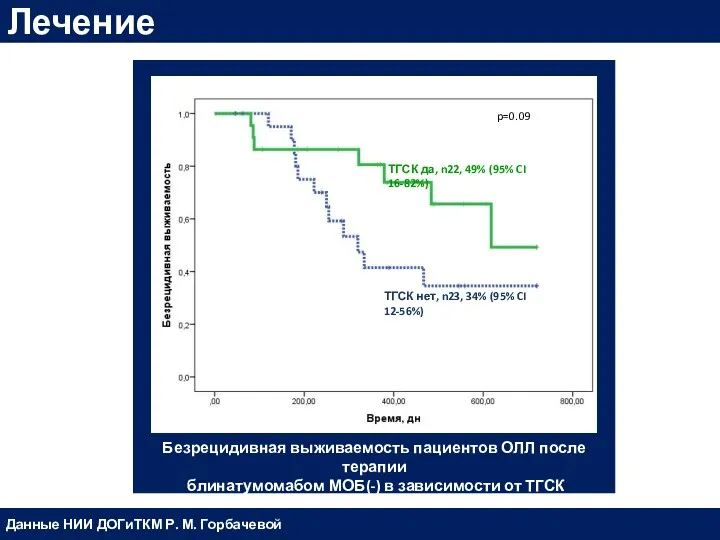
- 56. Безрецидивная выживаемость пациентов ОЛЛ после терапии блинатумомабом МОБ(-) в зависимости от ТГСК Лечение Данные НИИ ДОГиТКМ
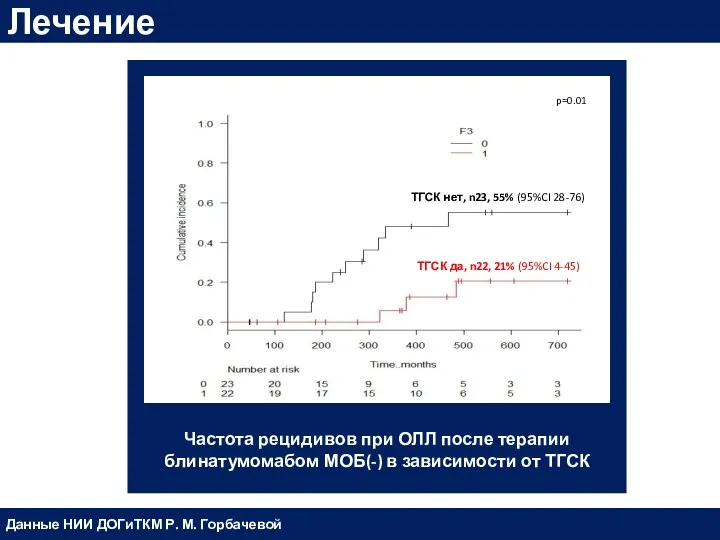
- 57. Частота рецидивов при ОЛЛ после терапии блинатумомабом МОБ(-) в зависимости от ТГСК Лечение Данные НИИ ДОГиТКМ
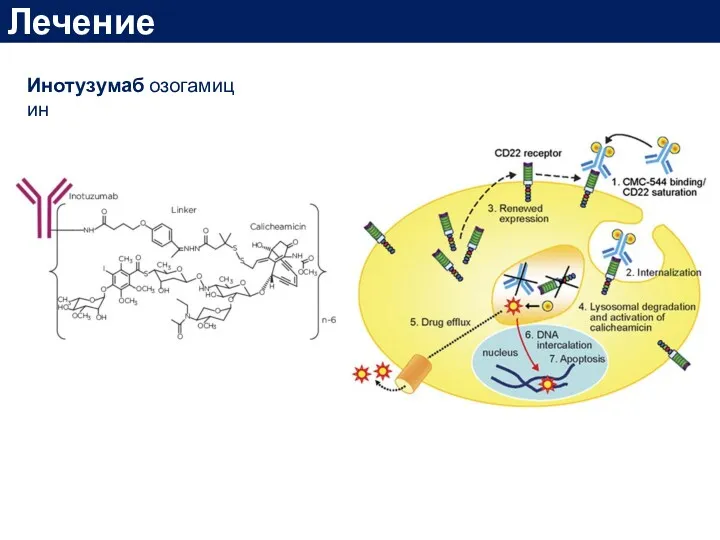
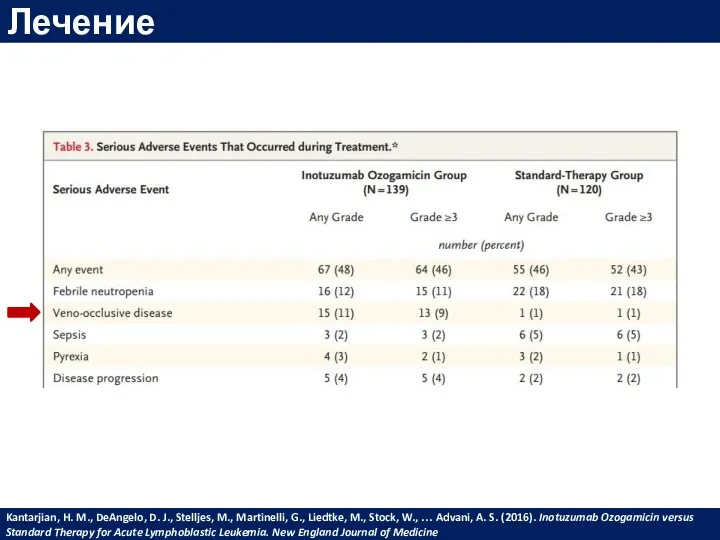
- 58. Лечение Инотузумаб озогамицин
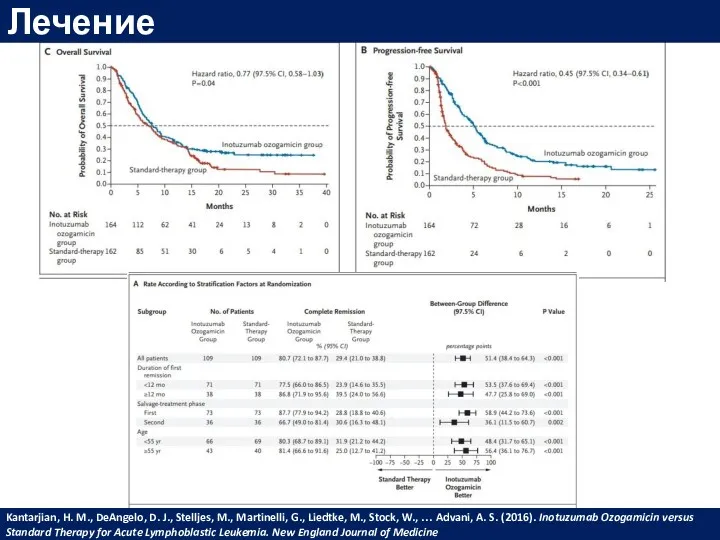
- 59. Лечение Kantarjian, H. M., DeAngelo, D. J., Stelljes, M., Martinelli, G., Liedtke, M., Stock, W., …
- 60. Лечение Kantarjian, H. M., DeAngelo, D. J., Stelljes, M., Martinelli, G., Liedtke, M., Stock, W., …
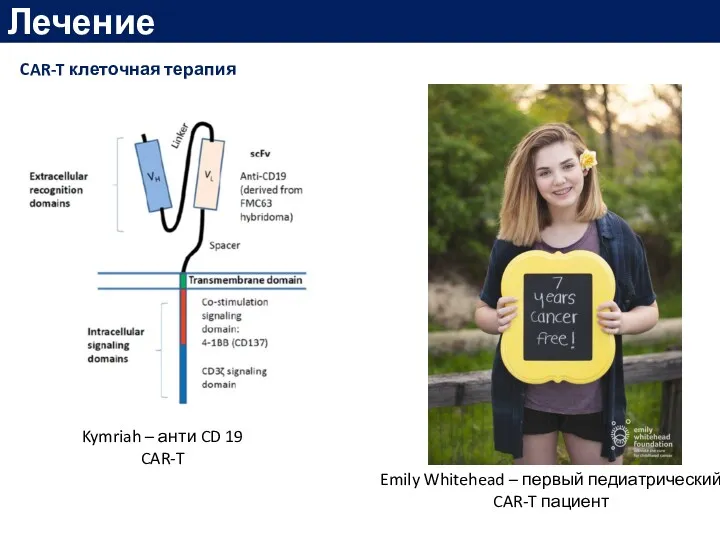
- 61. Лечение CAR-T клеточная терапия Kymriah – анти CD 19 CAR-T Emily Whitehead – первый педиатрический CAR-T
- 62. Лечение CAR-T клеточная терапия
- 63. Лечение «На данный момент мы находимся на стадии обсуждения плана, как внедрить эту технологию наиболее эффективно»,
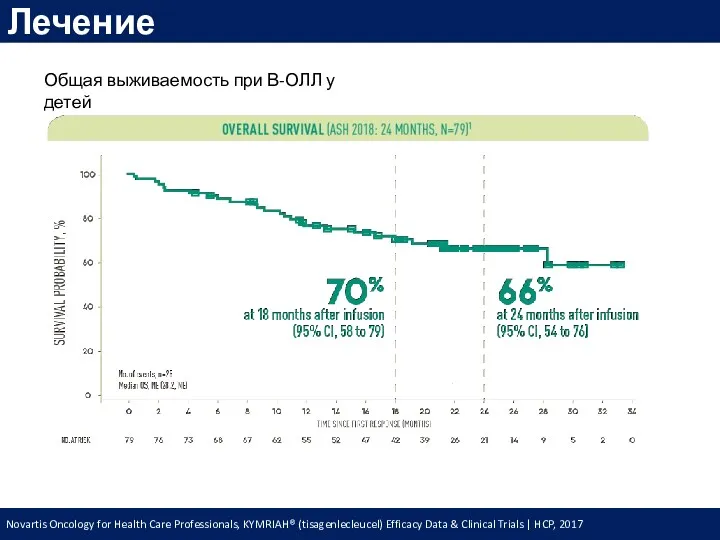
- 64. Лечение Novartis Oncology for Health Care Professionals, KYMRIAH® (tisagenlecleucel) Efficacy Data & Clinical Trials | HCP,
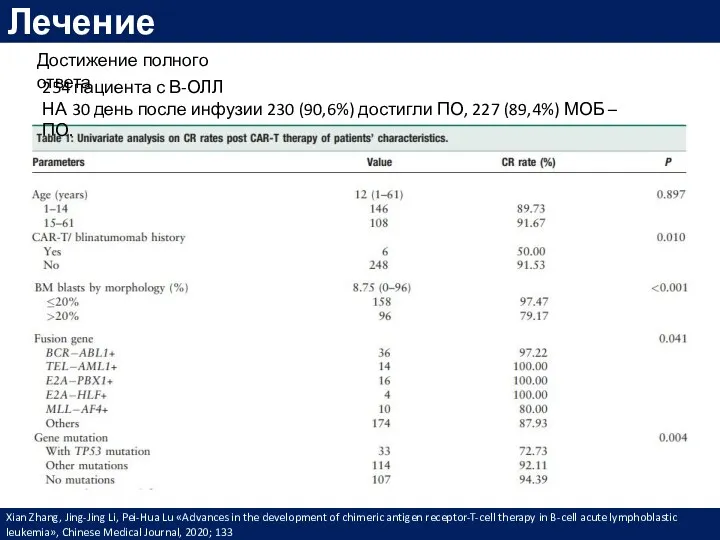
- 65. Лечение Xian Zhang, Jing-Jing Li, Pei-Hua Lu «Advances in the development of chimeric antigen receptor-T-cell therapy
- 66. Лечение Побочные эффекты : • Синдром выброса цитокинов • Нейротоксичность • В-клеточная аплазия Xian Zhang, Jing-Jing
- 67. Проблема : высокодозная химиотерапия повреждает лимфоциты пациента, снижая качество произведенных CAR-T Решение : использование «универсальных» клеток
- 68. Лечение CAR T – анти CD 19 (CD 52-, TCR αβ-) + Использование Алемтузумаба (анти CD
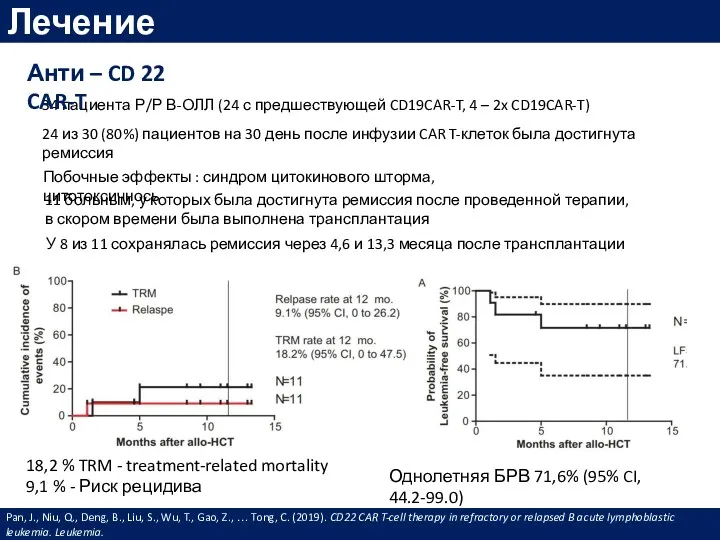
- 69. Лечение 34 пациента Р/Р В-ОЛЛ (24 с предшествующей CD19CAR-T, 4 – 2x CD19CAR-T) Анти – CD
- 71. Скачать презентацию























 Акушерские кровотечения при беременности
Акушерские кровотечения при беременности Тағамнан улану
Тағамнан улану Общие правила оказания первой медицинской помощи
Общие правила оказания первой медицинской помощи Неврологические проявления острых порфирий
Неврологические проявления острых порфирий PBSerum. Инновации в космецевтике
PBSerum. Инновации в космецевтике Клинический случай острого респираторного заболевания у ребенка с некетотической гиперглицинемией
Клинический случай острого респираторного заболевания у ребенка с некетотической гиперглицинемией Общие вопросы инфекционных болезней
Общие вопросы инфекционных болезней Гигиеническое обеспечение занятий физической культурой и спортом. Утомление
Гигиеническое обеспечение занятий физической культурой и спортом. Утомление Тактика врача при трещинах заднего прохода
Тактика врача при трещинах заднего прохода Врождённая глаукома
Врождённая глаукома Гастрит, асқазан ойық жарасы
Гастрит, асқазан ойық жарасы Поражение холодом: переохлаждение, холодовая травма
Поражение холодом: переохлаждение, холодовая травма Дезинфицирующие средства
Дезинфицирующие средства Сердечно-сосудистая недостаточность
Сердечно-сосудистая недостаточность Травматизм органа зрения
Травматизм органа зрения Все виды шрамов. Можно ли избавиться от шрамов и как
Все виды шрамов. Можно ли избавиться от шрамов и как Мозговые оболочки. Церебро-спинальная жидкость и ее циркуляция. Ликвор. Люмбальная пункция
Мозговые оболочки. Церебро-спинальная жидкость и ее циркуляция. Ликвор. Люмбальная пункция Судебно-медицинская экспертиза повреждений острыми предметами
Судебно-медицинская экспертиза повреждений острыми предметами Симптоматическая артериальная гипертензия
Симптоматическая артериальная гипертензия Первая медицинская помощь при ДТП
Первая медицинская помощь при ДТП Септическая коагулопатия
Септическая коагулопатия Eating well and feeling good
Eating well and feeling good Ребенок с низкой массой тела. Уход направленный на развитие
Ребенок с низкой массой тела. Уход направленный на развитие Доброкачественная гиперплазия предстательной железы
Доброкачественная гиперплазия предстательной железы Ультрозвуковая диагностика мочекаменной болезни
Ультрозвуковая диагностика мочекаменной болезни Использование средств физической культуры оздоровительной направленности для коррекции синдрома хронической усталости
Использование средств физической культуры оздоровительной направленности для коррекции синдрома хронической усталости Лекарственные средства, влияющие на гемостаз
Лекарственные средства, влияющие на гемостаз Диагностика хирургических заболеваний и повреждений грудной клетки и органов грудной полости
Диагностика хирургических заболеваний и повреждений грудной клетки и органов грудной полости