Слайд 2

Слайд 3
Актуальность
Сахарный диабет 2 типа (СД) является одной из самых актуальных проблем современной медицины.
Медико-социальная значимость СД 2 типа определяется несколькими факторами, одним из которых является высокая распространенность заболевания во всем мире. Среди всех форм диабета на долю СД 2 типа приходится 85-90%. По данным экспертов ВОЗ в 2010 г. согласно прогнозам на нашей планете будут жить около 215 млн. человек, страдающих этим заболеванием. Обращает на себя внимание тот факт, что истинная распространенность СД 2 типа в 2-3 раза превышает регистрируемую по обращаемости.
Диабет 2 типа являясь прогрессирующим заболеванием, которое часто требует от пациента использования нескольких гипогликемических препаратов для достижения гликемического контроля с прогрессированием заболевания. Что является большой проблемой для больных диабетом, так как пациенты забывают, отказываются от регулярного приема лекарств или принимают их нерегулярно, что в конечном итоге ухудшает состояние и приводит к быстрому развитию осложнений сахарного диабета.

Слайд 4
Цель:
Оценить эффективность применения ингибитора дипептидилпептидазы-4 у пациентов с сахарным диабетом 2 типа для
гликемического контроля ,предотвращения развития осложнений и улучшения качества жизни .

Слайд 5
Задачи
Произвести литературный обзор
Определение групп пациентов генеральной совокупности для формирования выборки
Путем рандомизации разделить пациентов
на 2 группы: 1 группа получающие ингибиторы депептидилпептидазы-4 и 2 группа получающая бигуаниды.

Слайд 6
Дизайн
РКИ
Выборка.
Систематическая выборка.
Генеральная совокупность все пациенты с сахарным диабетом 2 типа в ГП
№4,ГП№5,ГП№1,
КСМ в г.Актобе. Всего 1000 больных СД 2 типа.
Для исследования необходимо 100 пациентов. Предварительно пронумеровав всех пациентов от 1-1000.(1000/100=10, будет выбирать каждый 10 элемент. Для начала отобрав первый элемент с помощью генератора случайных чисел).

Слайд 7
Получив 100 пациентов с сахарным диабетом 2 типа, делим их на группы по
50 человек 1:1.В каждой группе делим пациентов на подгруппы, соответственно стадии и течения заболевания.
1 группа: получала ингибиторы депептидилпептидазы-4(ситаглиптин)
2 группа: получала бигуаниды(метформин)

Слайд 8
Критерии включения
Больные с установленным диагнозом сахарный диабетом 2 типа в стадии компенсации и
субкомпенсации.
Возраст 35-55 лет
Уровень глюкозы натощак 7 и более ммоль/л
Уровень гликированного гемоглобина 6,5% и более.
Длительность заболевания не менее 1 года.

Слайд 9
Критерии исключения
Больные с сахарным диабетом 1 типа
Возраст менее 35 лет и старше 55
лет
Беременные и кормящие
Тяжелое течение заболевания
Пациенты у которых в анамнезе: кетоацидоз, инсульт, инфаркт, онкологические заболевания.
Др. эндокринные заболевания

Слайд 10
Этические аспекты
Одобрено ЭК
Информированное согласие с полным раскрытием всей необходимой информацией (на понятном языке,
согласие написано на 2 языках: казахском и русском), крупный шрифт
Имеют право отказаться на любом этапе исследования, без неблагоприятных последствий
Получение необходимой медицинской помощи
Участие строго добровольное и бесплатное
Действие в интересах пациента
Польза и безопасность для пациента и общества

Слайд 11
Исследовательский вопрос
Приводит ли к снижению уровня глюкозы и гликированного гемоглобина применение ингибитора дипептидилпептидазы-4
ситаглиптина по сравнению с препаратами из группы бигуанидов метформина у пациентов с сахарным диабетом 2 типа в стадии компенсации и субкомпенсации?

Слайд 12
PICO
P -Пациенты с сахарным диабетом 2 типа в стадии компенсации и субкомпенсации
I -ситаглиптин
C
–Метформин
O –Снижение уровеня глюкозы и гликированного гемоглобина

Слайд 13
A randomized, placebo- and sitagliptin-controlled trial of the safety and efficacy of omarigliptin,
a once-weekly dipeptidyl peptidase-4 inhibitor, in Japanese patients with type 2 diabetes.
Gantz I1, Okamoto T2, Ito Y2, Okuyama K2, O'Neill EA1, Kaufman KD1, Engel SS1, Lai E1; the Omarigliptin Study 020 Group.
Abstract
AIMS:
To assess the safety and efficacy of omarigliptin in Japanese patients with type 2 diabetes (T2D).
METHODS:
In a 24-week double-blind trial, 414 patients with T2D were randomized to omarigliptin 25 mg once weekly, sitagliptin 50 mg once daily or placebo. The double-blind period was followed by a 28-week open-label extension during which all patients received omarigliptin 25 mg once weekly. Efficacy endpoints were glycated haemoglobin (HbA1c), 2-hour postprandial glucose (PPG) and fasting plasma glucose (FPG) levels.
RESULTS:
After 24 weeks, the least squares (LS) mean change from baseline in HbA1c was -0.66% for omarigliptin, -0.65% for sitagliptin and 0.13% for placebo. The difference in LS mean for omarigliptin vs placebo was -0.80% ( P < .001). The difference in LS mean for omarigliptin vs sitagliptin was -0.02% (95% confidence interval -0.15, 0.12), which met the criterion for non-inferiority to sitagliptin. Both active treatments provided significant reductions in FPG and 2-hour PPG compared with placebo (P < .001). Over the 24-week double-blind period, there were no clinically meaningful differences in the incidence rates of adverse events among the treatment groups. There was 1 episode of symptomatic hypoglycaemia in the sitagliptin group and none in the omarigliptin or placebo groups. In the 28-week open-label period, omarigliptin provided persistent improvements in glycaemic control without notable change in safety profile compared with the double-blind period. Omarigliptin had no meaningful effect on body weight.
CONCLUSIONS:
In Japanese patients with T2D, omarigliptin 25 mg once weekly provided significant glucose-lowering compared with placebo and was non-inferior to sitagliptin 50 mg once daily. Omarigliptin was generally well tolerated for up to 52 weeks.
TRIAL REGISTRATION:
ClinicalTrials.gov NCT01703221.

Слайд 14
Исследовательский вопрос по статье
Приводит ли к снижению уровня глюкозы и гликированного гемоглобина применение
омариглиптина по сравнению с плацебо или ситаглиптином у пациентов с сахарным диабетом 2 типа?

Слайд 15
PICO
P- Пациенты с сахарным диабетом 2 типа
I- омариглиптин
C- плацебо или ситаглиптин
O- снижение уровня
глюкозы и гликированного гемоглобина

Слайд 16
Дизайн исследования по статье
Исследование представляет собой рандомизированное, плацебо- и ситаглиптин-контролируемое параллельное групповое многоцентровое
двойное слепое исследование омариглиптина 25 мг один раз в неделю с расширением открытой метки, при котором все пациенты получали омариглиптин 25 мг один раз в неделю (рисунок S1). Исследование включало период скрининга до 2 недель, период вымывания 6 недель для пациентов на пероральном AHA, двухнедельный однократный период плацебо в режиме слепоты и 24-недельный двойной слепой период лечения за которым следует 28-недельный период расширения открытой метки. При рандомизации пациенты стратифицировали в соответствии с их использованием перорального AHA при скрининге. Пациенты были рандомизированы с использованием двойного манекена в соотношении 2: 2: 1: омариглиптин 25 мг один раз в неделю / плацебо, сопоставляющий ситаглиптин 50 мг один раз в день; ситаглиптин 50 мг один раз в день / плацебо, соответствующий омариглиптину 25 мг один раз в неделю; или плацебо, сопоставляющий омариглиптин 25 мг один раз в неделю / плацебо, сопоставляющий ситаглиптин 50 мг один раз в день. Sitagliptin 50 мг один раз в день был выбран в качестве соответствующей дозы для использования в исследовании, потому что это обычная начальная доза и наиболее широко используемая доза в Японии. Для рандомизации использовался интерактивный речевой ответ или интегрированная система веб-ответов. Пациенты, не отвечающие заранее заданным критериям гликемического контроля после рандомизации (с 4 по 24 неделю, FPG> 13,3 ммоль / л, после недели 24, FPG> 11,1 ммоль / л) были прекращены из исследования.

Слайд 17
Дизайн…
Тест на переносимость пищи проводился при рандомизации (1-й день), а также в неделях
24 и 52 (или при прекращении приема). Испытания на толерантность к еде должны проводиться в корыте через 7 дней после предыдущей дозы омариглиптина или плацебо, соответствующих омариглиптину, и до ежедневного ситаглиптина или плацебо, соответствующих дозе ситаглиптина. Стандартный прием пищи для теста на переносимость еды составлял ~ 500 ккал, с 75 г углеводов, 14 г жира и 17 г белка. Ожидается, что пациент закончит еду в течение 15 минут после начала еды. Образец крови для глюкозы собирали непосредственно перед употреблением в пищу и через 30, 60 и 120 минут с начала приема пищи.
Исследование (Omarigliptin Protocol 020; ClinicalTrials.gov : NCT01703221) проводилось в соответствии с принципами хорошей клинической практики и было одобрено соответствующими институциональными обзорными советами.

Слайд 18
Критерии включения по статье
Пациенты с СД 2 типа (мужчины и женщины)
Возраст 20 лет
Индекс
массы тела> 18 и <40 кг / м 2 .
На скрининговом визите пациенты, которые не получали лечение (никогда не были оральным антигипергликемическим агентом [AHA]) или не принимали лекарство от AHA в течение ≥6 недель и имели Национальную программу стандартизации Гликогемоглобина (NGSP) HbA1c ≥7,0% и ≤10,0%, были право на участие в исследовании; при монотерапии монотерапией AHA с использованием NGSP HbA1c ≥6,5% и ≤9,0%, а также после 6-недельного периода промывания AHA, NGSP HbA1c ≥7,0% и ≤10,0%, также были пригодны для исследования. На неделе -2 пациенты должны были иметь уровень HbA1c между ≥7,0% и ≤ 10,0% и уровнем FPG ≤12,8 ммоль / л.

Слайд 19
Критерии исключения по статье
Пациенты были исключены из исследования, если у них был диабет
типа 1, история кетоацидоза, активное заболевание печени, значительное сердечно-сосудистое заболевание, история злокачественных новообразований или гематологических расстройств или ранее были обработаны ситаглиптином или омариглиптином в любое время или с тиазолидиндионами или терапии инсулином в течение 12 недель до посещения скрининга.
Критерии лабораторного исключения включали оценочную скорость клубочковой фильтрации <50 мл / мин / 1,73 м 2 , аланинаминотрансферазу или аспартатаминотрансферазу> в 2 раза превышающую верхний предел нормальных, триглицеридов> 6,78 ммоль / л или тиреотропный гормон вне нормального диапазона центральной лаборатории.



















 Атеросклероз
Атеросклероз Иммунитет. Врожденный и приобретенный иммунитет
Иммунитет. Врожденный и приобретенный иммунитет Долголетие в добром здравии
Долголетие в добром здравии Инфекционно-токсический шок. Критические состояния и факторы риска их развития у инфекционных больных
Инфекционно-токсический шок. Критические состояния и факторы риска их развития у инфекционных больных Способы лечения варикозной болезни нижних конечностей
Способы лечения варикозной болезни нижних конечностей Воспалительные заболевания челюстно-лицевой области
Воспалительные заболевания челюстно-лицевой области Болезнь Гентингтона
Болезнь Гентингтона Диагностика туберкулеза
Диагностика туберкулеза Энтеровирусты инфекция
Энтеровирусты инфекция МРТ-диагностики патологии позвоночника
МРТ-диагностики патологии позвоночника Здоровый образ жизни
Здоровый образ жизни Профилактика хронических неинфекционных заболеваний. Школы здоровья
Профилактика хронических неинфекционных заболеваний. Школы здоровья Фонові та передракові захворювання жіночих статевих органів. Злоякісні новоутворення геніталій
Фонові та передракові захворювання жіночих статевих органів. Злоякісні новоутворення геніталій Что такое Здоровье?
Что такое Здоровье? Amphetamine Psychosis
Amphetamine Psychosis Гемоглобин. Соединения и виды гемоглобина. Практическая значимость их определения
Гемоглобин. Соединения и виды гемоглобина. Практическая значимость их определения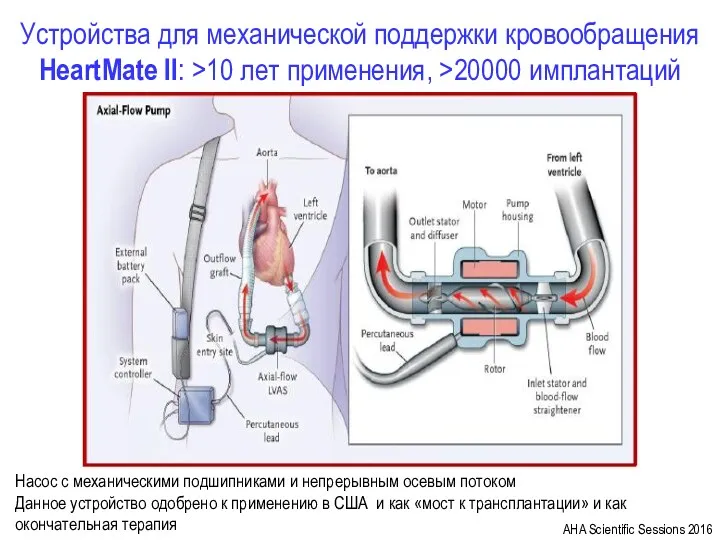 Устройства для механической поддержки кровообращения HeartMate II
Устройства для механической поддержки кровообращения HeartMate II Неврозы у детей и подростков
Неврозы у детей и подростков Лечебные диеты. Лечебно-профилактическое питание
Лечебные диеты. Лечебно-профилактическое питание ВКР: Анализ работы медсестры процедурного кабинета хирургического отделения стационара
ВКР: Анализ работы медсестры процедурного кабинета хирургического отделения стационара Вирусные гепатиты В, С, D
Вирусные гепатиты В, С, D Остеохондропатии
Остеохондропатии Анаэробная энтеротоксемия крупного рогатого скота
Анаэробная энтеротоксемия крупного рогатого скота Methods of examination in gynecology
Methods of examination in gynecology Що нового в діагностиці і лікуванні H. pylori
Що нового в діагностиці і лікуванні H. pylori Болезнь Альцгеймера
Болезнь Альцгеймера Сестринский процесс при эндокринных заболеваниях, при сахарном диабете
Сестринский процесс при эндокринных заболеваниях, при сахарном диабете Биохимия почек и мочи. (Лекция 10)
Биохимия почек и мочи. (Лекция 10)