Сәулелік терапия қатерлі ісіктері органдарының репродуктивті жүйесі принциптері. Брахитерапия және сәулелік терапиясы презентация
Содержание
- 2. Cәулелі терапия (СТ) Ауруларды емдеуде сәулелерді қолдану, негізінде қатерлі ісіктерді. Өзіндік СТ КОМБИНИРЛЕНГЕН СТ- комбинация хир.
- 3. Қатерлі ісіктерді емдеуге иондаушы сәулелерді 1895 жылы рентеген сәулелерін неміс ғалымы В.Рентген ашқаннан кейін және 1896
- 4. Сәулелі терапия принциптері Патологиялық ошақты оптималды дозаға әкелу Қоршаған органдары мен тіндерді минималды жарақаттау Организмнің қорғаныш
- 5. Сәлелі терапия РАДИКАЛЬДЫ - ауруды толық емдеу – біріншілік ошақта және мүмкін метастаздану зоналарындағы ісік клеткаларын
- 6. Иондық сәулелердің түрлері: Қатерлі ісіктерді сәулелеуге корпускулярлы (бета-частицы-β, нейтрондар – n, протондар – р, пи-минус-мезоны) және
- 7. Сәулелі терапияда келесідей радиоактивті изотоптар қолданылады: радиоактивті кобальт – 60Со, цезий – 137Cs, иридий – 192Ir,
- 8. а, б : заманауи ротационды терапевтикалық қондырғы TERAGAM (UJP PRAHA a.s.) в: Аппликатор жиынтығы к MicroSelectron-HDR
- 10. Радиочувствительность (или радиорезистентность) — выражает скорость и степень реакции опухоли в ходе лечения. Быстро размножающиеся клетки
- 11. Различают два вида гибели клеток вследствие облучения: митотическая гибель (инактивация клетки вслед за облучением после первого
- 12. Распределение злокачественных опухолей по степени радио-чувствительности: высокая: гематосаркомы (ходжинские и неходжинские лимфомы), эмбриональные опухоли (семиномы, дисгерминомы),
- 14. Показания к ЛТ опухолевых заболеваний Показанием к ЛТ является наличие гистологически верифицированнойзлокачественной опухоли (иногда возможна цитологическая
- 15. Противопоказания к ЛТ злокачественных опухолей Резкое ослабление сопротивляемости организма (раковая кахексия) Лучевая болезнь Тяжелые декомпенсированные заболевания
- 16. Основным принципом лучевой терапии является создание достаточной дозы в области опухоли для полного подавления ее роста
- 17. Сәулелі терапия әдістерінің классификациясы 1) Дистанционные методы облучения – это такие методы лучевой терапии, при которых
- 18. 2)Контактные методы – это такие методы лучевой терапии, когда источник излучения во время лечения находится в
- 19. Лучевая терапия может быть использована: 1. как самостоятельный или основной метод лечения; 2. в комбинации с
- 20. Лучевая терапия как компонент комбинированного лечения позволяет повысить эффективность хирургического вмешательства за счет снижения частоты развития
- 21. Операция алды сәулелену: снизить митотическую активность и жизнеспособность опухолевых клеток, уменьшая их имплантационную способность, что, в
- 22. Операциядан кейінгі сәулелік терапия снижение биологической потенции опухолевых клеток, возможно оставшихся в зоне операционного поля; обеспечение
- 23. Интраоперационды сәулелік терапия предусматривает однократное облучение опухоли перед ее удалением (предоперационный вариант), или для воздействия на
- 24. Приборлар Л и н е й н ы й у с к о р и т
- 25. Г а м м а- а п п а р а ты типа РОКУС для подвижных
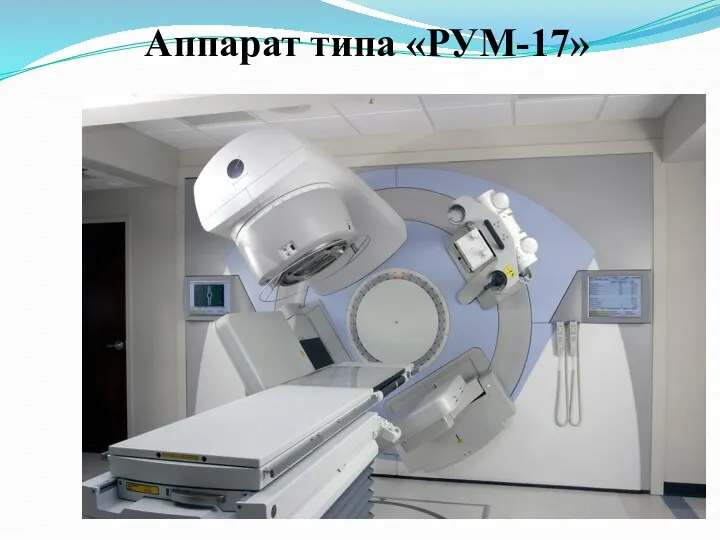
- 26. Аппарат типа «РУМ-17»
- 27. Аппарат типа «Рентген ТА-Д»
- 28. Гамма-терапевтические аппараты
- 29. Аппараты для контактной лучевой терапии.
- 30. Брахитерапия Органосохраняющим методом лечения локализованных форм рака предстательной железы, органов полости рта, ротоглотки, носоглотки, гортани, новообразований
- 31. Брахитерапия Брахитерапия (контактная лучевая терапия, кюри-терапия (уст.)) — вид радиотерапии, когда источник излучения (Ra-226, Ir-192, I-125,
- 32. К о н т а к т н ы е методы облучения- брахитерапия А п п
- 33. В н у т р и т к а н е в о й метод -
- 34. Установки брахитерапии (внутриполостной терапии) общего назначения (с извлечением источников после облучения) выпускает целый ряд фирм, наиболее
- 35. Основные применения брахитерапии: Внутриполостная брахитерапия с размещением радиоактивных источников в аппликаторах установленных в полостях, т.е. в
- 36. Брахитерапия – микроисточники I-125 ДЛИТЕЛЬНОСТЬ ГОСПИТАЛИЗАЦИИ – 1 СУТКИ ПЕРИОД РЕАБИЛИТАЦИИ – 3-4 ДНЯ ЭФФЕКТИВНОСТЬ РАВНА
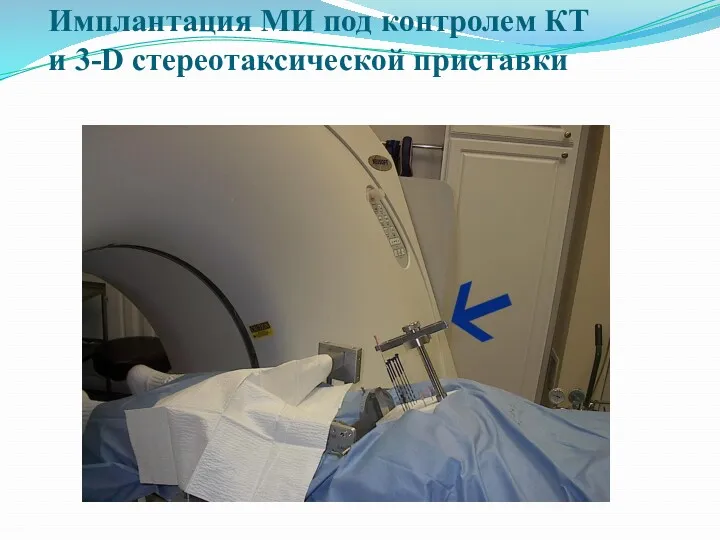
- 37. Имплантация МИ под контролем КТ и 3-D стереотаксической приставки
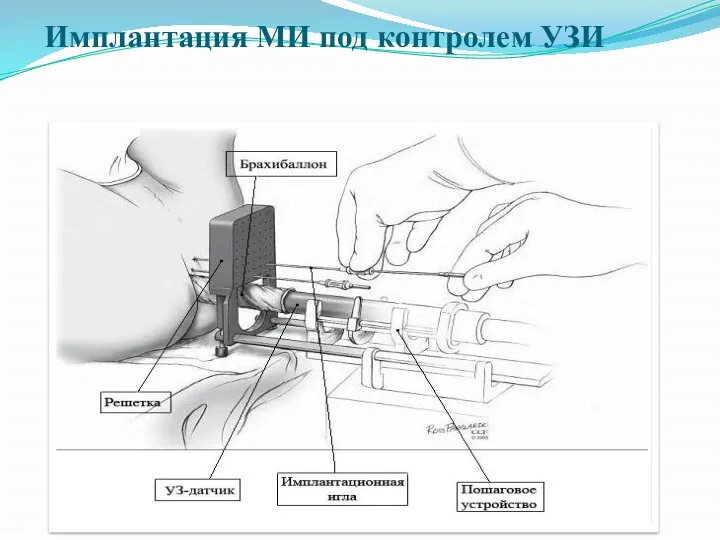
- 38. Имплантация МИ под контролем УЗИ
- 39. Микроисточники с йодом-125 Герметичная титановая капсула с изотопом йода-125 Испускает мягкое рентгеновское излучение Видны на УЗИ
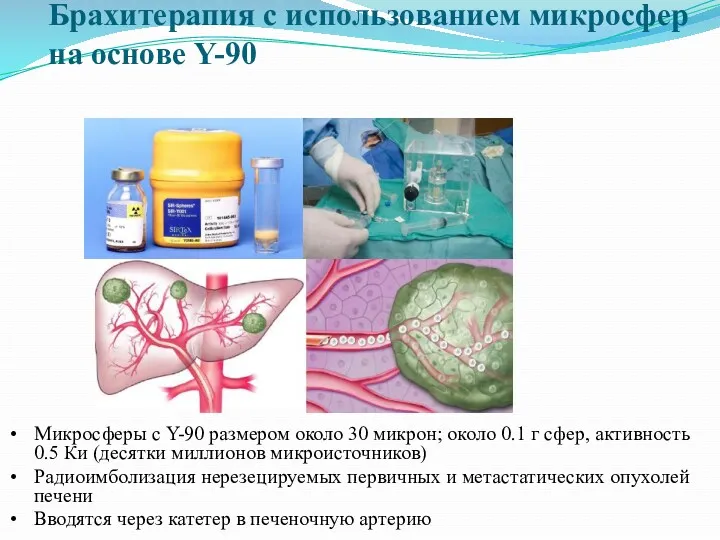
- 40. Брахитерапия с использованием микросфер на основе Y-90 Микросферы с Y-90 размером около 30 микрон; около 0.1
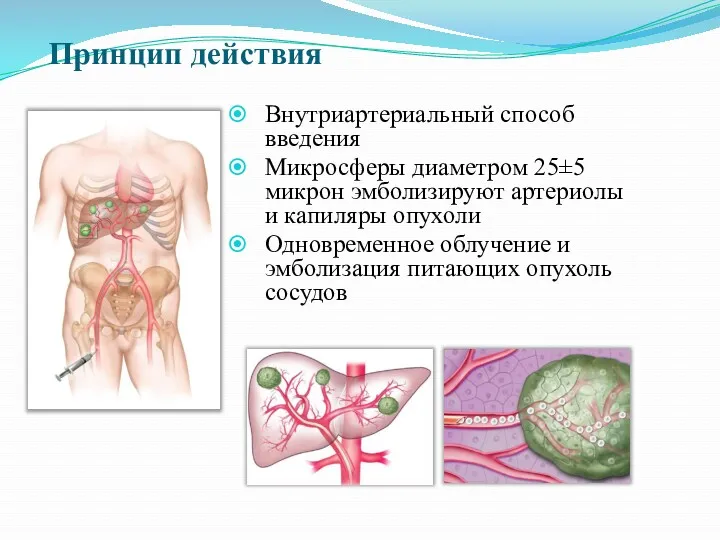
- 41. Принцип действия Внутриартериальный способ введения Микросферы диаметром 25±5 микрон эмболизируют артериолы и капиляры опухоли Одновременное облучение
- 42. Достоинства и проблемы Достоинства Малоинвазивный процесс введения Минимальные повреждения здоровой ткани Поражение сразу всех очагов и
- 43. Микросферы на основе радионуклида иттрия-90 Микросферы под микроскопом Микросферы упакованные в виалу
- 45. Скачать презентацию





































 Патология внешнего дыхания
Патология внешнего дыхания Дифференциальная диагностика инфекционных заболеваний с респираторным синдромом
Дифференциальная диагностика инфекционных заболеваний с респираторным синдромом Электронная поликлиника – новые возможности медицины
Электронная поликлиника – новые возможности медицины Рак предстательной железы
Рак предстательной железы Вибрационная болезнь (2)
Вибрационная болезнь (2) Операции на сосудах. Сосудистый шов, виды, инструменты для операций на сосудах
Операции на сосудах. Сосудистый шов, виды, инструменты для операций на сосудах Фармакология. Применение лекарственных растений, обладающих вяжущим действием, в медицинской практике
Фармакология. Применение лекарственных растений, обладающих вяжущим действием, в медицинской практике Методы определения центрального соотношения челюстей в стоматологии
Методы определения центрального соотношения челюстей в стоматологии Функциональная магнитно-резонансная томография
Функциональная магнитно-резонансная томография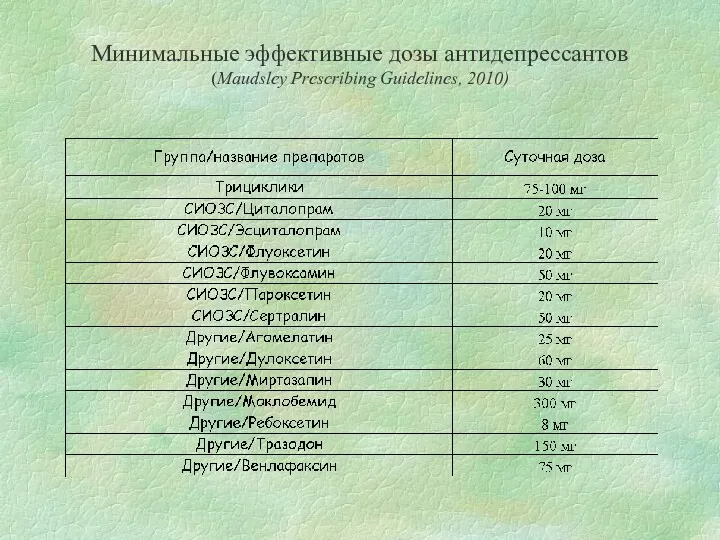 Минимальные эффективные дозы антидепрессантов (Maudsley Prescribing Guidelines, 2010)
Минимальные эффективные дозы антидепрессантов (Maudsley Prescribing Guidelines, 2010) Подари улыбку. Здоровое долголетие - образовательно-оздоровительная программа для пожилых
Подари улыбку. Здоровое долголетие - образовательно-оздоровительная программа для пожилых Роль и значение анестезиологии, реанимации и интенсивной терапии в современной медицине
Роль и значение анестезиологии, реанимации и интенсивной терапии в современной медицине Лечение нейросенсорной тугоухости
Лечение нейросенсорной тугоухости Жүйке жүйесі
Жүйке жүйесі Острая сердечная недостаточность
Острая сердечная недостаточность Поражение мозжечка
Поражение мозжечка Несахарный диабет
Несахарный диабет Туберкулез кожи
Туберкулез кожи Поведенческие расстройства, связанные с физиологическими нарушениями
Поведенческие расстройства, связанные с физиологическими нарушениями Хроническая ишемия мозга. Транзиторная ишемическая атака
Хроническая ишемия мозга. Транзиторная ишемическая атака БДТ мен ЖК жүргізілетін сабақтың балалар мен жасөспірімдердің ағзасының функционалдық жағдайына әсері
БДТ мен ЖК жүргізілетін сабақтың балалар мен жасөспірімдердің ағзасының функционалдық жағдайына әсері Лечебное питание при различных нарушениях обмена веществ
Лечебное питание при различных нарушениях обмена веществ Организация деятельности медицинской сестры перевязочного кабинета
Организация деятельности медицинской сестры перевязочного кабинета Аневризма грудного отдела аорты
Аневризма грудного отдела аорты Неврозы. Классификация. Этиология. Профилактика
Неврозы. Классификация. Этиология. Профилактика Слуховой анализатор
Слуховой анализатор Дифференциальная диагностика геморрагических высыпаний при системных васкулитах сосудов мелкого и среднего калибра
Дифференциальная диагностика геморрагических высыпаний при системных васкулитах сосудов мелкого и среднего калибра Дифтерия. Вакцинопрофилактика
Дифтерия. Вакцинопрофилактика