Содержание
- 2. Вода Рис.1 Химическая формула воды
- 3. Состояния воды Рис.2 Газообразное состояние воды ( пар). Рис.3 Жидкое состояние воды. Рис.4 Твёрдое состояние воды
- 4. Аномальные свойства воды Аномальные свойства воды — это свойства воды, которые выпадают из общих закономерностей и
- 5. Формы материи Все вещества существуют в трех различных состояниях, которые зависят от температуры и давления. Твердые
- 6. Точки кипения и замерзания Рис.9 Температуры кипения и замерзания соединений водорода Аномальными свойствами воды являются ее
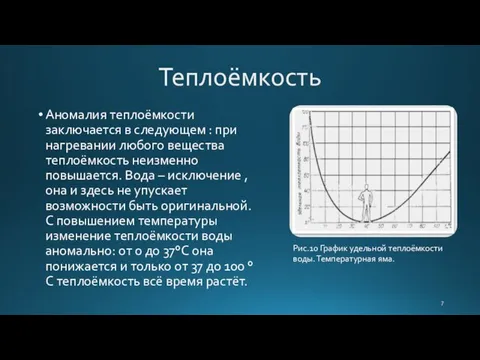
- 7. Теплоёмкость Аномалия теплоёмкости заключается в следующем : при нагревании любого вещества теплоёмкость неизменно повышается. Вода –
- 8. Эффект Мпембы Удивительно, но факт – горячая вода замерзает быстрее холодной, что противоречит логике и общему
- 9. Поверхностное натяжение воды Известно, что если стальную иголку осторожно положить на поверхность воды, налитой в блюдце
- 10. Аномалия плотности При охлаждении вода сначала ведет себя как и другие жидкости: постепенно уплотняясь, уменьшает свой
- 11. Вода —растворитель В воде растворяется больше веществ, чем в любом другом растворителе. В ней можно найти
- 13. Скачать презентацию









 Институт социально-гуманитарных технологий и коммуникаций. Программы обучения
Институт социально-гуманитарных технологий и коммуникаций. Программы обучения Телевидение и видеозапись. Обработка видео
Телевидение и видеозапись. Обработка видео Графы
Графы В Мире животных и насекомых. Фото: бабочки, животные
В Мире животных и насекомых. Фото: бабочки, животные Адміністративне право. Курс лекцій
Адміністративне право. Курс лекцій Использование технических средств обучения в учебно-воспитательной работес дошкольниками
Использование технических средств обучения в учебно-воспитательной работес дошкольниками  Взаимосвязь биологических и социальных факторов в психическом развитии
Взаимосвязь биологических и социальных факторов в психическом развитии Презентация Вредно ли сладкое для зубов?
Презентация Вредно ли сладкое для зубов? Отработка порядка приема Военной присяги
Отработка порядка приема Военной присяги Крестьянская реформа 1861 года
Крестьянская реформа 1861 года Говорит она беззвучно,а понятно и не скучно.Ты беседуй чаще с ней – станешь вчетверо умней.
Говорит она беззвучно,а понятно и не скучно.Ты беседуй чаще с ней – станешь вчетверо умней. Агит-дизайн в СССР. Этапы развития агит-дизайна
Агит-дизайн в СССР. Этапы развития агит-дизайна Прямая. Луч. Отрезок
Прямая. Луч. Отрезок 20230821_prezentatsiya_po_teme_deystvitelnye_prichastiya_proshedshego_vremeni_7_klass
20230821_prezentatsiya_po_teme_deystvitelnye_prichastiya_proshedshego_vremeni_7_klass Презентация на педагогический совет Роль книжной иллюстрации в речевом развитии ребенка-дошкольника
Презентация на педагогический совет Роль книжной иллюстрации в речевом развитии ребенка-дошкольника Средняя линия треугольника
Средняя линия треугольника Делинквентное поведение у детей и подростков
Делинквентное поведение у детей и подростков Размещение и расчет водопропускных сооружений
Размещение и расчет водопропускных сооружений Фантазии с листом бумаги
Фантазии с листом бумаги Презентация профессионального опыта
Презентация профессионального опыта Поняття птахи
Поняття птахи Паломнический туризм в России
Паломнический туризм в России Задачи по управленческому учету
Задачи по управленческому учету Архитектура информационной системы
Архитектура информационной системы М.Гоголь. Ревізор. Образи чиновників
М.Гоголь. Ревізор. Образи чиновників родительское собрание: Как развить ответственность в наших детях
родительское собрание: Как развить ответственность в наших детях Презентация: Специфика обучения и воспитания детей в логопедической группе. Роль семьи в преодолении дефектов речи
Презентация: Специфика обучения и воспитания детей в логопедической группе. Роль семьи в преодолении дефектов речи Кем быть, каким быть?
Кем быть, каким быть?