Слайд 2

Решим задачу
Определите формулу углеводорода, плотность паров которого по водороду равна 2,69.
Массовая доля углерода в веществе составляет 92,3%
Слайд 3

Майкл Фарадей (1791 - 1867)
Английский физик и химик, член Лондонского
королевского общества. В 1823 г. впервые получил жидкие хлор, сероводород, оксид углерода(IV), аммиак, оксид азота(IV). В 1825 г. открыл бензол, изучил его физические и некоторые химические свойства. Положил начало исследованиям каучука. В 1833 - 1836 гг. установил количественные законы электролиза.
Слайд 4

Фридрих Август Кекуле
1829 - 1896
Немецкий химик-органик. Предложил структурную формулу молекулы бензола.
С целью проверки гипотезы о равноценности всех шести атомов водорода в молекуле бензола получил его галоген-, нитро-, амино-, и карбоксипроизводные.
Слайд 5
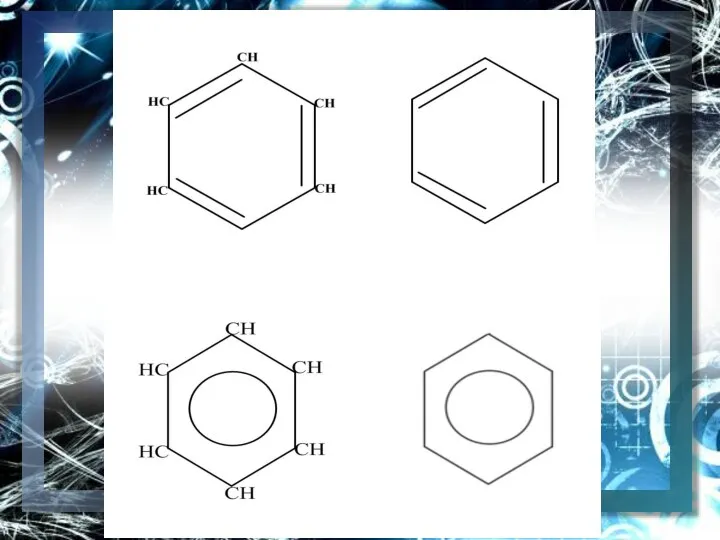
Слайд 6
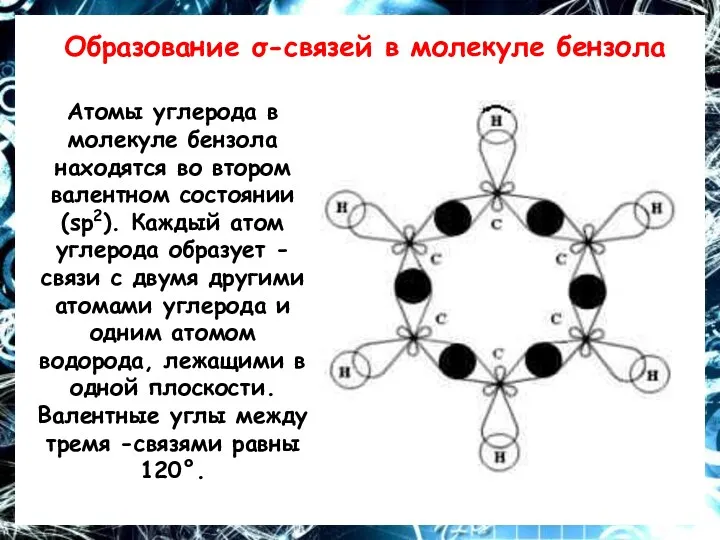
Образование σ-связей в молекуле бензола
Атомы углерода в молекуле бензола находятся во
втором валентном состоянии (sp2). Каждый атом углерода образует -связи с двумя другими атомами углерода и одним атомом водорода, лежащими в одной плоскости. Валентные углы между тремя -связями равны 120°.
Слайд 7
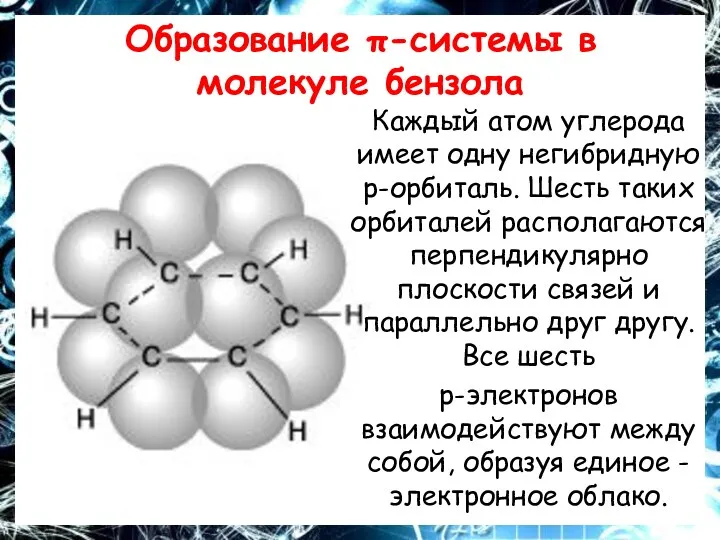
Образование π-системы в молекуле бензола
Каждый атом углерода имеет одну негибридную
р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскости связей и параллельно друг другу. Все шесть
р-электронов взаимодействуют между собой, образуя единое -электронное облако.
Слайд 8
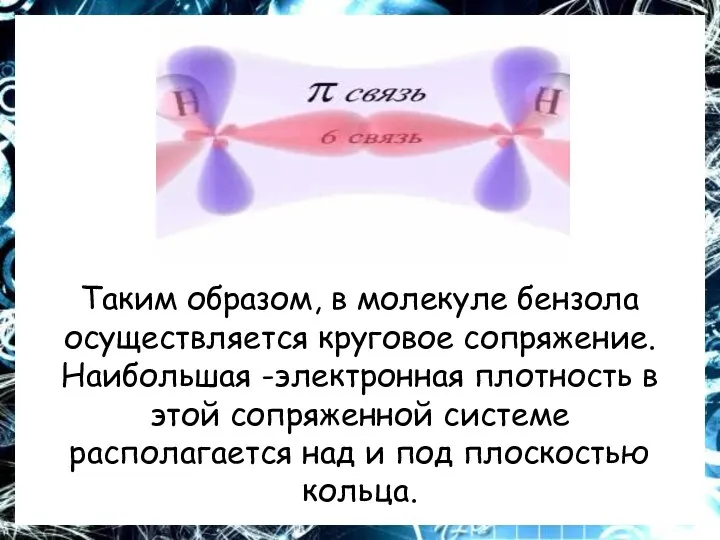
Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая -электронная плотность
в этой сопряженной системе располагается над и под плоскостью кольца.
Слайд 9
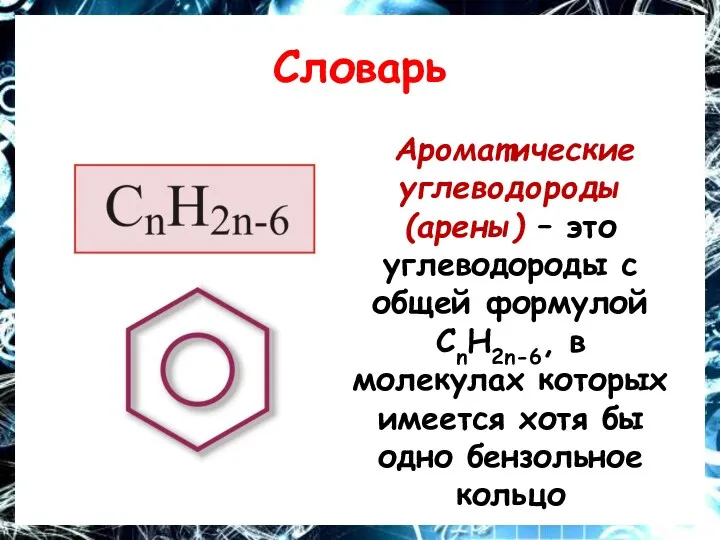
Словарь
Ароматические углеводороды (арены) – это углеводороды с общей формулой СnH2n-6,
в молекулах которых имеется хотя бы одно бензольное кольцо
Слайд 10
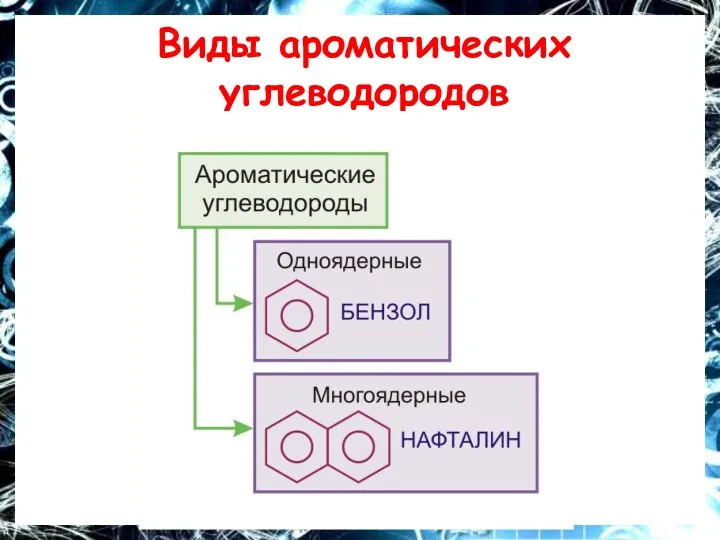
Виды ароматических углеводородов
Слайд 11
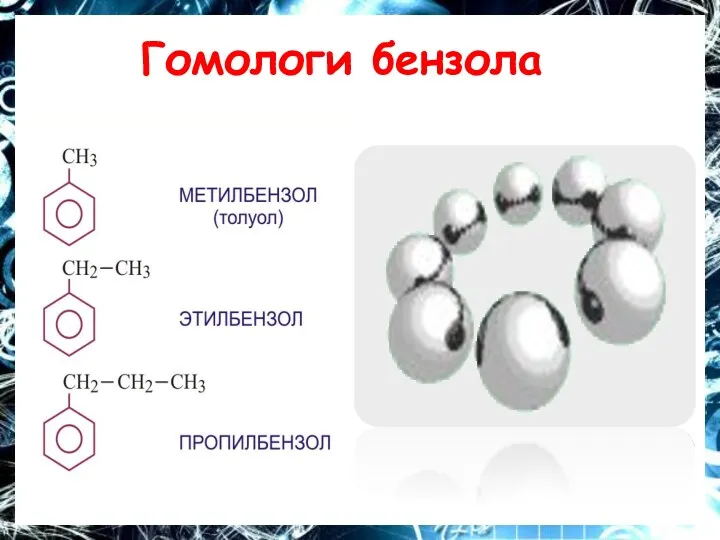
Слайд 12
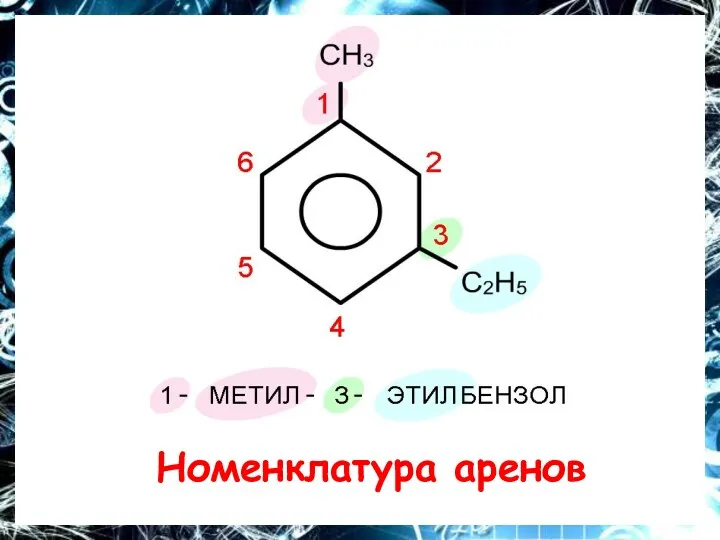
Слайд 13

Физические свойства
Бензол – бесцветная, летучая, огнеопасная жидкость с неприятным запахом. Он
легче воды ( =0,88 г/см3) и с ней не смешивается, но растворим в органических растворителях, и сам хорошо растворяет многие вещества. Бензол кипит при 80,1 С, при охлаждении легко застывает в белую кристаллическую массу. Бензол и его пары ядовиты. Систематическое вдыхание его паров вызывает анемию и лейкемию.
Слайд 14
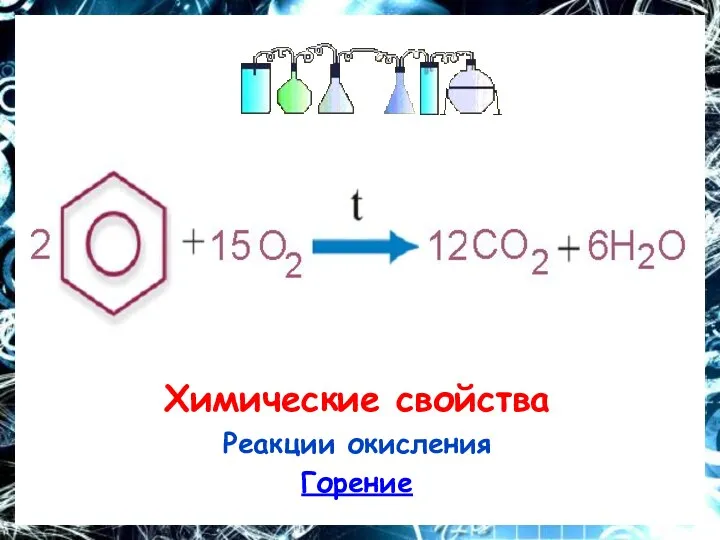
Химические свойства
Реакции окисления
Горение
Слайд 15

Химические свойства
Реакции окисления
Мягкое окисление
Бензол не обесцвечивает раствор перманганата калия
Слайд 16
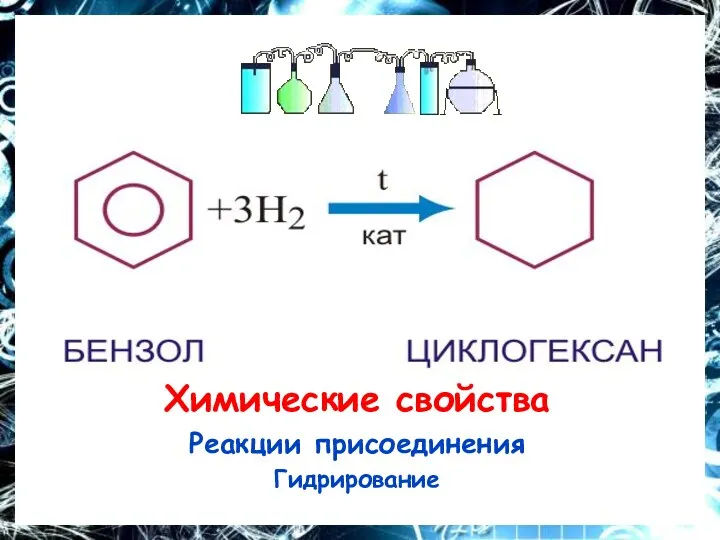
Химические свойства
Реакции присоединения
Гидрирование
Слайд 17
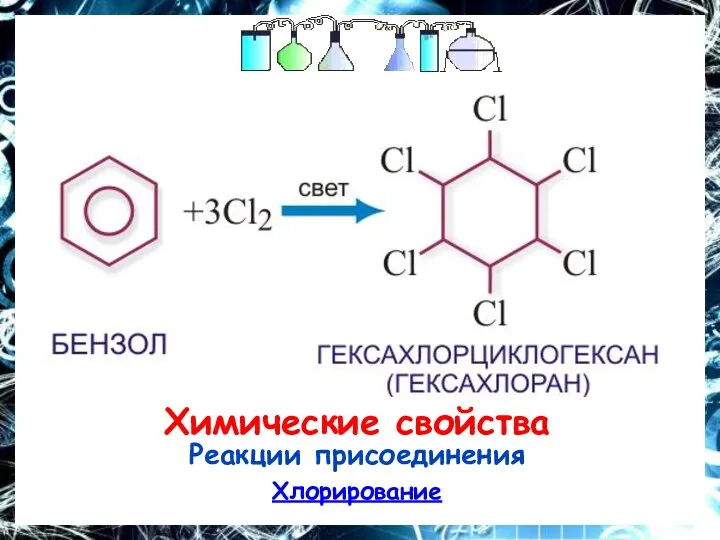
Химические свойства
Реакции присоединения
Хлорирование
Слайд 18
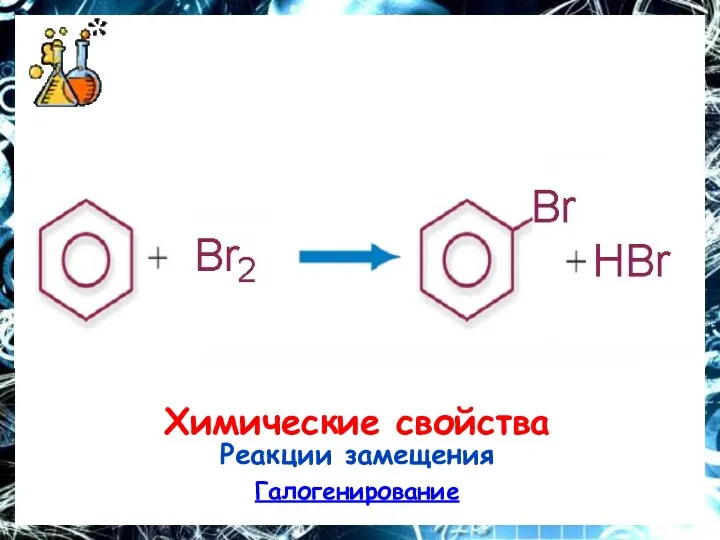
Химические свойства
Реакции замещения
Галогенирование
Слайд 19
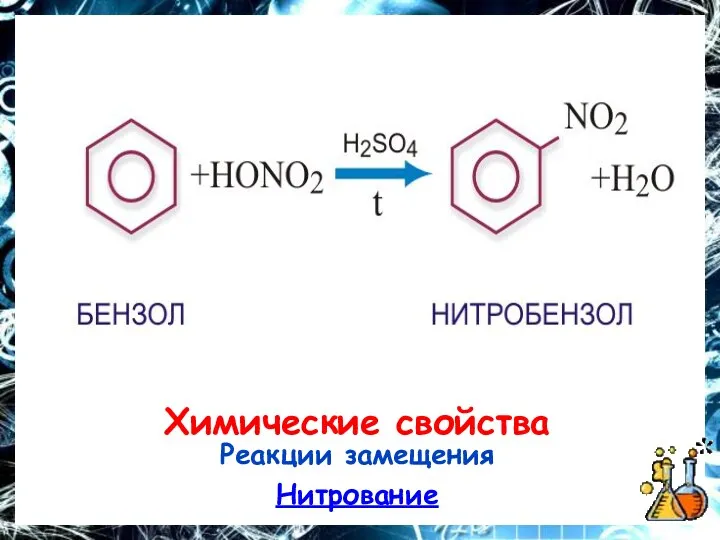
Химические свойства
Реакции замещения
Нитрование


















 Инклюзивное образование
Инклюзивное образование Несеп-тас ауруы кезіндегі дәрілілік емнің негізгі бағыттары
Несеп-тас ауруы кезіндегі дәрілілік емнің негізгі бағыттары Котики
Котики Языковая личность в коммуникативном пространстве социальных сетей Facebook и Вконтакте
Языковая личность в коммуникативном пространстве социальных сетей Facebook и Вконтакте Практика по орг. занятий
Практика по орг. занятий Инновационные технологии в развитии музыкальности детей дошкольного возраста
Инновационные технологии в развитии музыкальности детей дошкольного возраста Порядок организации и проведения процедур закупок в ОАО РЖД
Порядок организации и проведения процедур закупок в ОАО РЖД Технология психолого-педагогической поддержки ребенка в адаптационный период
Технология психолого-педагогической поддержки ребенка в адаптационный период веселые игрушки
веселые игрушки 8 марта – праздник всех женщин
8 марта – праздник всех женщин Основные принципы организации рационального питания в младшем школьном возрасте (презентация)
Основные принципы организации рационального питания в младшем школьном возрасте (презентация) Общие сведения о пожарных извещателях
Общие сведения о пожарных извещателях Урок химии в 8 классе Что изучает химия
Урок химии в 8 классе Что изучает химия Представление информации, языки, кодирование. Информация
Представление информации, языки, кодирование. Информация Программа стажировки инженеров-разработчиков службы главного геолога. ООО Иркутская нефтяная компания
Программа стажировки инженеров-разработчиков службы главного геолога. ООО Иркутская нефтяная компания Промышленная архитектура. Новая Голландия
Промышленная архитектура. Новая Голландия Сладкие блюда и напитки. Часть 1
Сладкие блюда и напитки. Часть 1 Будущая женщина, или Как правильно воспитывать девочку (консультация для родителей)
Будущая женщина, или Как правильно воспитывать девочку (консультация для родителей) Как развивать внимание? (часть 2)
Как развивать внимание? (часть 2) Таможенный контроль товаров и транспортных средств
Таможенный контроль товаров и транспортных средств Презентация: ата- аналар җыелышы
Презентация: ата- аналар җыелышы Обслуговування материнської плати ASUS P5K у складі ПК
Обслуговування материнської плати ASUS P5K у складі ПК Краткое руководство по синтаксису C#. Часть I. Основы
Краткое руководство по синтаксису C#. Часть I. Основы Собор Парижской Богоматери
Собор Парижской Богоматери Создание классной газеты в программе Microsoft Office Publisher 2003 (мастер-класс)
Создание классной газеты в программе Microsoft Office Publisher 2003 (мастер-класс) ВКР: Разработка проекта СТО СМК Внутренний аудит для повышения качества соды кальцинированной
ВКР: Разработка проекта СТО СМК Внутренний аудит для повышения качества соды кальцинированной Предметно-пространственная развивающая среда в соответствии с ФГОС
Предметно-пространственная развивающая среда в соответствии с ФГОС Социальный проект : Скуку, простуду, безделье меняем на бодрость, здоровье, веселье
Социальный проект : Скуку, простуду, безделье меняем на бодрость, здоровье, веселье