Содержание
- 2. Жизнь – это способ существования белковых тел. Ф.Энгельс
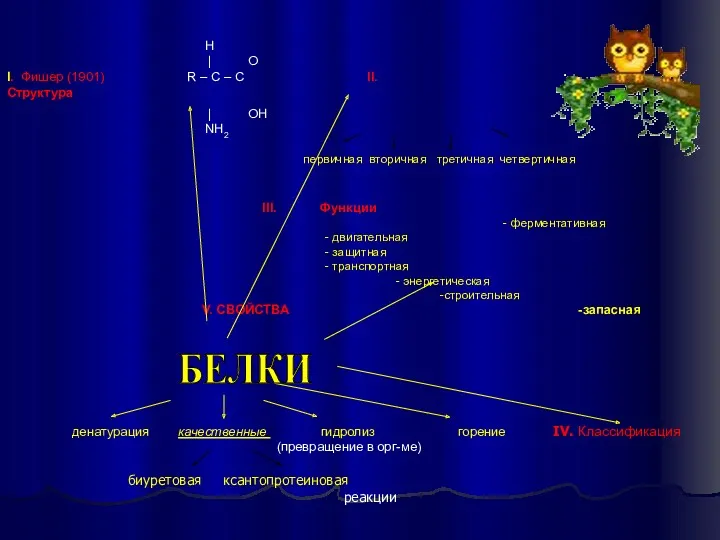
- 4. Н | O I. Фишер (1901) R – C – C II. Структура | OH NH2
- 5. Белок – это высокомолекулярное органическое соединение, представляющее собой биополимер, состоящий из мономеров, которыми являются аминокислоты соединенные
- 6. Белки, входящие в состав живых организмов: * альбумин - яичный белок * кератин - рога, шерсть
- 7. Фишер Эмиль Герман (1852-1919) 1901г.- в продуктах расщепления белков открыл пролин, валин. 1902г.- экспериментально доказал, что
- 8. Аминокислоты- азотсодержащие органические вещества, молекулы которых содержат две функциональные группы: 1. аминогруппу(NH2 ), 2. карбоксильную группу(
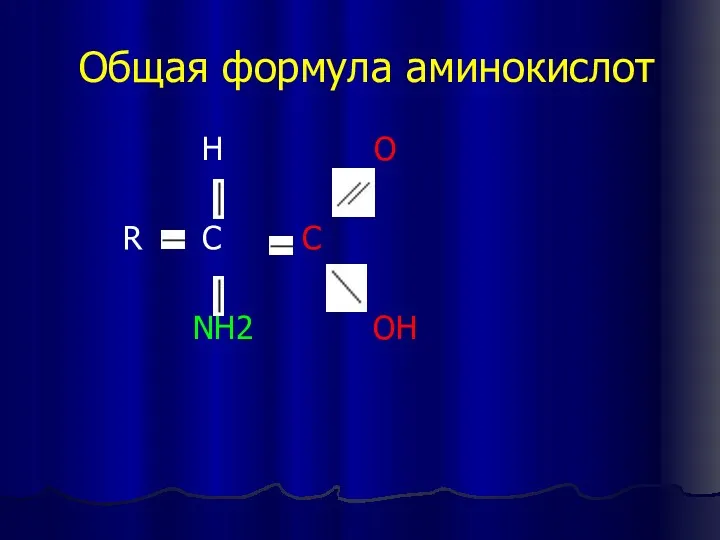
- 9. Общая формула аминокислот H O R C C NH2 OH
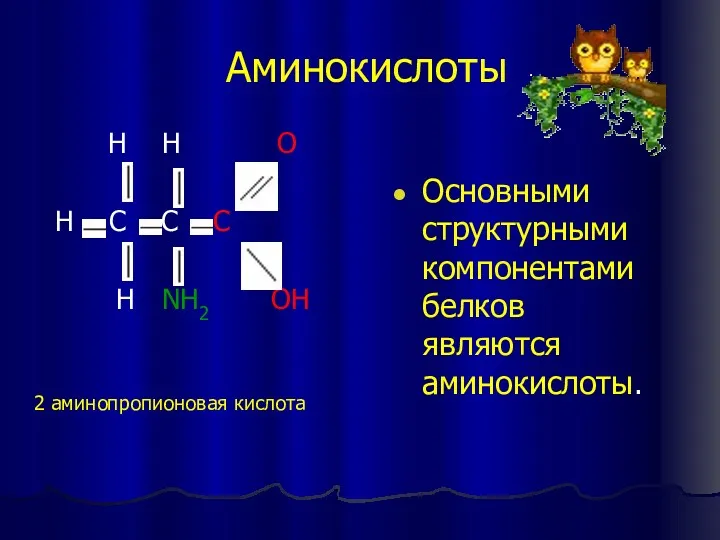
- 10. Аминокислоты H H O H C C C H NH2 OH Основными структурными компонентами белков являются
- 11. Образование пептидной связи NH2 – CH2 – COOH + NH2 – CH2 – COOH = NH2
- 12. В состав белковых веществ входят: углерод, водород, кислород, азот, сера, фосфор. Гемоглобин – C3032H4816O872N780S8Fe4. Молекулярная масса
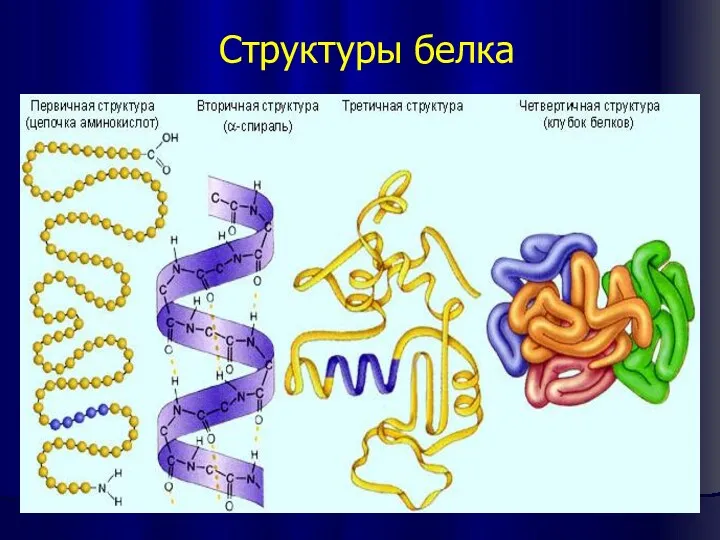
- 13. Структуры белка
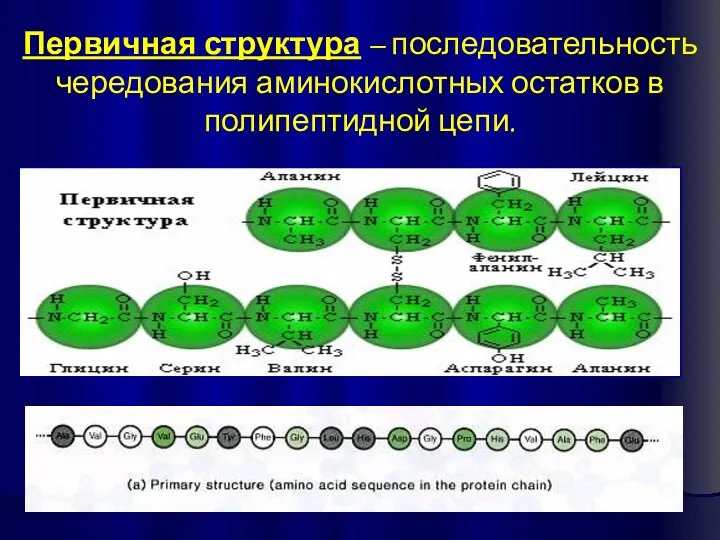
- 14. Первичная структура – последовательность чередования аминокислотных остатков в полипептидной цепи.
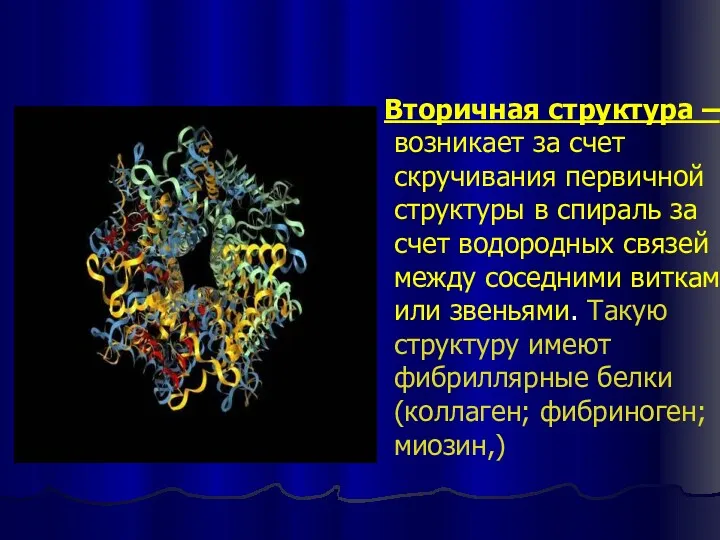
- 15. Вторичная структура – возникает за счет скручивания первичной структуры в спираль за счет водородных связей между
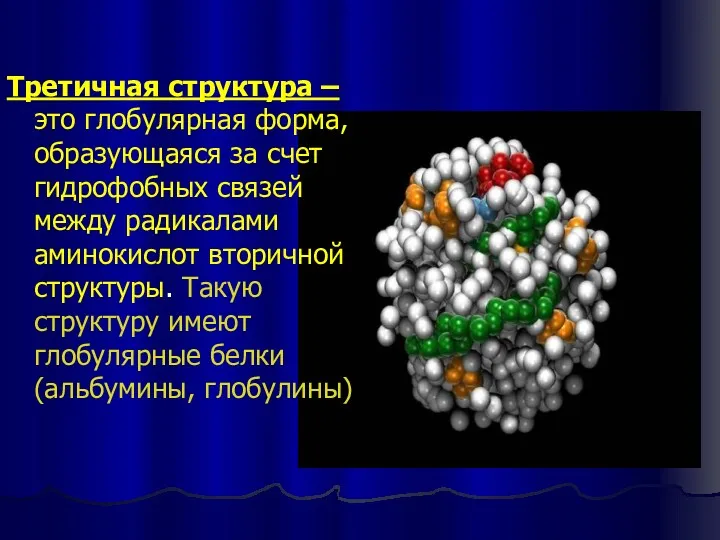
- 16. Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот вторичной структуры.
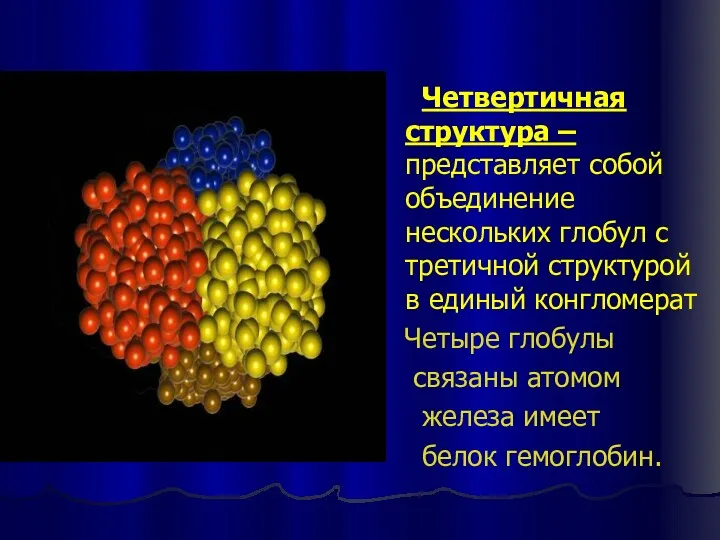
- 17. Четвертичная структура – представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат Четыре глобулы
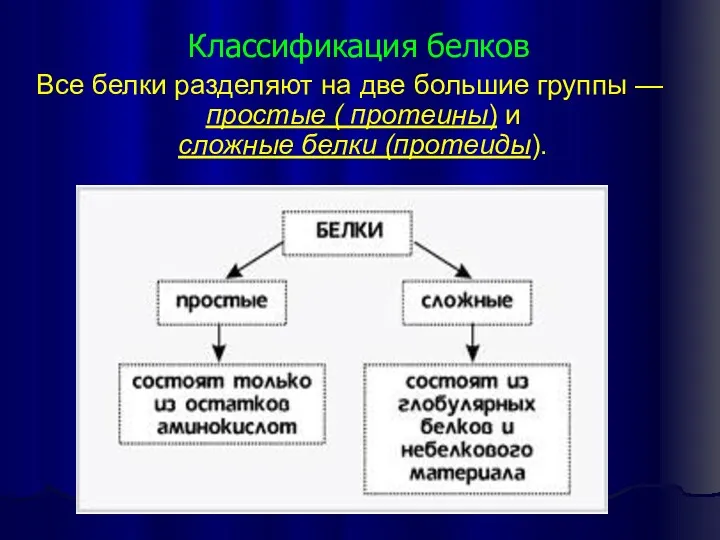
- 18. Классификация белков Все белки разделяют на две большие группы — простые ( протеины) и сложные белки
- 19. Классификация белков Белки могут быть как растворимы, так и нерастворимы в воде в зависимости от их
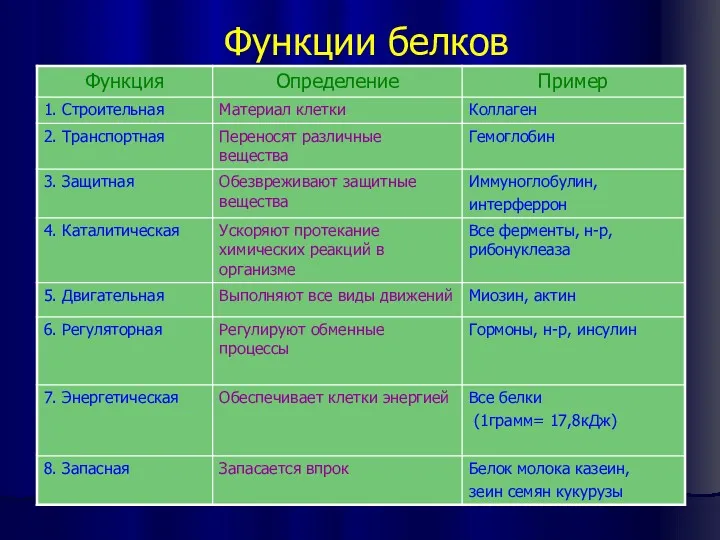
- 20. Функции белков
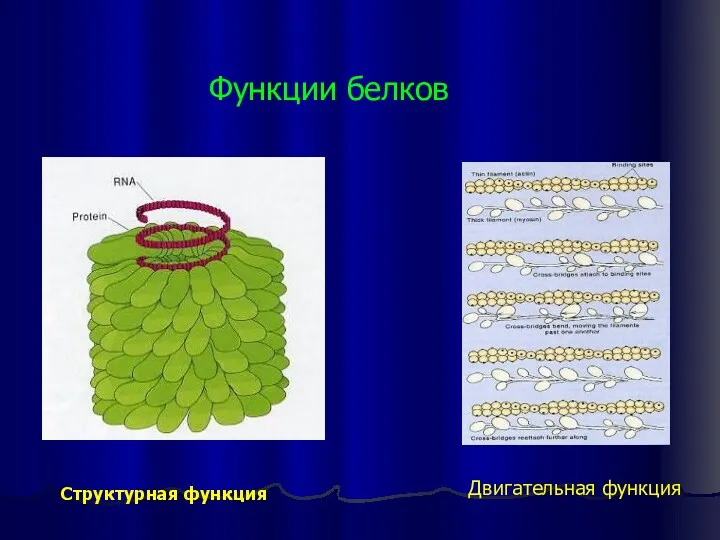
- 21. Функции белков Двигательная функция Структурная функция
- 22. 1. Гидролиз (кислотно-основный, ферментативный), в результате которого образуются аминокислоты. 2. Денатурация – нарушение природной структуры белка
- 23. Свойства белков Кислоты, щелочи и высокая температура разрушают структуру белков и приводят к их денатурации. Белки
- 24. Качественные реакции служат как для определения принадлежности вещества к классу белков, так и для идентификации входящих
- 25. Биуретовая реакция Определяет наличие пептидной связи в растворе исследуемого соединения. пептидная связь
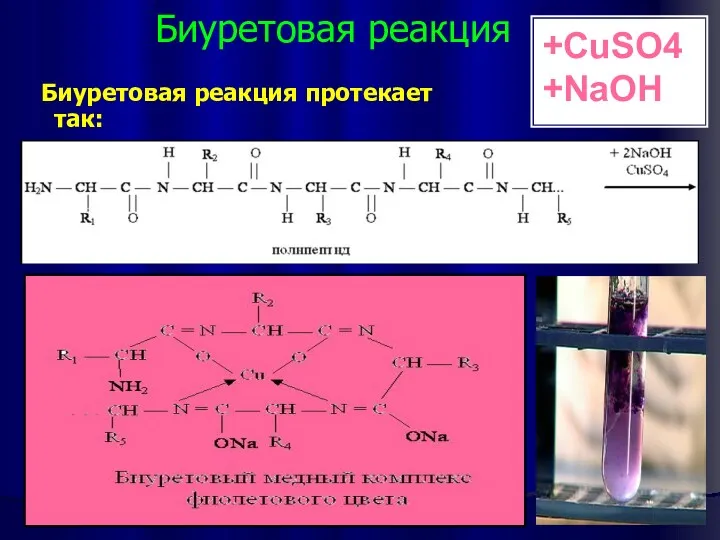
- 26. Биуретовая реакция Биуретовая реакция протекает так: +CuSO4 +NaOH
- 27. Ксантопротеиновая реакция Определяет присутствие в белке аминокислот : 1. триптофана, 2. фенилаланина, 3. тирозина, 4.гистидина.
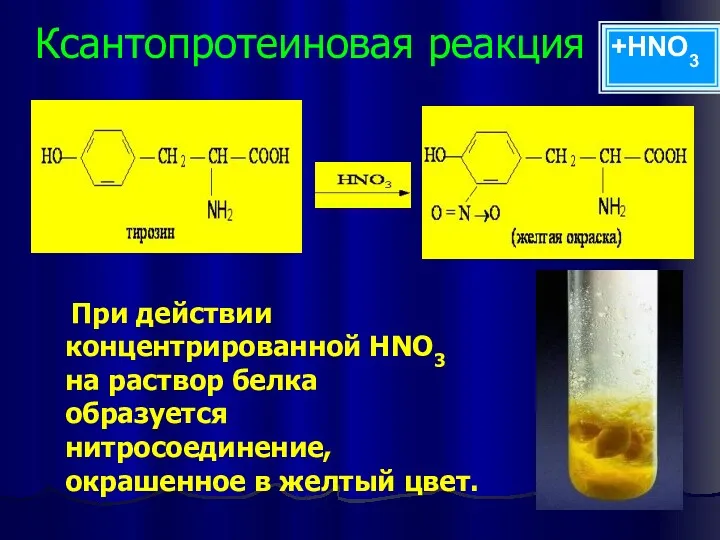
- 28. Ксантопротеиновая реакция При действии концентрированной НNО3 на раствор белка образуется нитросоединение, окрашенное в желтый цвет. +HNO3
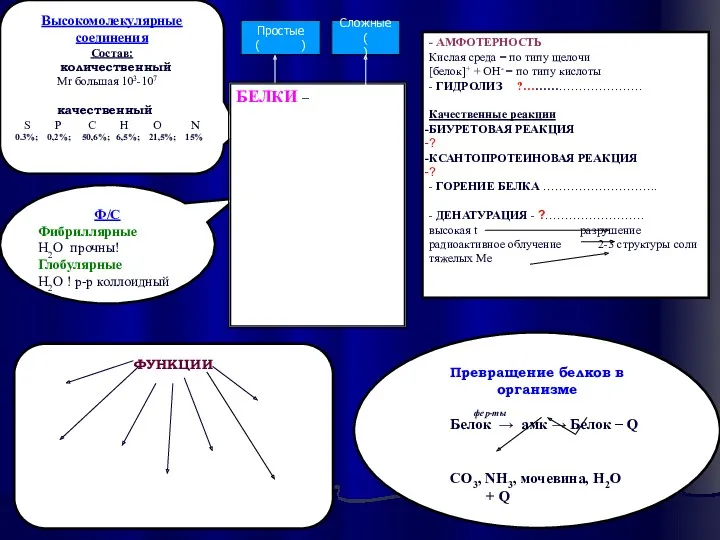
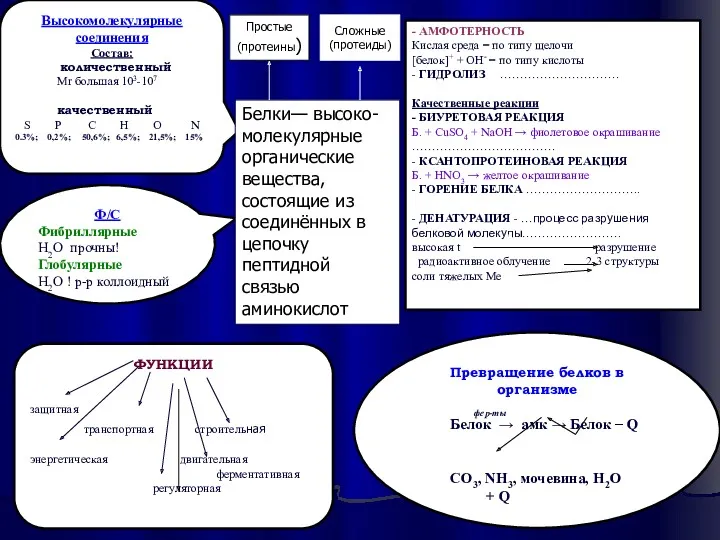
- 29. Высокомолекулярные соединения Состав: количественный Mr большая 103-107 качественный S P C H O N 0.3%; 0,2%;
- 30. Высокомолекулярные соединения Состав: количественный Mr большая 103-107 качественный S P C H O N 0.3%; 0,2%;
- 31. Я всегда говорил и не устаю повторять, что мир не мог существовать, если бы был так
- 32. Домашнее задание: параграфы 26,27
- 34. Скачать презентацию















 Приоритетные отрасли Донбасса
Приоритетные отрасли Донбасса Виды обработки различных материалов. (Лекция 2)
Виды обработки различных материалов. (Лекция 2) Сочинение –рассуждение
Сочинение –рассуждение обследование звукопроизношения и фонетико-фонематической стороны речи
обследование звукопроизношения и фонетико-фонематической стороны речи Ломыга И.В._Психологическая безопасность как фактор корпоративной культуры
Ломыга И.В._Психологическая безопасность как фактор корпоративной культуры Собедование. Правила успешного трудоустройства
Собедование. Правила успешного трудоустройства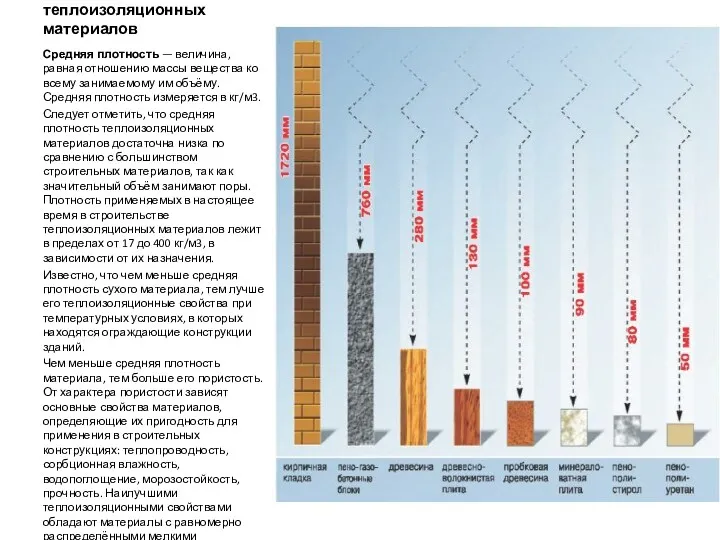 Плотность теплоизоляционных материалов
Плотность теплоизоляционных материалов Производственная структура организации и её элементы. Принципы организации производственного процесса. Тема 7
Производственная структура организации и её элементы. Принципы организации производственного процесса. Тема 7 Динамика движения
Динамика движения Удаление органических веществ, запахов и привкусов содержащихся в воде. (Тема 8.5)
Удаление органических веществ, запахов и привкусов содержащихся в воде. (Тема 8.5) Аренда недвижимого имущества
Аренда недвижимого имущества Электронное портфолио учителя начальных классов
Электронное портфолио учителя начальных классов Сообщающиеся сосуды
Сообщающиеся сосуды Главный циркуляционный контур на АЭС
Главный циркуляционный контур на АЭС С новым годом, Маша
С новым годом, Маша Сечение. Фигура сечения на чертеже
Сечение. Фигура сечения на чертеже Длина окружности
Длина окружности Методическое пособие Контроль знаний по теме: Условные линии на карте
Методическое пособие Контроль знаний по теме: Условные линии на карте Программа капитального ремонта общего имущества в многоквартирных домах на территории ЗАО и ЦАО города Москвы
Программа капитального ремонта общего имущества в многоквартирных домах на территории ЗАО и ЦАО города Москвы Час за часом или какие бывают часы
Час за часом или какие бывают часы Методические рекомендации для воспитателей об агрессивном поведение в дошкольном возрасте.
Методические рекомендации для воспитателей об агрессивном поведение в дошкольном возрасте. Характеристика органических соединений
Характеристика органических соединений Методы решения тригонометрических уравнений
Методы решения тригонометрических уравнений Автоматические выключатели. Общие сведения
Автоматические выключатели. Общие сведения Реализация задач ФГТ в образовательной области Безопасность
Реализация задач ФГТ в образовательной области Безопасность Підвищення ефективності електропостачання торговельних комплексів міста вінниці з використанням сонячної електростанції
Підвищення ефективності електропостачання торговельних комплексів міста вінниці з використанням сонячної електростанції Принципы организации по ведению школ с БА и ХОБЛ
Принципы организации по ведению школ с БА и ХОБЛ электронное портфолио
электронное портфолио