Содержание
- 2. Задачи: Научить определять вещества по качественным реакциям. Развивать умения работать с лабораторным оборудованием и химическими веществами.
- 3. Цель: решить предложенные задачи практическим путём. Оборудование: пробирки в штативе, спиртовка, стакан с водой, пипетки. Реактивы:
- 4. Опыт №2 Определить в какой пробирке каждое вещество? Цвет раствора голубой бесцветный бесцветный Na2SO4 BaSO4 белый
- 5. Опыт №3 Получить вещество Из Mg Mg(OH)2 Mg MgCl2 Mg(OH)2 Mg + HCl = MgCl2 +
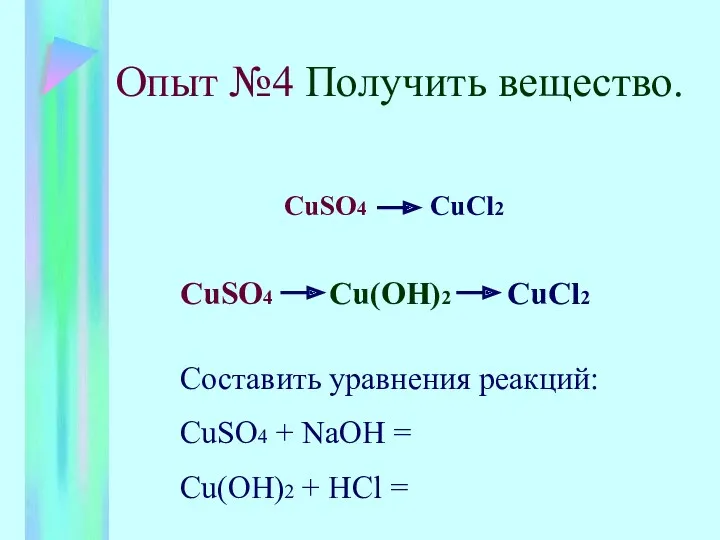
- 6. Опыт №4 Получить вещество. CuSO4 CuCl2 CuSO4 Cu(OH)2 CuCl2 Составить уравнения реакций: CuSO4 + NaOH =
- 7. Опыт №5 Осуществить превращение FeCl3 Fe(OH)3 Fe2O3 FeCl3 + … = Fe(OH)3 + … Fe(OH)3 =
- 8. Решить предложенные задания. Систематизировать формулы оксидов по: а) основности б) амфотерности в) кислотности Mn2O7, BaO, CO,
- 9. Тест 1. Выберите формулы оснований: а) SO3 б) Mg(OH)2 в) H2SO4 г) СаО 2. Если к
- 10. 4. Раствор гидроксида калия вступает в химические реакции с веществами, формулы которых а) СО2 б) H2S
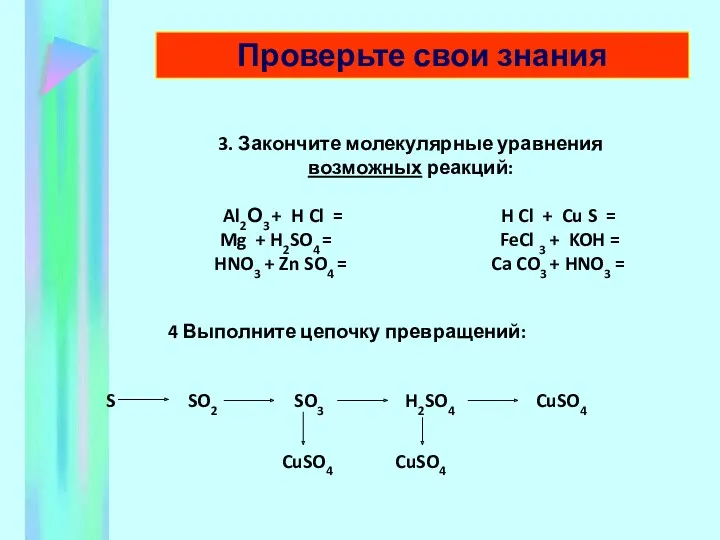
- 11. 3. Закончите молекулярные уравнения возможных реакций: Al2О3 + H Cl = H Cl + Cu S
- 13. Скачать презентацию








 Основные направления, включаемые в сеть высокоскоростных магистралей в России
Основные направления, включаемые в сеть высокоскоростных магистралей в России История создания велосипеда
История создания велосипеда Осанка, признаки правильной осанки, факторы влияющие на формирование осанки, условия для предупреждения ее нарушения
Осанка, признаки правильной осанки, факторы влияющие на формирование осанки, условия для предупреждения ее нарушения Освящение храма в честь иконы Божией Матери Призри на смирение
Освящение храма в честь иконы Божией Матери Призри на смирение Зернові корми та комбікорми
Зернові корми та комбікорми С днем рождения любимая доченька
С днем рождения любимая доченька Презентация урока Формирование территории России по географии 9 класса
Презентация урока Формирование территории России по географии 9 класса Наши достижения. Клуб РЭМ робототехника и электромоделирование
Наши достижения. Клуб РЭМ робототехника и электромоделирование Горы и равнины
Горы и равнины Медиация будущего
Медиация будущего Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Моя Родина - Россия. Классный час 2-4 класс.
Моя Родина - Россия. Классный час 2-4 класс. Адренергические средства. Локализация и физиологические эффекты
Адренергические средства. Локализация и физиологические эффекты 04. ИЗОНИТЬ
04. ИЗОНИТЬ Линейная алгебра
Линейная алгебра Орнамент
Орнамент Антарктида. Географическое положение и история исследования
Антарктида. Географическое положение и история исследования Собрание родителей будущих первоклассников
Собрание родителей будущих первоклассников Мы за мирное детство!
Мы за мирное детство! Занятие по предшкольной подготовке Дикие животные
Занятие по предшкольной подготовке Дикие животные Отчет о выставке творческих работ к Новому году.
Отчет о выставке творческих работ к Новому году. Работа с возражениями клиентов компании Пивград
Работа с возражениями клиентов компании Пивград Презентация Загадки об осени
Презентация Загадки об осени Предварительное обогащение
Предварительное обогащение Логопедическое пособие
Логопедическое пособие презинтация
презинтация Знаменательные и памятные даты 2012 года в истории России
Знаменательные и памятные даты 2012 года в истории России Монтаж на примере программы ShotCut
Монтаж на примере программы ShotCut