Содержание
- 2. У ферментов, имеющих в своем составе несколько мономеров, может быть несколько активных центров по числу субъединиц.
- 5. Множественные формы ферментов можно разделить на две категории: 1. Изоферменты 2. Собственно множественные формы (истинные)
- 6. Изоферменты, или изоэнзимы,– это множественные формы фермента, катализирующие одну и ту же реакцию, но отличающиеся друг
- 7. Виды изоферментов: Органные — например, ферменты гликолиза в печени и мышцах. Клеточные — например, малатдегидрогеназа цитоплазматическая
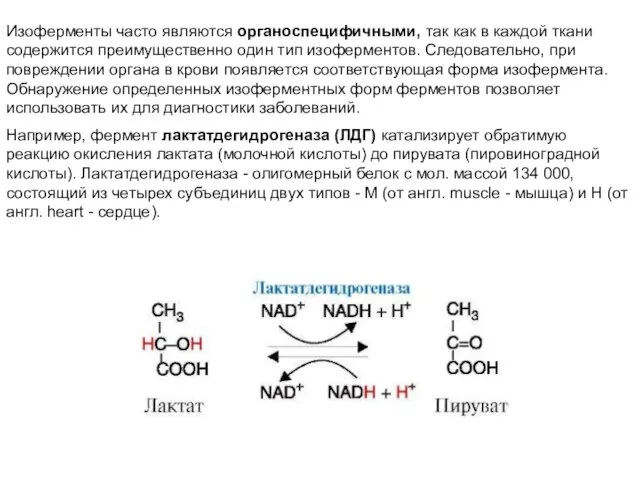
- 8. Изоферменты часто являются органоспецифичными, так как в каждой ткани содержится преимущественно один тип изоферментов. Следовательно, при
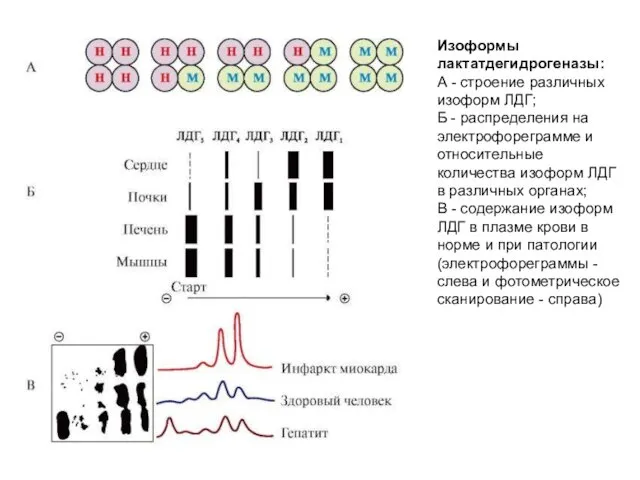
- 9. Комбинация этих субъединиц лежит в основе формирования пяти изоформ лактатдегидрогеназы (рис. А, см. след. слайд). ЛДГ1
- 10. Изоформы лактатдегидрогеназы: А - строение различных изоформ ЛДГ; Б - распределения на электрофореграмме и относительные количества
- 11. Собственно множественные формы (истинные) — это ферменты, синтез которых кодируется одним и тем же аллелем одного
- 12. Итак, термин «множественные формы фермента» применим к белкам, катализирующим одну и ту же реакцию и встречающимся
- 13. Классы ферментов
- 14. Название ферментам в течение долгого времени давали путем добавления окончания -аза к названию субстрата, который участвует
- 15. Для того чтобы систематизировать имеющиеся в природе ферменты, Международный союз биохимии и молекулярной биологии (IUBMB) в
- 16. Эта классификация необходима для точного определения фермента: для каждого фермента имеется кодовое число. Например, фермент маладегидрогеназа
- 17. 1. Оксидоредуктазы катализируют различные окислительно-восстановительные реакции, характеризующиеся переносом электронов и протонов. Класс делится на подклассы: а)
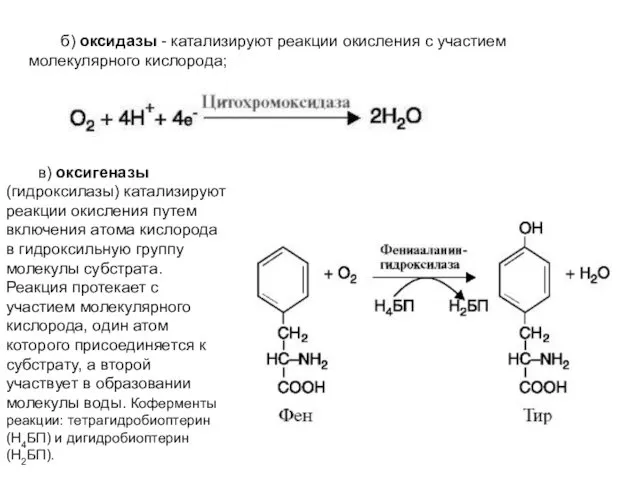
- 18. б) оксидазы - катализируют реакции окисления с участием молекулярного кислорода; в) оксигеназы (гидроксилазы) катализируют реакции окисления
- 19. 2. Трансферазы - катализируют реакции переноса функциональных групп. В зависимости от переносимой группы подразделяются на подклассы:
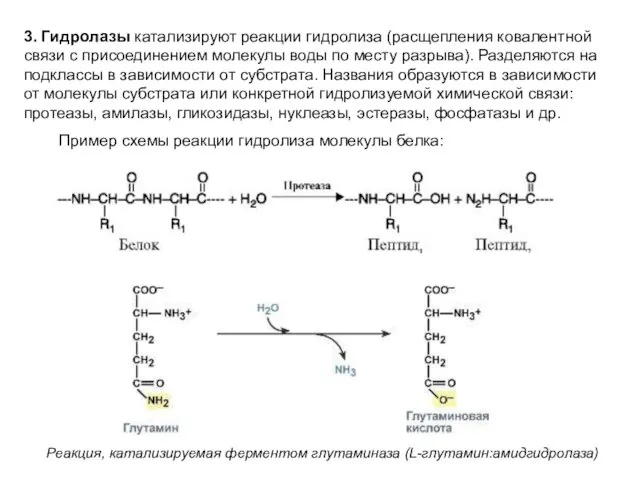
- 20. 3. Гидролазы катализируют реакции гидролиза (расщепления ковалентной связи с присоединением молекулы воды по месту разрыва). Разделяются
- 21. 4. Лиазы - ферменты, отщепляющие от субстратов негидролитическим путем определенные группы (при этом могут отщепляться СО2,
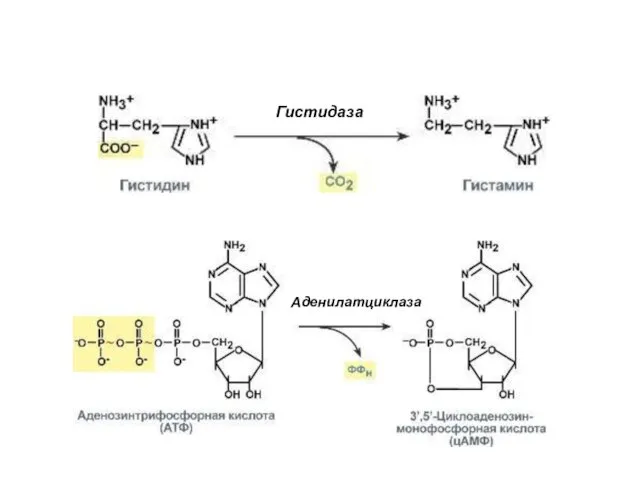
- 22. Гистидаза Аденилатциклаза
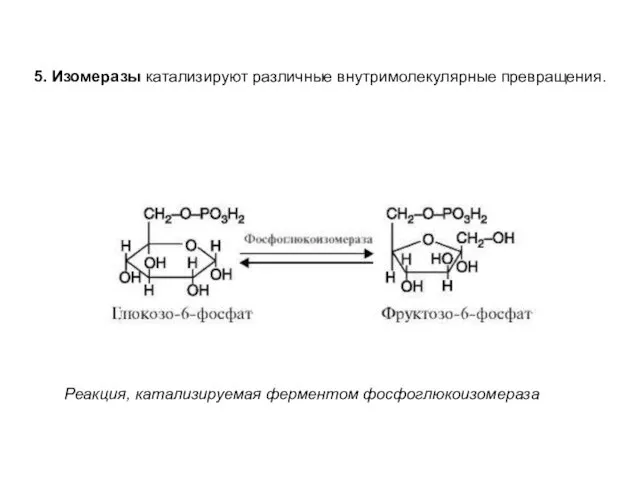
- 23. 5. Изомеразы катализируют различные внутримолекулярные превращения. Реакция, катализируемая ферментом фосфоглюкоизомераза
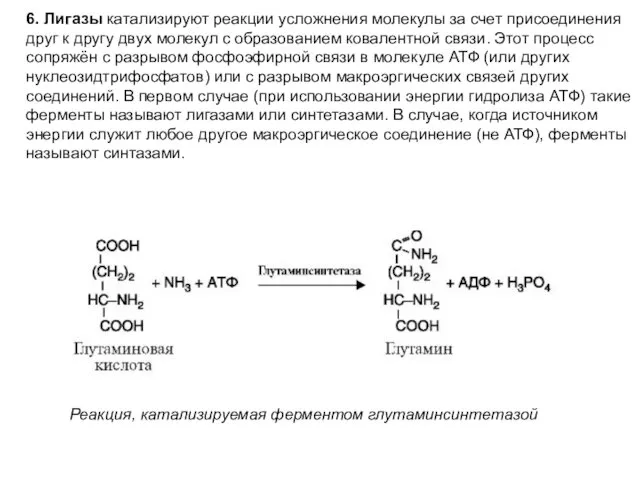
- 24. 6. Лигазы катализируют реакции усложнения молекулы за счет присоединения друг к другу двух молекул с образованием
- 25. РЕГУЛЯЦИЯ АКТИВНОСТИ ФЕРМЕНТОВ
- 26. Одним из важнейших свойств живых организмов является способность к поддержанию гомеостаза. Гомеостаз в организме поддерживается за
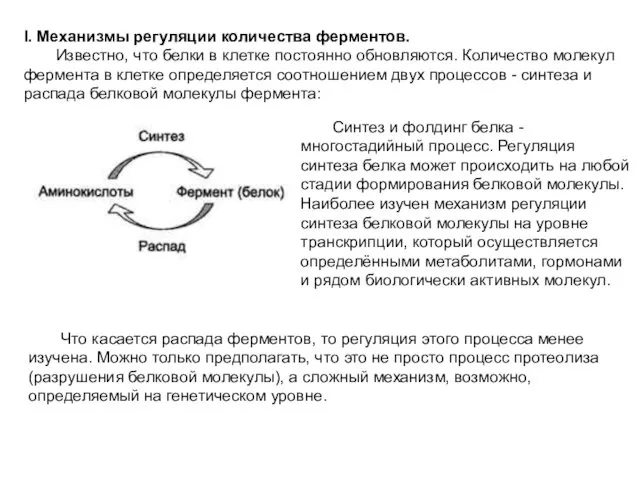
- 27. I. Механизмы регуляции количества ферментов. Известно, что белки в клетке постоянно обновляются. Количество молекул фермента в
- 28. II. Доступность молекул субстратов обеспечивается контролируемой работой трансмембранных транспортных систем. Доступность коферментов зависит от скорости их
- 29. III. Регуляция каталитической активности ферментов. Бывает: 1). Неспецифическая регуляция. В связи с лабильностью всех ферментов, на
- 30. Механизмы специфической регуляции каталитической активности ферментов. К основным способам регуляции каталитической активности молекул ферментов относят: 1).
- 31. ИНГИБИТОРЫ ФЕРМЕНТОВ Под термином «ингибирование активности ферментов» понимают специфическое снижение каталитической активности, вызванное определенными химическими веществами
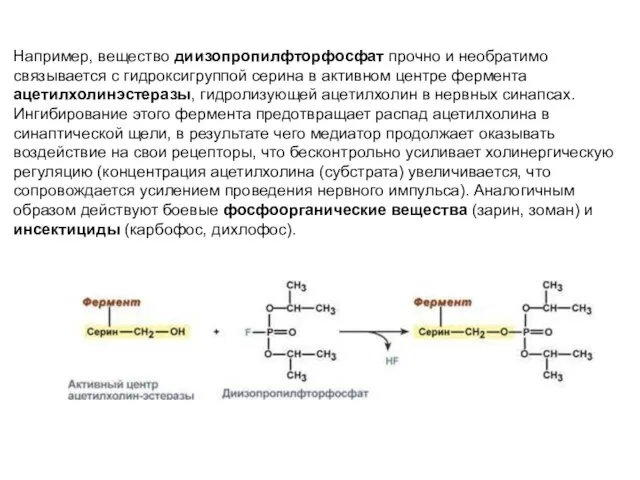
- 32. Например, вещество диизопропилфторфосфат прочно и необратимо связывается с гидроксигруппой серина в активном центре фермента ацетилхолинэстеразы, гидролизующей
- 33. По типу воздействия на зависимость ферментативной реакции от концентрации субстрата обратимые ингибиторы делятся на конкурентные, неконкурентные,
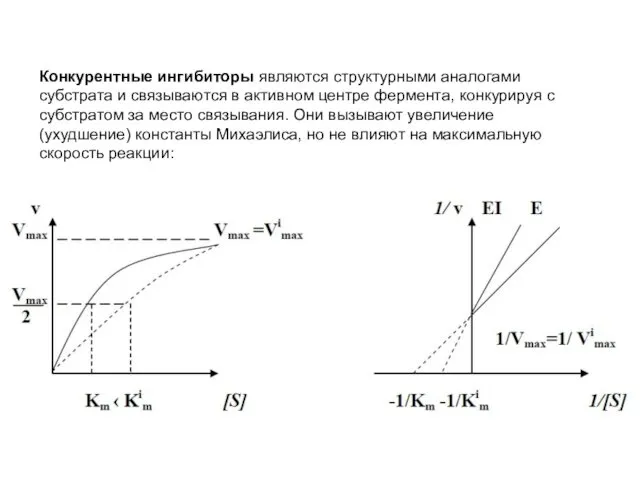
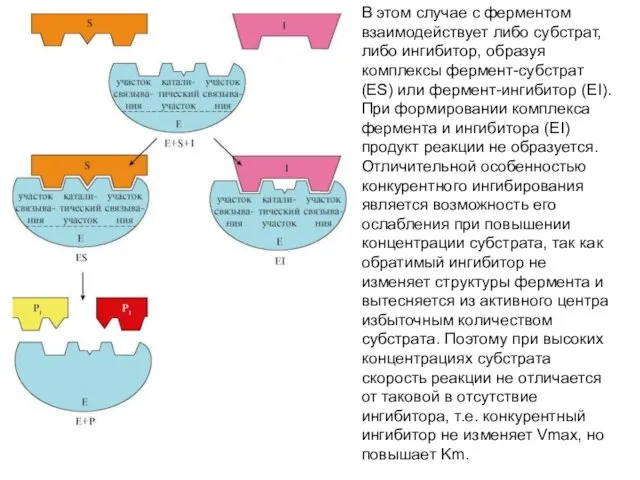
- 34. Конкурентные ингибиторы являются структурными аналогами субстрата и связываются в активном центре фермента, конкурируя с субстратом за
- 35. В этом случае с ферментом взаимодействует либо субстрат, либо ингибитор, образуя комплексы фермент-субстрат (ES) или фермент-ингибитор
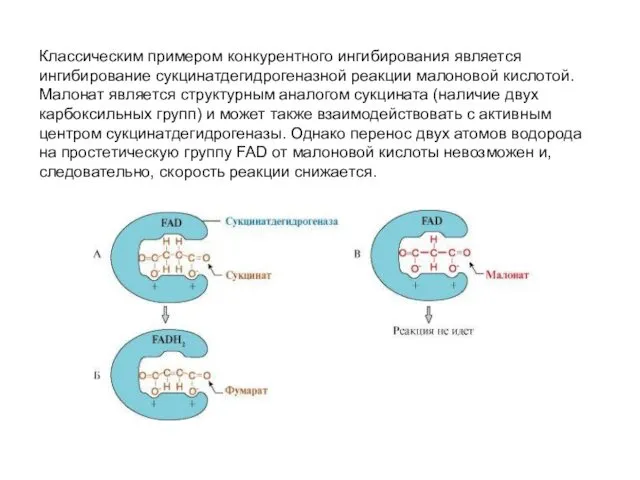
- 36. Классическим примером конкурентного ингибирования является ингибирование сукцинатдегидрогеназной реакции малоновой кислотой. Малонат является структурным аналогом сукцината (наличие
- 37. Неконкурентное ингибирование наблюдается, если ингибитор связывается вне активного центра. Ингибитор реагирует с функционально важной группой фермента,
- 38. Бесконкурентное ингибирование - ингибитор связывается только с фермент-субстратным комплексом, но не со свободным ферментом, изменяя его
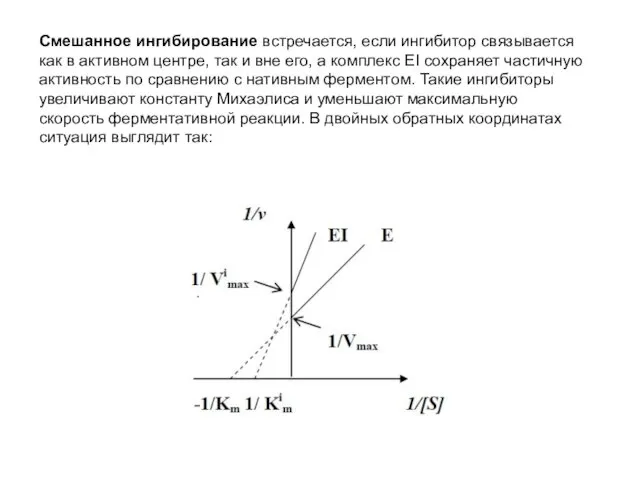
- 39. Смешанное ингибирование встречается, если ингибитор связывается как в активном центре, так и вне его, а комплекс
- 41. Аллостерическая регуляция Ферменты, имеющие такой механизм регуляции, являются, как правило, олигомерными белками. Они состоят из нескольких
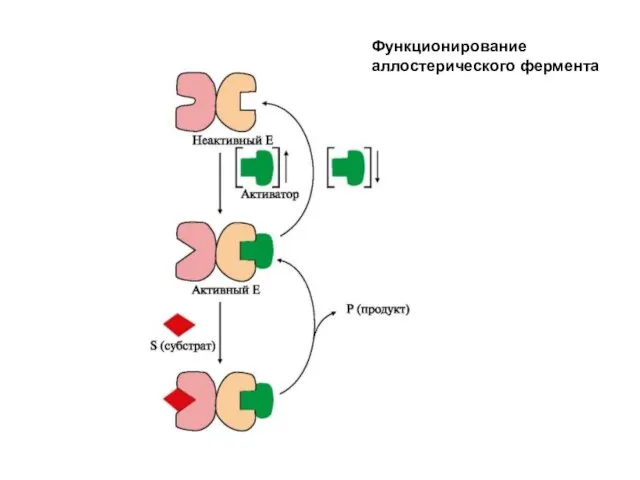
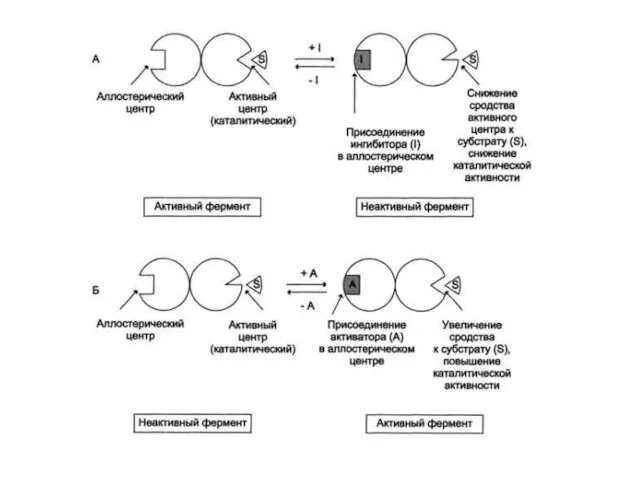
- 42. Функционирование аллостерического фермента
- 43. Аллостерические ферменты имеют определенные особенности строения: - обычно являются олигомерными белками, состоящими из нескольких протомеров; -
- 44. Аллостерические ферменты обладают свойством кооперативности: взаимодействие аллостерического эффектора с аллостерическим центром вызывает кооперативное изменение конформации всех
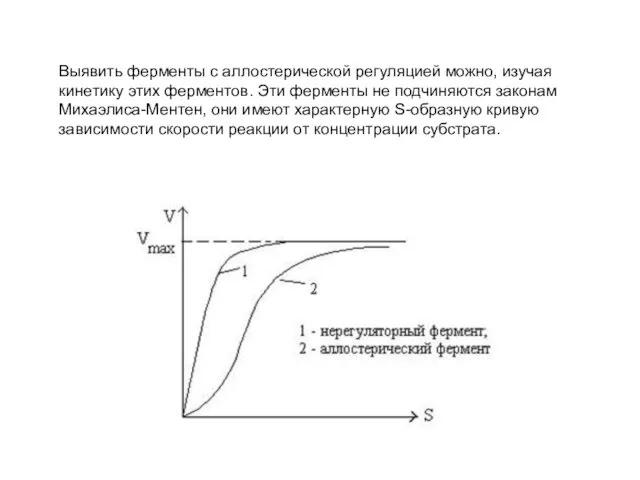
- 46. Выявить ферменты с аллостерической регуляцией можно, изучая кинетику этих ферментов. Эти ферменты не подчиняются законам Михаэлиса-Ментен,
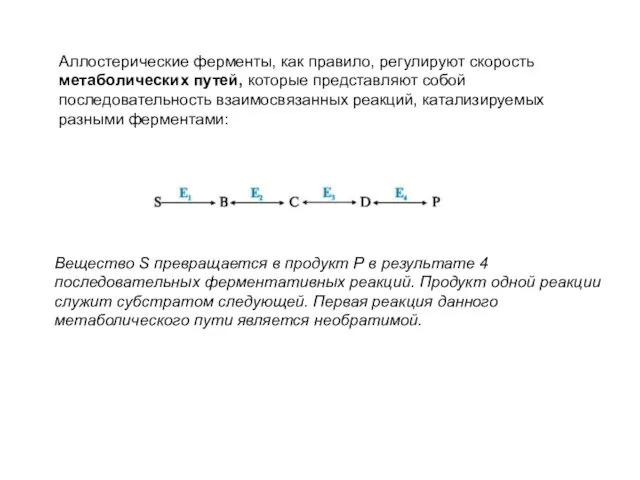
- 47. Аллостерические ферменты, как правило, регулируют скорость метаболических путей, которые представляют собой последовательность взаимосвязанных реакций, катализируемых разными
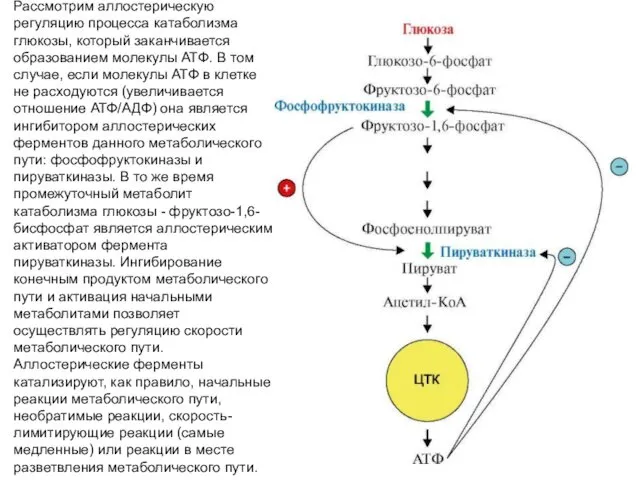
- 49. Рассмотрим аллостерическую регуляцию процесса катаболизма глюкозы, который заканчивается образованием молекулы АТФ. В том случае, если молекулы
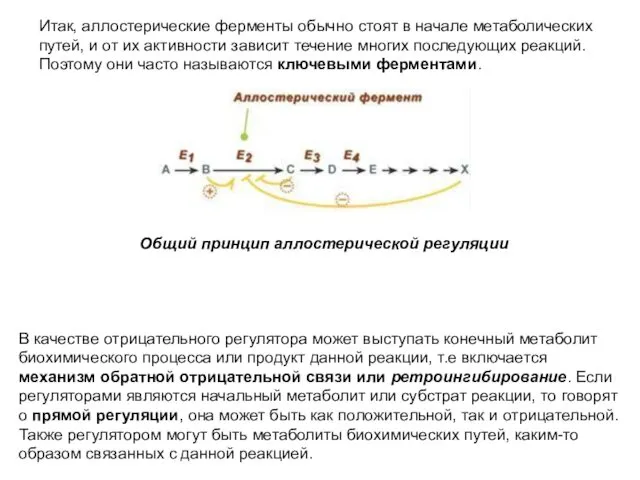
- 50. Итак, аллостерические ферменты обычно стоят в начале метаболических путей, и от их активности зависит течение многих
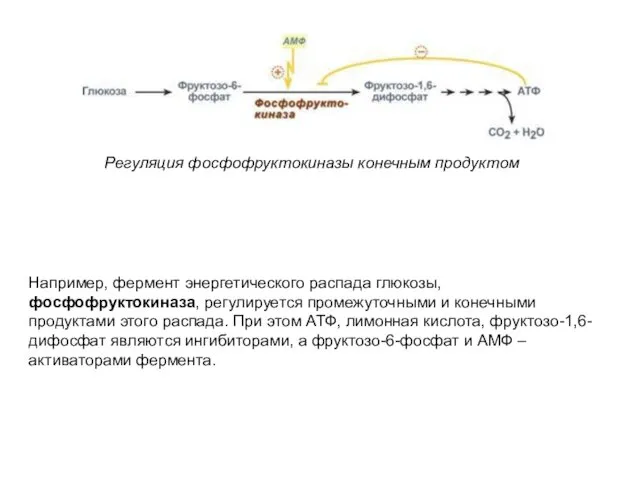
- 51. Регуляция фосфофруктокиназы конечным продуктом Например, фермент энергетического распада глюкозы, фосфофруктокиназа, регулируется промежуточными и конечными продуктами этого
- 52. Регуляция с помощью белок-белковых взаимодействий Некоторые ферменты изменяют свою активность в результате белок-белковых взаимодействий. Можно выделить
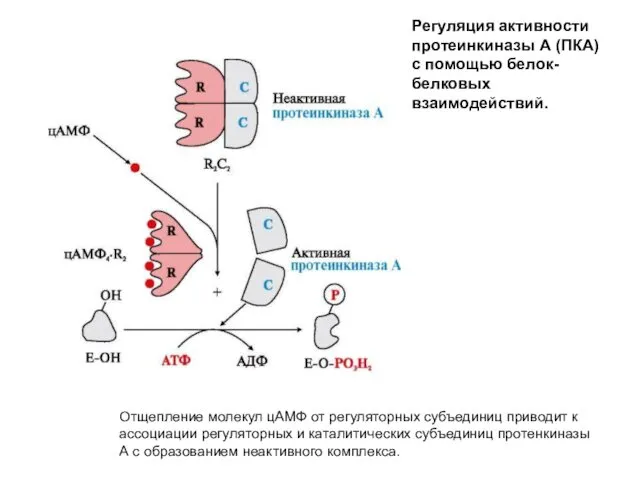
- 53. В качестве примера регуляции каталитической активности ферментов ассоциацией или диссоциацией протомеров можно рассмотреть регуляцию фермента протеинкиназы
- 54. Отщепление молекул цАМФ от регуляторных субъединиц приводит к ассоциации регуляторных и каталитических субъединиц протенкиназы А с
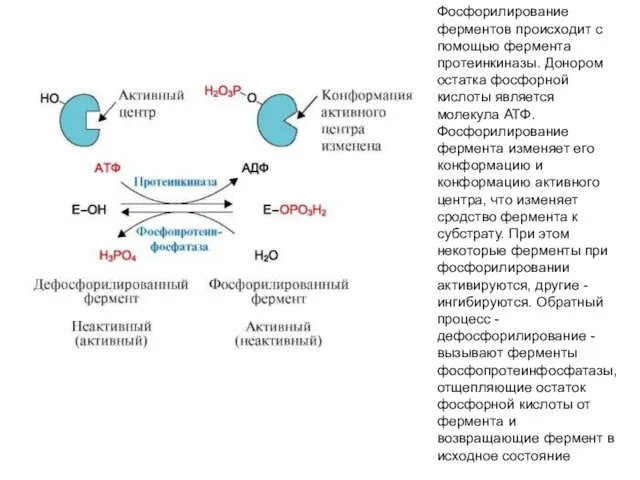
- 55. Регуляция каталитической активности ферментов путем фосфорилирования-дефосфорилирования В биологических системах часто встречается механизм регуляции активности ферментов с
- 56. Фосфорилирование ферментов происходит с помощью фермента протеинкиназы. Донором остатка фосфорной кислоты является молекула АТФ. Фосфорилирование фермента
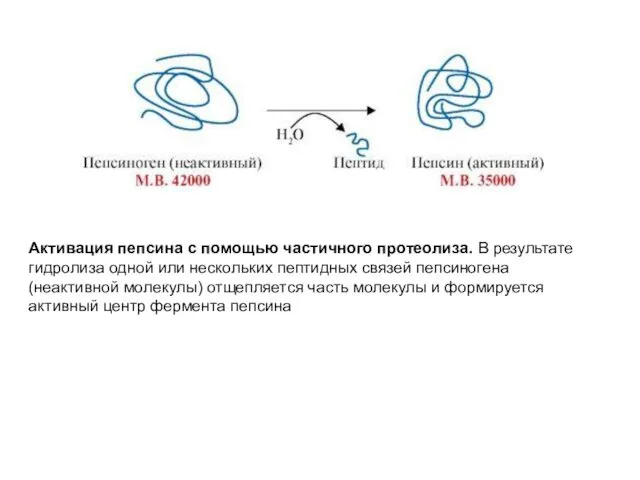
- 57. Регуляция каталитической активности ферментов частичным (ограниченным) протеолизом Некоторые ферменты, которые функционируют вне клеток (в желудочно-кишечном тракте
- 58. Активация пепсина с помощью частичного протеолиза. В результате гидролиза одной или нескольких пептидных связей пепсиногена (неактивной
- 60. Скачать презентацию
































 Дизайн и архитектура моего сада. 7 класс
Дизайн и архитектура моего сада. 7 класс Разработка и экономическое обоснование экскурсионного маршрута
Разработка и экономическое обоснование экскурсионного маршрута Профессия - полицейский.
Профессия - полицейский. Кафе быстрого обслуживания Dio Cafe
Кафе быстрого обслуживания Dio Cafe Строение атома
Строение атома Общие особенности античной философии
Общие особенности античной философии Урок технологии швейного дела
Урок технологии швейного дела Что такое учебный проект
Что такое учебный проект Биохимические методы исследования,используемые в эндокринологии,в норме и в патологии,иетерпретация результатов
Биохимические методы исследования,используемые в эндокринологии,в норме и в патологии,иетерпретация результатов День профессий 2022
День профессий 2022 Пасха. Светлое Христово Воскресение
Пасха. Светлое Христово Воскресение Четыре замечательные точки треугольника
Четыре замечательные точки треугольника Портфолио Андрея Джеджулы
Портфолио Андрея Джеджулы Раны. Раневой процесс
Раны. Раневой процесс Component Enabler for .NET
Component Enabler for .NET Организационные формы обучения
Организационные формы обучения Успехи в освоении технологии за 6 класс
Успехи в освоении технологии за 6 класс ПОУ СКУИТ Северодвинский колледж управления и информационных технологий
ПОУ СКУИТ Северодвинский колледж управления и информационных технологий Мастер-класс для родителей Артикуляционная гимнастика
Мастер-класс для родителей Артикуляционная гимнастика сценарий и презентация праздника ко дню Победы. Я еще не хочу умирать
сценарий и презентация праздника ко дню Победы. Я еще не хочу умирать праздник Осени во 2 классе
праздник Осени во 2 классе презентация к занятию Земля - наш общий дом!
презентация к занятию Земля - наш общий дом! Шахта лифта в панельных зданиях. Опирание перекрытий на шахту лифта. (Тест 3.1)
Шахта лифта в панельных зданиях. Опирание перекрытий на шахту лифта. (Тест 3.1) Презентация Индийский океан
Презентация Индийский океан Русская Православная церковь. Страницы истории. Обзор
Русская Православная церковь. Страницы истории. Обзор Знатоки правил дорожного движения
Знатоки правил дорожного движения Международный валютный рынок
Международный валютный рынок Натюрморт в технике гризайль
Натюрморт в технике гризайль