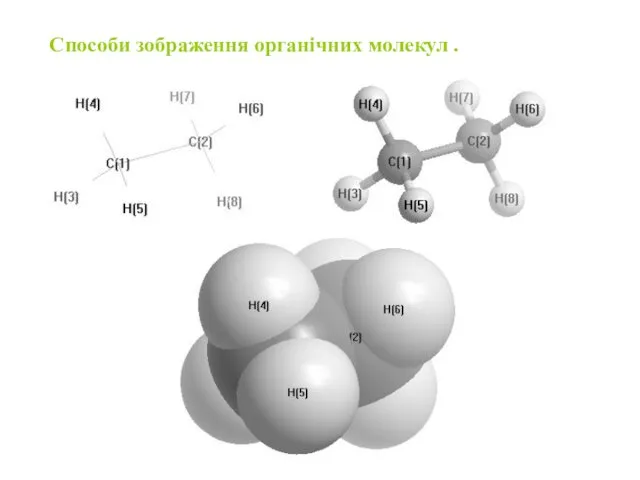
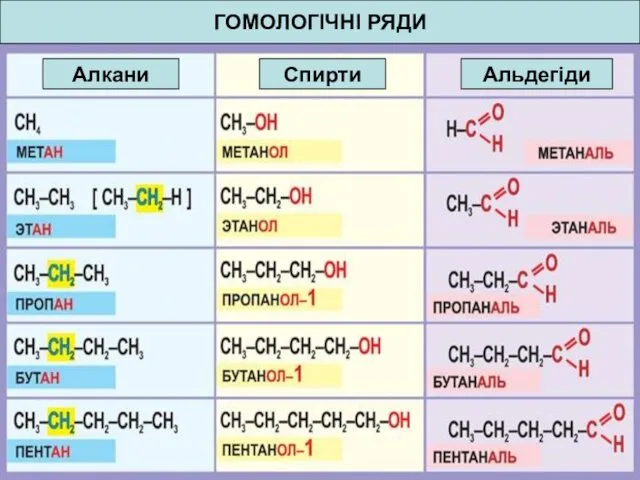
Причини багатоманітності сполук Карбону
Сполуки Карбону вивчаються у курсі органічної хімії. Тільки
невелика кількість із сполук Карбону вважається неорганічними. Проте такий розподіл умовний і спирається більше на традиції, ніж на особливості будови і властивості сполук Карбону.
Крім простих речовин, що утворює цей хімічний елемент
(алмаз, графіт, карбін, букибол…),
а також карбідів,
оксидів карбону (ІІ) і (ІV),
карбонілів металів ( наприклад Fe(CO)5 ),
карбонатної кислоти і карбонатів,
сірковуглецю,
ціанідної ( HCN ), ціанатної ( HOCN ), тіоціанатної ( HSOCN ) кислот та їх солей,
Карбон ( С* 1s2 2s1 2p3 ),
виявляючи валентність – ІV ( >•< )
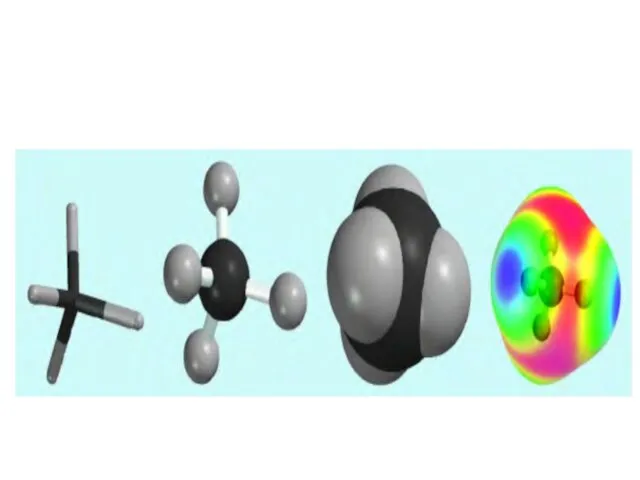
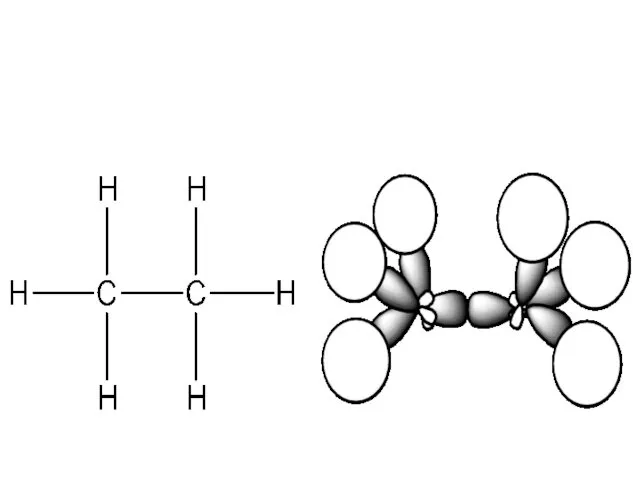
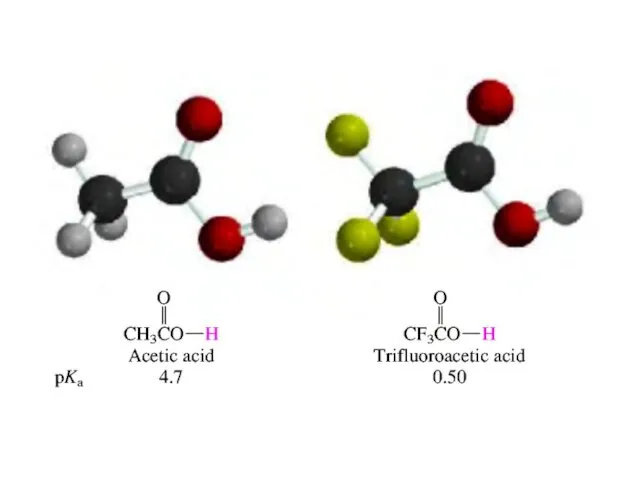
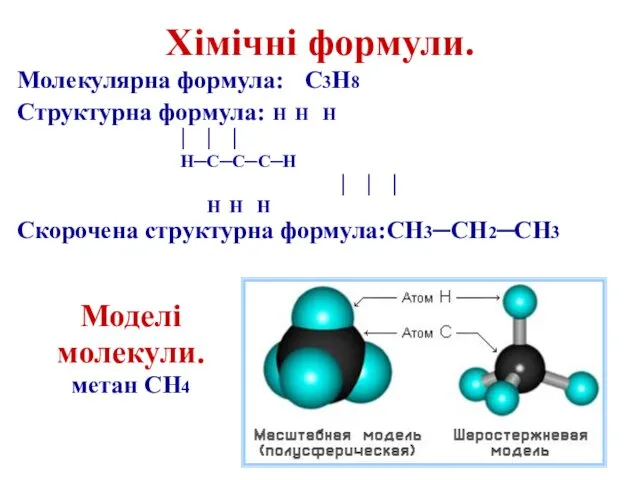
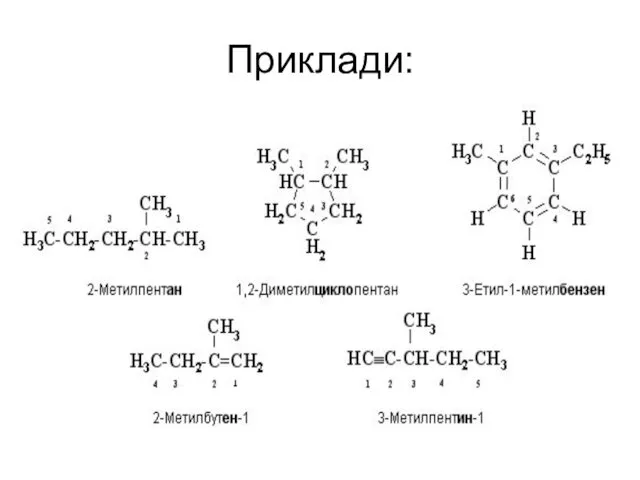
і ковалентно зв'язуючись з невеликим числом інших хімічних елементів (H, O, S, N, P, Hal, та де-які Me), утворює ще >30 млн.сполук, число яких постійно збільшується так як щорічно вилучають із природної сировини або синтезують ≈ 300 тис. нових речовин.
Число сполук Карбону більш ніж в 50 раз перевищує число відомих сполук всіх інших хімічних елементів.








 Навыки уверенного человека
Навыки уверенного человека Математический аппарат для проектирования компьютерных сетей. Нахождение максимального потока
Математический аппарат для проектирования компьютерных сетей. Нахождение максимального потока Основы анатомии и физиологии животных
Основы анатомии и физиологии животных урок технологии в 1 классе Веселая гусеница
урок технологии в 1 классе Веселая гусеница Щелочные металлы: общая характеристика 9 класс
Щелочные металлы: общая характеристика 9 класс Газпромбанк. Комплексная программа
Газпромбанк. Комплексная программа Файлы и файловые системы
Файлы и файловые системы Общая характеристика галогенов на основе положения химических элементов в периодической системе
Общая характеристика галогенов на основе положения химических элементов в периодической системе Родительское собрание Учим детей мыслить
Родительское собрание Учим детей мыслить Современные материалы для изготовления трубопроводов
Современные материалы для изготовления трубопроводов Сравнительный анализ софизмов и парадоксов
Сравнительный анализ софизмов и парадоксов Колбасные изделия
Колбасные изделия Презентация урока Строгание Специальность:Мастер столярного и мебельного производства.
Презентация урока Строгание Специальность:Мастер столярного и мебельного производства. Предпосылки открытия периодического закона Д.И. Менделеевым
Предпосылки открытия периодического закона Д.И. Менделеевым Чудо-писанки
Чудо-писанки Презентация к логопедическому занятию Полевые цветы
Презентация к логопедическому занятию Полевые цветы Презентация Суша часть 2
Презентация Суша часть 2 Презентация1
Презентация1 Горные породы и минералы.
Горные породы и минералы. Мое ПОРТФОЛИО
Мое ПОРТФОЛИО Самоанализ работы учителя-логопеда за 2014-2015 учебный год
Самоанализ работы учителя-логопеда за 2014-2015 учебный год Транспорт в моем городе. Фрагмент урока географии.
Транспорт в моем городе. Фрагмент урока географии. Интеграция ИКТ в воспитательно - образовательный процесс в ДОУ
Интеграция ИКТ в воспитательно - образовательный процесс в ДОУ Презентация на тему: Глаза-главные помощники человека.
Презентация на тему: Глаза-главные помощники человека. Средние величины
Средние величины Санатории по кожным заболеваниям
Санатории по кожным заболеваниям 6-ой Всероссийский фестиваль Культуры и Искусства имени Святого праведного воина Федора Ушакова
6-ой Всероссийский фестиваль Культуры и Искусства имени Святого праведного воина Федора Ушакова Определители. Определение определителя
Определители. Определение определителя