Содержание
- 2. Соединения галогенов Галогеноводороды, – Это едкие газы с резким запахом, хорошо раствормые в воде HF HCl
- 3. Получение хлороводорода NaСl(тв) + Н2SО4(конц) = НСl↑ + КНSО4.
- 4. Галогеноводородные кислоты Образуются при растворении галогеноводородов в воде. HF HCl HBr HI Фтороводородная кислота ( плавиковая)
- 5. Оксокислоты Хлорная – НСlO4 Сl2O7 Хлорноватая – НСlO3 Сl2O5 Хлористая – НСlO2 Сl2O3 Хлорноватистая- НСlO Сl2O
- 6. Качественная реакция на галогенид - ионы Взаимодействие с ионом серебра: (AgNO3) AgNO3 + KCl = KNO3
- 7. Фтор F2 Открыт Муассаном в 1886 году электролизом безводного фторида углерода Плавиковый шпат СаF2 Криолит: Na3AlF6
- 8. Соединения фтора n(-CF2-CF2-) Тефлон устойчив к действию всех известных кислот и их смесей. Он выдерживает температуры
- 9. Хлор Галит (NaCl ) ДДТ (дихлородифенилтрихлорэтан) KClO3 - Бертолетова соль. 2KClO3 + 3S = 2KСl +
- 10. Бром AgBr- фотография NaBr- дубление кожи KBr- линзы LiBr- используется в кондиционерах.
- 12. Скачать презентацию
 Презентация по самообразованию
Презентация по самообразованию Формирование падежных окончаний существительных в родительном падеже
Формирование падежных окончаний существительных в родительном падеже Слава армии родной
Слава армии родной О задачах развития отечественной промышленности в современных социально-экономических условиях
О задачах развития отечественной промышленности в современных социально-экономических условиях Технико-экономическое и оперативное планирование на горном предприятии
Технико-экономическое и оперативное планирование на горном предприятии Формирование многофункционального транспортно-пересадочного узла на базе железнодорожного вокзала г. Красноярска
Формирование многофункционального транспортно-пересадочного узла на базе железнодорожного вокзала г. Красноярска Проектная работа Положительные и отрицательные числа, Занимательная математика. Отчеты.
Проектная работа Положительные и отрицательные числа, Занимательная математика. Отчеты. День народного единства
День народного единства Православные праздники как средство приобщения детей к истокам национальной культуры
Православные праздники как средство приобщения детей к истокам национальной культуры Способы добычи нефти
Способы добычи нефти Развитие языковых способностей дошкольников
Развитие языковых способностей дошкольников Диалоговые окна и элементы управления
Диалоговые окна и элементы управления Основные функции при управлении адаптацией и их распределение
Основные функции при управлении адаптацией и их распределение Презентация: Урок-безопасности Чужой
Презентация: Урок-безопасности Чужой Профессия машинист локомотива
Профессия машинист локомотива Инструментальная палитра программы AUTOCAD-2014
Инструментальная палитра программы AUTOCAD-2014 Презентация к уроку СПИРТЫ
Презентация к уроку СПИРТЫ Master class de português
Master class de português Штрафной бросок в баскетболе
Штрафной бросок в баскетболе Что изучает история
Что изучает история Мы теперь не просто дети!
Мы теперь не просто дети! Возрастные особенности детей 5-6 лет
Возрастные особенности детей 5-6 лет Иммунные заболевания. Аллергии. История алергии
Иммунные заболевания. Аллергии. История алергии Первые названия в честь героев Великой Отечественной войны
Первые названия в честь героев Великой Отечественной войны Все виды разбора
Все виды разбора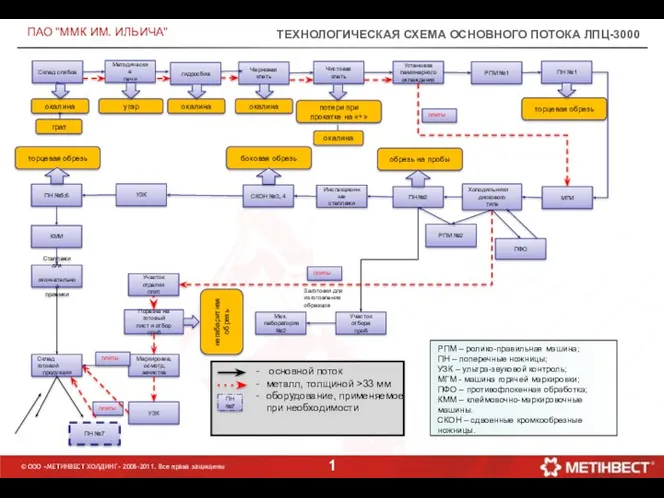 Технологическая схема основного потока ЛПЦ-3000
Технологическая схема основного потока ЛПЦ-3000 Аналіз та оцінка ефективності роботи системи контролю в Державній службі України з надзвичайних ситуацій
Аналіз та оцінка ефективності роботи системи контролю в Державній службі України з надзвичайних ситуацій Русская матрёшка
Русская матрёшка