Содержание
- 2. Раствор – это сложная равновесная химическая система, образованная растворителем, растворенным веществом и продуктами их взаимодействия.
- 3. 3 Растворами называют однородные (гомогенные) системы , состоящие из двух или нескольких компонентов, состав которых можно
- 4. Растворы 4 газообразные: газ-газ (воздух, смеси газов); жидкие: газ –жидкость, жидкость-жидкость, твердое вещество-жидкость; твердые: газ-твёрдое вещество,
- 5. Большая роль в установлении природы процесса растворения принадлежит Д. И. Менделееву – создателю химической теории растворов.
- 6. Основные теории растворов Физическая Растворитель является инертной средой, в которую могут диффундировать частицы растворенного вещества Химическая
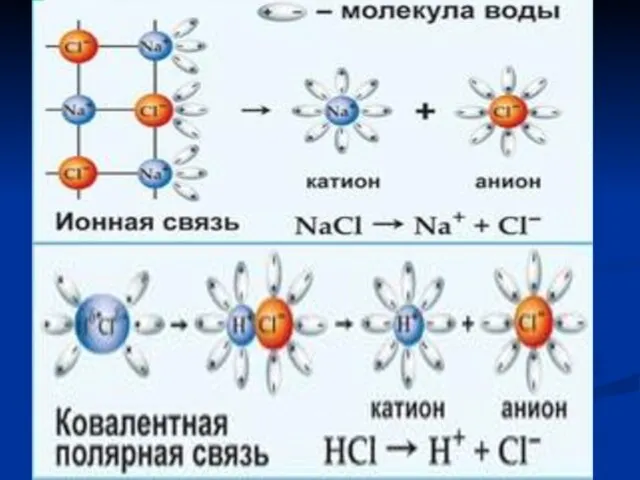
- 7. - молекулярная диссоциация, - образование сольватов, - ионизация , - электролитическая диссоциация. Растворение – это сложный
- 8. 6
- 10. Концентрация раствора – это количество растворённого вещества, содержащееся в единице массы, единице объема раствора или растворителя.
- 11. Моляльная концентрация (моляльность) «Сm» – число молей растворенного вещества в 1000 г растворителя. Выражается в моль/1000
- 12. Растворимость – это способность вещества образовывать с другими соединениями (растворителями) растворы. 11 Титр (Тв) – число
- 13. 1. Природа растворяемого вещества. Кристаллические вещества подразделяются: Р – хорошо растворимые (более 1,0 г на 100
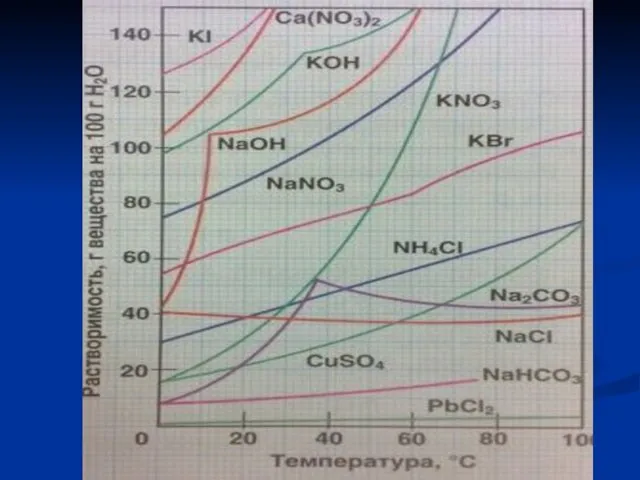
- 14. 4. ВЛИЯНИЕ ТЕМПЕРАТУРЫ. ПРИ НАГРЕВАНИИ ДЛЯ БОЛЬШИНСТВА СОЛЕЙ ХАРАКТЕРНО УВЕЛИЧЕНИЕ РАСТВОРИМОСТИ ПРИ НАГРЕВАНИИ. РАСТВОРИМОСТЬ ГАЗОВ В
- 16. Вода – наиболее распространенное в природе вещество. Общее количество составляет 1,39·1018 тонн. Свойство D2O H2O Молекулярная
- 17. Аномальные свойства воды высокая температура плавления; высокая удельная теплоемкость воды; изменение плотности с изменением температуры; высокое
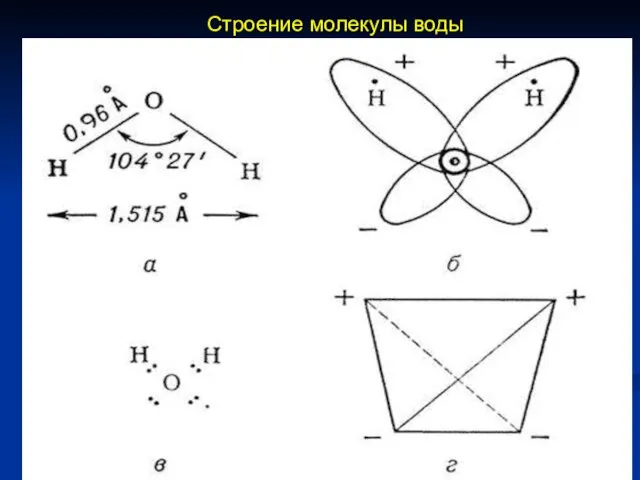
- 18. Свойства воды обусловлены тремя факторами: полярным характером молекул; наличием неподеленных пар электронов у атомов кислорода; образованием
- 19. Строение молекулы воды
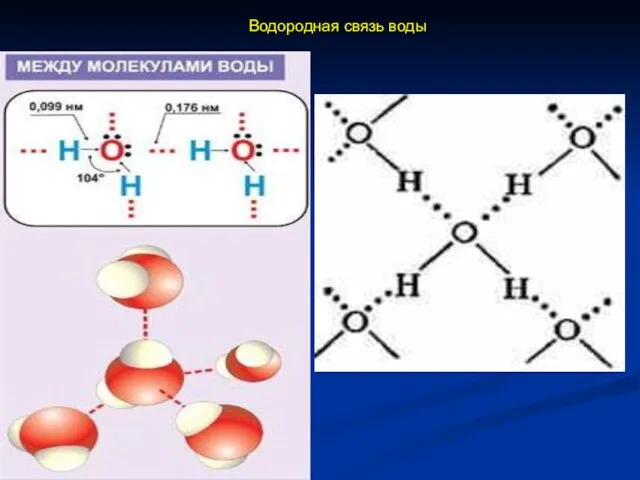
- 20. Водородная связь воды
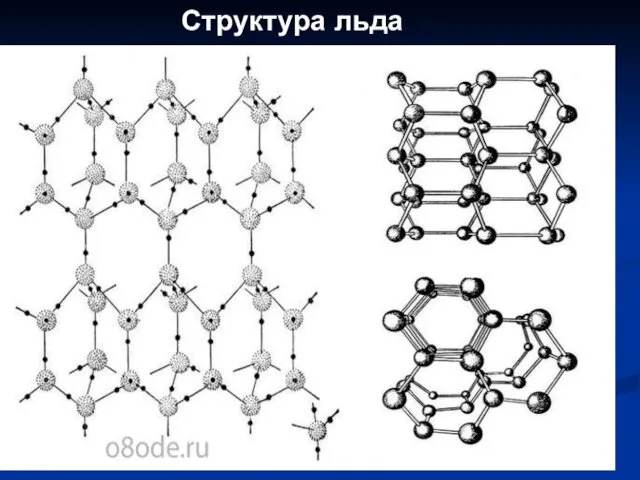
- 21. Структура льда
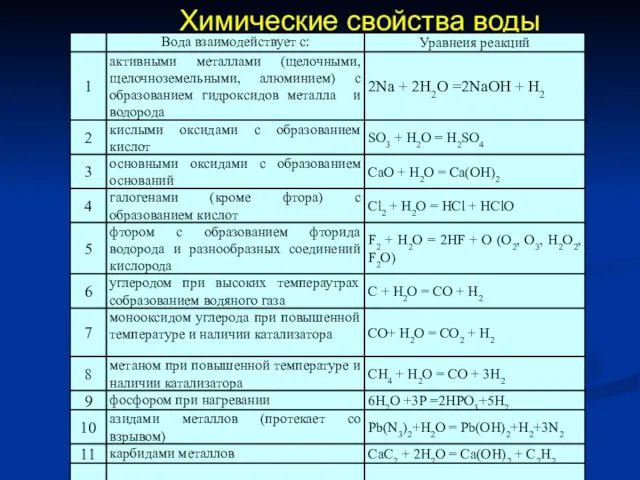
- 22. Химические свойства воды
- 23. Вода обладает рядом достоинств - термической стойкостью; - высокой теплоёмкостью; - высокой теплотой испарения; - относительной
- 24. Отрицательные свойства воды: высокая температура замерзания и аномальное изменение плотности воды при охлаждении, что затрудняет её
- 26. Таблица 9.7 Краткий перечень веществ, для тушения которых нельзя применять воду и водопенные средства
- 27. Характеристика и свойства истинных растворов Учение о растворах: физическая теория Вант-Гоффа, С.Аррениуса и Оствальда, опиралась на
- 28. Термодинамические условия образования растворов Процесс растворения сопровождается различными тепловыми явлениями. Энергетической характеристикой растворения является теплота образования
- 29. Условия образования растворов Если энергия разрушения кристаллической решетки меньше энергии гидратации растворенного вещества, то растворение идет
- 30. Условия образования растворов Процесс растворения сопровождается значительным возрастанием энтропии системы (в результате равномерного распределения частиц одного
- 31. Условия образования растворов При равновесии ∆G = 0. Исключение составляют термодинамически неустойчивые пересыщенные растворы. Термодинамические свойства
- 32. Условия образования растворов Растворение – это сложный физико-химический процесс, при котором происходит взаимодействие (электростатическое, донорно-акцепторное, образование
- 33. Растворы неэлектролитов Если процесс останавливается на стадии образования сольватов, то система представляет собой раствор неэлектролита. Она
- 34. Первый закон Рауля Над поверхностью каждой жидкости всегда присутствует ее пар, образовавшийся в результате эндотермического процесса
- 35. Кипение растворов. Каждое вещество характеризуется строго определенной температурой кипения, то есть переходит из одного агрегатного состояния
- 36. Первый закон Рауля: Относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
- 37. Замерзание растворов Над раствором при температуре кристаллизации (замерзания) растворителя давление насыщенного пара меньше, чем над его
- 38. Разность между температурами кипения раствора и чистого растворителя называют повышением температуры кипения раствора (∆ tкип.). ∆
- 39. Второй закон Рауля Изучая кристаллизацию и кипение растворов, Рауль установил, что для разбавленных растворов неэлектролитов ∆
- 40. Константы Коэффициенты пропорциональности в этих выражениях называют соответственно эбуллиоскопической (от латинского ebullio – выкипаю) (Е) и
- 41. Диффузия Если осторожно слить два раствора различной концентрации, то благодаря тепловому движению молекул концентрации смеси через
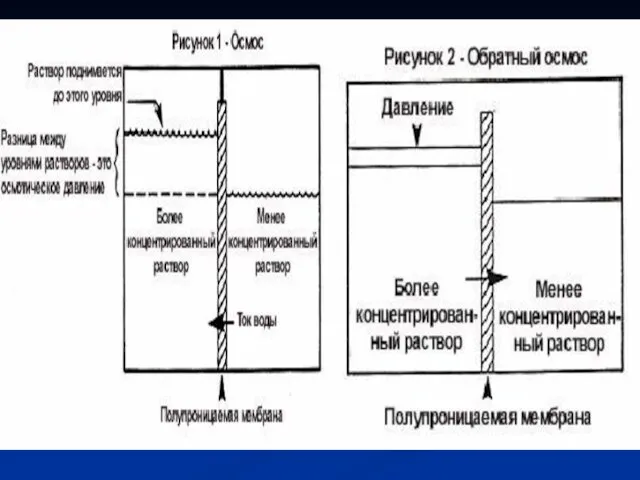
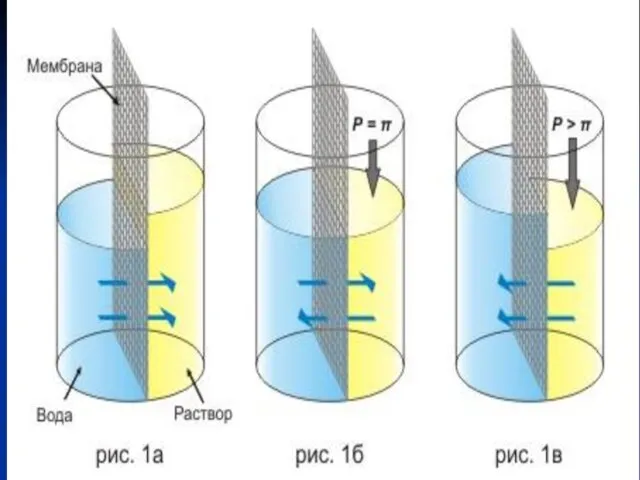
- 42. Осмос. Осмосом называется самопроизвольный процесс проникновения растворителя в раствор, отделенный от него полупроницаемой перегородкой, через которую
- 43. Осмотическое давление. Давление, которое необходимо приложить к раствору, чтобы процесс осмоса прекратился, называется осмотическим давлением. Осмотическое
- 44. Осмотическое давление. Pосм. = RTCм где Росм. - осмотическое давление раствора, кПа; См – его молярность,
- 45. Закон Вант-Гоффа В разбавленных растворах неэлектролитов осмотическое давление численно равно тому давлению, которое производило бы данное
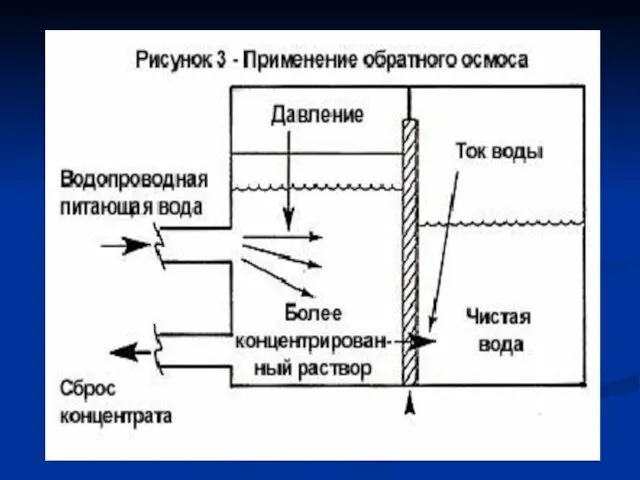
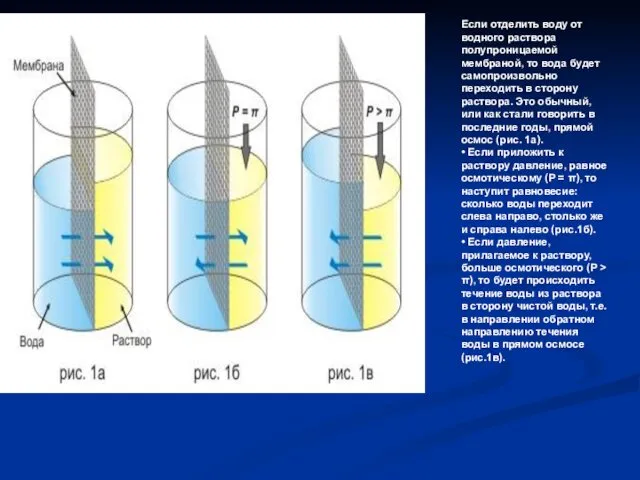
- 49. Если отделить воду от водного раствора полупроницаемой мембраной, то вода будет самопроизвольно переходить в сторону раствора.
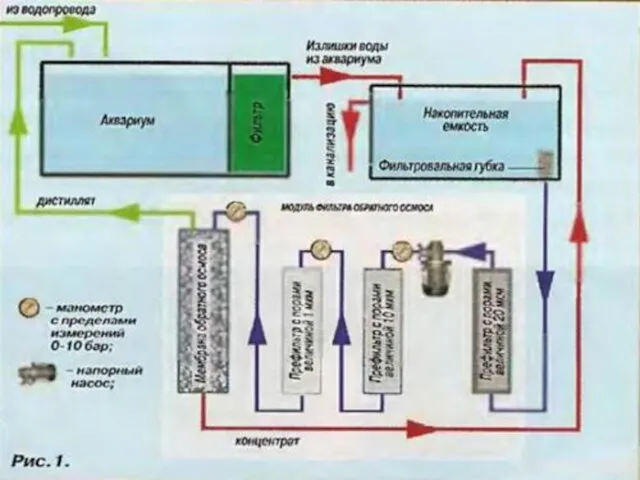
- 50. Бытовые осмотические системы
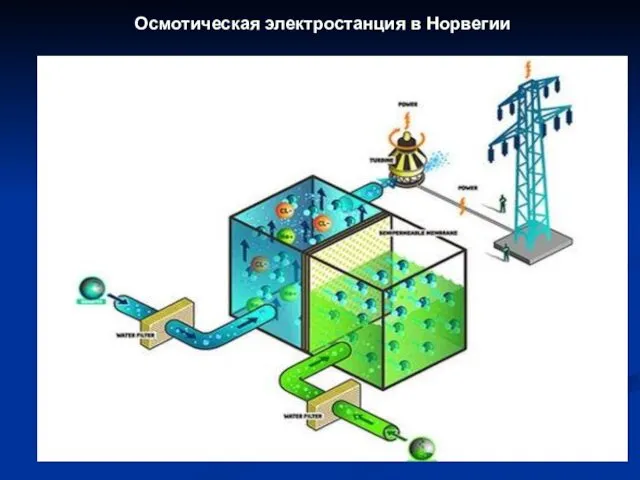
- 51. Осмотическая электростанция в Норвегии
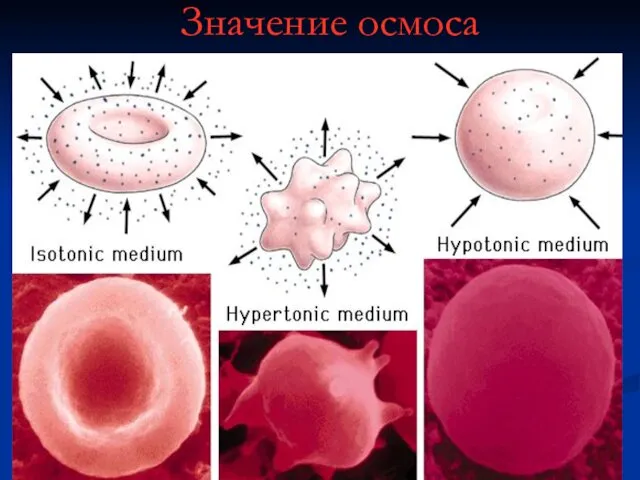
- 54. Значение осмоса
- 56. Скачать презентацию








































 Роль самоподготовки в режиме деятельности группы продлённого дня
Роль самоподготовки в режиме деятельности группы продлённого дня Горные породы, классификация их свойств
Горные породы, классификация их свойств Нелинейные модели парной регрессии
Нелинейные модели парной регрессии Викторина по сказке Г.Х.Андерсена Бузинная матушка
Викторина по сказке Г.Х.Андерсена Бузинная матушка Художественная обработка древесины. Мозаика. 7 класс
Художественная обработка древесины. Мозаика. 7 класс Арифметико-логические устройства, микропроцессоры
Арифметико-логические устройства, микропроцессоры Некоторые приемы работы со сборками. Конструирование сборки сверху вниз
Некоторые приемы работы со сборками. Конструирование сборки сверху вниз презентация ППРС
презентация ППРС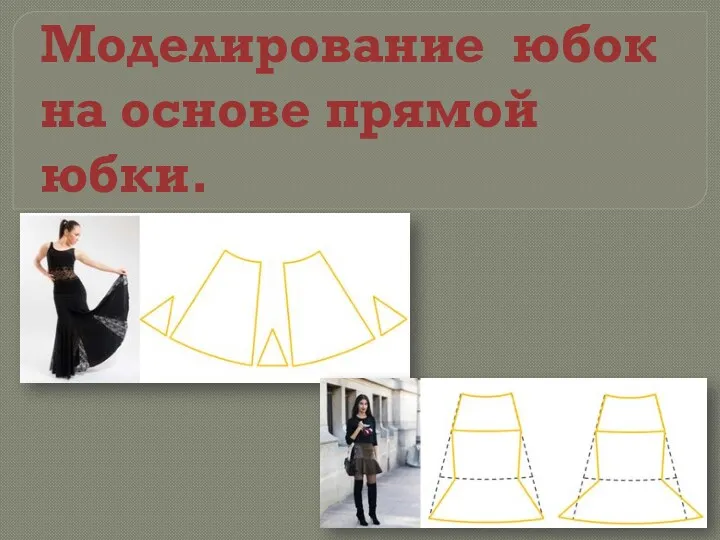 Моделирование юбок на основе прямой юбки
Моделирование юбок на основе прямой юбки Клещевой энцефалит
Клещевой энцефалит Я Научу Тебя Творить
Я Научу Тебя Творить Презентация. Философия. Тема 6. Социальная философия (1)
Презентация. Философия. Тема 6. Социальная философия (1) Угрозы информационной безопасности
Угрозы информационной безопасности Социальная реклама. Разработка социальной кампании по защите окружающей среды от мусора
Социальная реклама. Разработка социальной кампании по защите окружающей среды от мусора Моё хобби
Моё хобби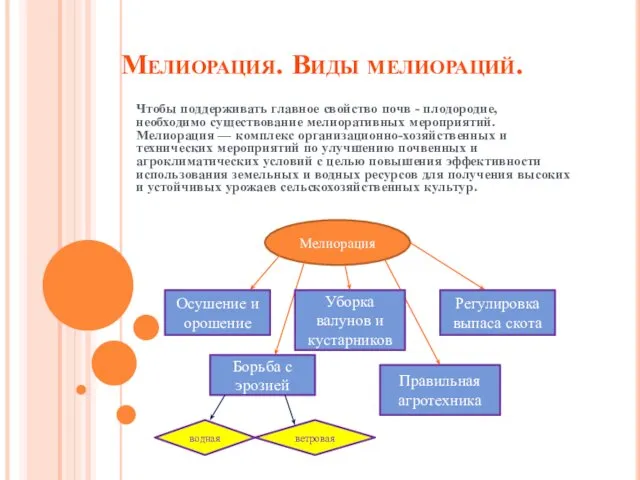 Мелиорация. Виды мелиораций
Мелиорация. Виды мелиораций Авиастроение и авиационный транспорт
Авиастроение и авиационный транспорт Особенности консультирования одаренных детей и подростков
Особенности консультирования одаренных детей и подростков Недвижимость для дальновидных инвесторов
Недвижимость для дальновидных инвесторов Грыжи живота
Грыжи живота Повышение эффективности ТЭУ
Повышение эффективности ТЭУ Игра Архитектурные ансамбли Петербурга
Игра Архитектурные ансамбли Петербурга 20231008_zreloe_i_pozdnee_srednevekove
20231008_zreloe_i_pozdnee_srednevekove Похвальное слово знакам препинания
Похвальное слово знакам препинания Презентация Золотые рыбки в технике оригами
Презентация Золотые рыбки в технике оригами Нотариальное производство. (Лекция 3)
Нотариальное производство. (Лекция 3) Проект строительства житлового комплекса в г. Ялта (2018 г.)
Проект строительства житлового комплекса в г. Ялта (2018 г.) Подготовка к ОГЭ: задача 18 (логика)
Подготовка к ОГЭ: задача 18 (логика)