Содержание
- 3. Реакции: а) гомогенные (отсутствуют границы раздела фаз между реагентами, протекают во всем объеме): 2H2 + O2
- 4. Скорость химической реакции Под скоростью химической реакции понимают число элементарных актов реакции, в результате которых происходит
- 5. Закон действия масс (К. Гульдберг и П. Вааге, 1864 – 1867 г.г.) Скорость химической реакции зависит
- 6. Скорость реакции не зависит от концентрации твердого вещества 2NO(г) + O2(г) = 2NO2(г); V = k∙CNO2
- 7. Молекулярность реакции определяется числом молекул, участвующих в элементарном акте реакции. Мономолекулярная реакция: I2 → 2I Бимолекулярная
- 8. Порядок простой реакции определяется ее молекулярностью. Порядок сложной реакции определяется порядком наиболее медленной стадии. 2HI +
- 9. Примеры решения задач Как изменится скорость прямой реакции 2SO2(г) + O2(г) = 2SO3(г) если уменьшить объем
- 10. Правило Вант Гоффа (влияние температуры на скорость химической реакции) При увеличении температуры на 10° скорость реакции
- 11. Примеры решения задач Скорость некоторой реакции увеличивается в 3 раза при повышении температуры реакционной смеси на
- 12. Уравнение Аррениуса – более точная зависимость скорости реакции от температуры k – константа скорости реакции; А
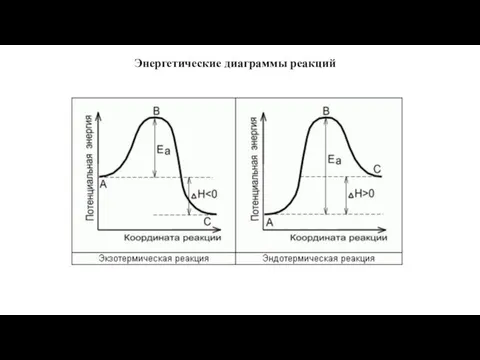
- 13. Энергетические диаграммы реакций
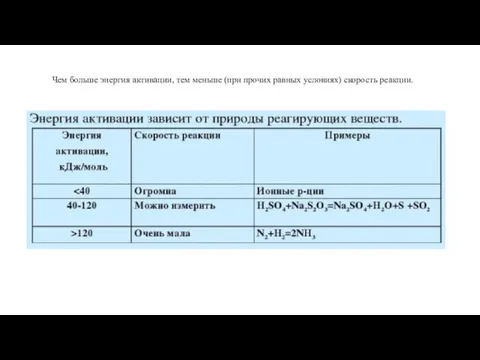
- 14. Чем больше энергия активации, тем меньше (при прочих равных условиях) скорость реакции.
- 16. aA + bB cC + dD v = k1 [A] [B] a b v = k2
- 17. Примеры решения задач В системе 3А + В 2С + D концентрации веществ А, В и
- 18. Примеры решения задач Вычислите равновесные концентрации [NO] и [O2] и константу равновесия реакции если исходные концентрации
- 19. Смещение химического равновесия подчиняется принципу Ле Шателье (принципу противодействия): еcли на систему, находящуюся в состоянии химического
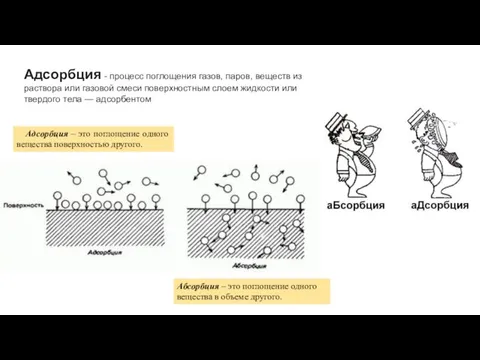
- 21. Адсорбция - процесс поглощения газов, паров, веществ из раствора или газовой смеси поверхностным слоем жидкости или
- 22. Нескомпенсированность сил притяжения и отталкивания молекул вещества на поверхности приводит к возникновению поверхностного натяжения и способности
- 24. Зависимость величины адсорбции от концентрации адсорбата (или давления) при постоянной температуре называется изотермой адсорбции: Г =
- 25. Скорость адсорбции пропорциональна концентрации адсорбата в окружающей среде и количеству свободных мест на поверхности адсорбента (доле
- 26. Г = Гmax⋅ K⋅ [адсорбат] / 1 + K⋅ [адсорбат] В начальный момент адсорбции концентрация адсорбата
- 28. Процесс изменения скорости химической реакции за счет введения в реакционную систему веществ, не входящих в состав
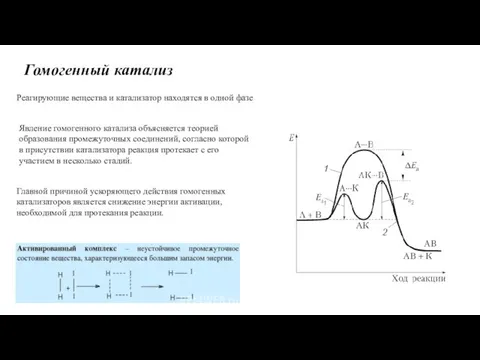
- 29. Гомогенный катализ Реагирующие вещества и катализатор находятся в одной фазе Явление гомогенного катализа объясняется теорией образования
- 30. Гетерогенный катализ Реагирующие вещества и катализатор находятся в различных фазах (как правило, катализатором является твердое вещество,
- 31. Стадии гетерогенной каталитической реакции Диффузия реагентов к внешней поверхности катализатора (внешняя диффузия); 2. Диффузия в порах
- 32. Биологический (ферментативный) катализ – это катализ биохимических реакций с помощью биокатализаторов – ферментов. Присоединение субстрата (S)
- 33. Механизмы катализа Кислотно-основной катализ – в активном центре фермента находятся группы специфичных аминокислотных остатков, которые являются
- 34. 1. Тип "пинг-понг" – фермент сначала взаимодействует с субстратом А, отбирая у него какие либо химические
- 35. Типы ферментативных реакций 2. Тип последовательных реакций – к ферменту последовательно присоединяются субстраты А и В,
- 36. Типы ферментативных реакций 3. Тип случайных взаимодействий – субстраты А и В присоединяются к ферменту в
- 38. Скачать презентацию












![aA + bB cC + dD v = k1 [A]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/49611/slide-15.jpg)

![Примеры решения задач Вычислите равновесные концентрации [NO] и [O2] и](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/49611/slide-17.jpg)






![Г = Гmax⋅ K⋅ [адсорбат] / 1 + K⋅ [адсорбат]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/49611/slide-25.jpg)









 Александр Сергеевич Пушкин
Александр Сергеевич Пушкин Рекомендации для родителей Безопасность вашего ребенка
Рекомендации для родителей Безопасность вашего ребенка Растворы. Гетерогенные равновесия растворов с осадком
Растворы. Гетерогенные равновесия растворов с осадком Россия и страны СНГ
Россия и страны СНГ Проект Нравственно-патриотическое воспитание в ДОУ. Диск
Проект Нравственно-патриотическое воспитание в ДОУ. Диск Цифровое эфирное наземное телевидение
Цифровое эфирное наземное телевидение Организация работы с дошкольниками по ручному труду.
Организация работы с дошкольниками по ручному труду. Потребители и производители, 8 класс
Потребители и производители, 8 класс Галогены: фтор F, хлор Cl, бром Br, иод I, астат At
Галогены: фтор F, хлор Cl, бром Br, иод I, астат At ТЕАТРАЛИЗОВАННАЯ ДЕЯТЕЛЬНОСТЬ В РАЗВИТИИ ДЕТЕЙ ДОШКОЛЬНОНОГО ВОЗРОСТА
ТЕАТРАЛИЗОВАННАЯ ДЕЯТЕЛЬНОСТЬ В РАЗВИТИИ ДЕТЕЙ ДОШКОЛЬНОНОГО ВОЗРОСТА Презентация Устав школы (новая редакция)
Презентация Устав школы (новая редакция) Комплектація та монтаж релейних блочних стативів
Комплектація та монтаж релейних блочних стативів Владимир Иванович Даль
Владимир Иванович Даль Презентация к модульному уроку по теме Соединения галогенов
Презентация к модульному уроку по теме Соединения галогенов Лазерные системы сигнализации на железнодорожных переездах
Лазерные системы сигнализации на железнодорожных переездах Программа Истоки 3класс тема:Любовь
Программа Истоки 3класс тема:Любовь Личность, индивид и индивидуальность. Характер
Личность, индивид и индивидуальность. Характер Введение в экономику
Введение в экономику Орфография в ребусах
Орфография в ребусах 04 (2)
04 (2) Исторические мемы
Исторические мемы Нестероїдні протизапальні засоби
Нестероїдні протизапальні засоби Эпоха позднего Возрождения. Маньеризм
Эпоха позднего Возрождения. Маньеризм Презентация к логопедическому занятию в старшей группе по теме Зима. Зимние забавы.
Презентация к логопедическому занятию в старшей группе по теме Зима. Зимние забавы. Легендарный разведчик Николай Иванович Кузнецов
Легендарный разведчик Николай Иванович Кузнецов Высота. Медиана. Биссектриса
Высота. Медиана. Биссектриса Презентация Трудности адаптации ребенка в 5 классе
Презентация Трудности адаптации ребенка в 5 классе Презентация Как мы провели лето!
Презентация Как мы провели лето!