Содержание
- 2. Алканы
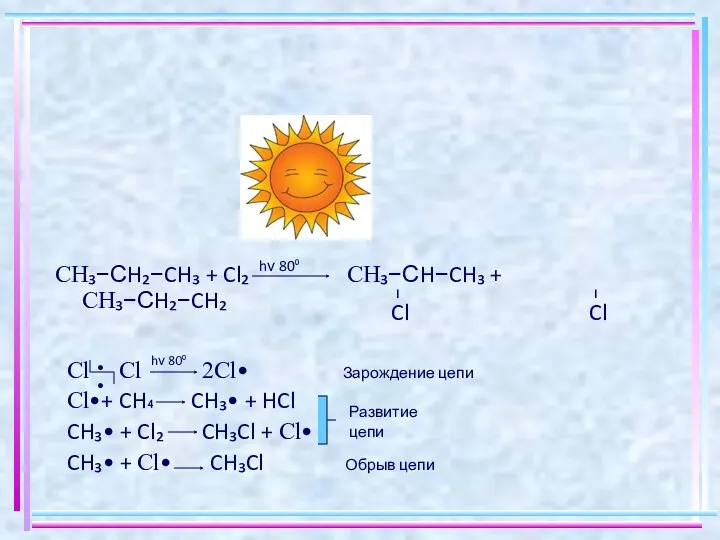
- 3. CH₃−СH₂−CH₃ + Cl₂ CH₃−СH−CH₃ + CH₃−СH₂−CH₂ hν 80⁰ − − Cl Cl Cl Cl 2Cl• Зарождение
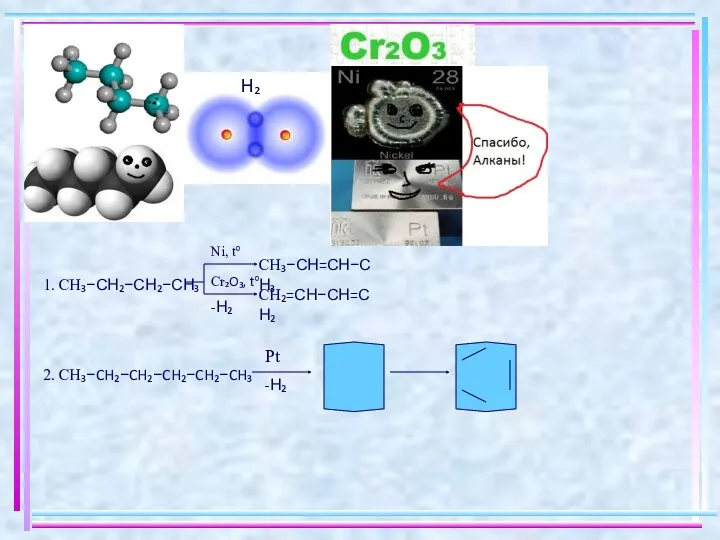
- 4. 1. СН₃−СН₂−СН₂−СН₃ 2. CH₃−CH₂−CH₂−CH₂−CH₂−CH₃ Н₂ Ni, t⁰ СН₃−СН=СН−СН₃ СН₂=СН−СН=СН₂ Cr₂O₃, t⁰ Pt -Н₂ -Н₂
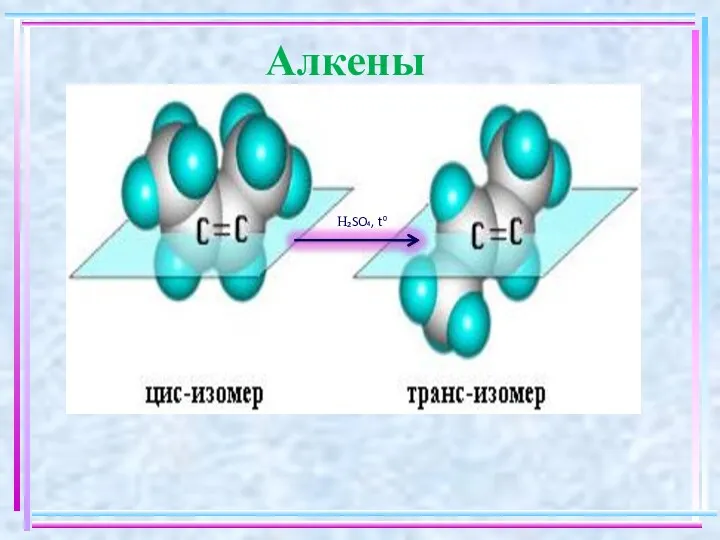
- 5. Алкены ны H₂SO₄, t⁰
- 6. В реакции присоединения полярных молекул к несимметричным алкенам, атом водорода преимущественно присоединяется к наиболее гидрированному атому
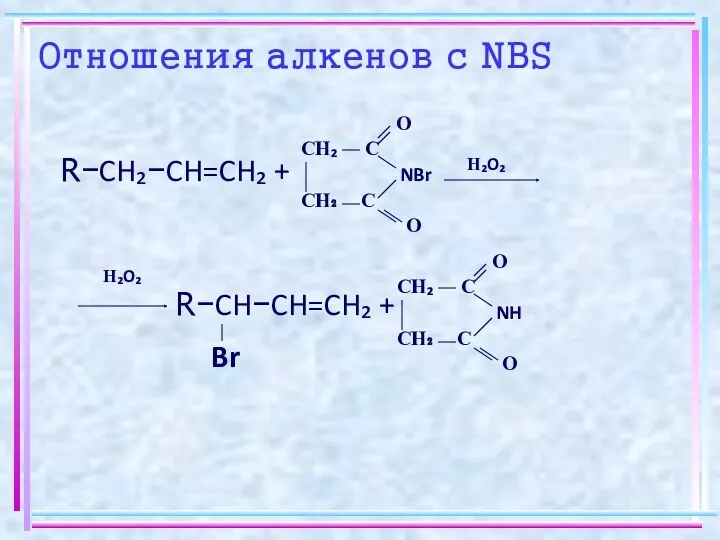
- 7. R−CH₂−CH=CH₂ + R−CH−CH=CH₂ + Отношения алкенов с NBS O CH₂ C NBr CH₂ C O H₂O₂
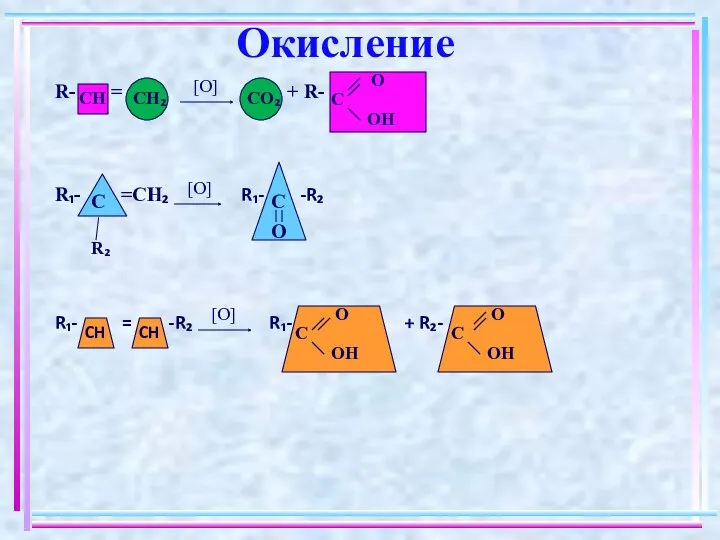
- 8. Окисление R- = + R- R₁- =CH₂ R₁- -R₂ R₁- = -R₂ R₁- + R₂- CH
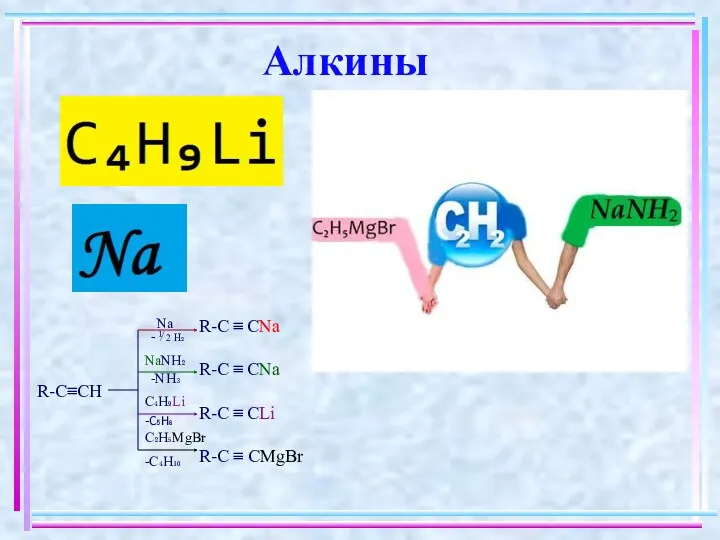
- 9. Алкины R-C ≡ CNa R-C ≡ CNa R-C≡CH R-C ≡ CLi R-C ≡ CMgBr Na -
- 10. Купание в бассейне HgSO₄ O Н−C≡C−H + H2O ⎯→ [HC=CH₂] ⎯→ CH3−C ⏐ H :OH
- 11. Классная дружба 1. Димеризация под действием водного раствора CuCl и NH4Cl: НC≡CH + НC≡CH ⎯→ Н2C=CH−C≡CH
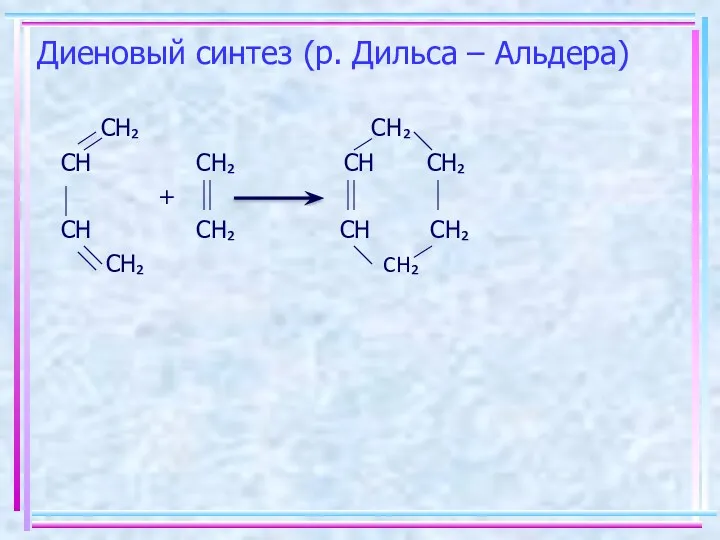
- 12. Диеновый синтез (р. Дильса – Альдера) СH₂ СH₂ СН CH₂ СН CH₂ + СН CH₂ СН
- 13. Событие на мировом уровне CH₂=CH-CH=CH₂ + CH₂=CH-C≡N бутадиен акрилонитрил [ CH₂-CH=CH-CH₂-CH₂-CH ] элементарное звено буна -
- 14. Алкилгалогениды
- 15. SN1 опережает процесс Е1 и берет над ним верх CH₃ CH₃ CH₃-C-OH 80% SN1 CH₃-C- Cl
- 16. SN2 и Е2 конкурируют при помощи катализаторов СH₃-CH₂-CH-CH₃ + CH₃-CH=CH-CH₃ Cl SN2 70% Е2 30% СH₃-CH₂-CH-CH₃
- 17. Спирты [O]
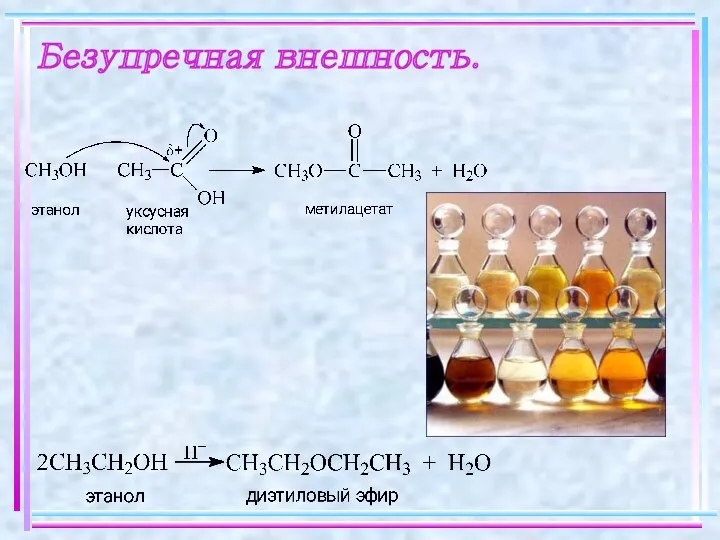
- 18. Безупречная внешность.
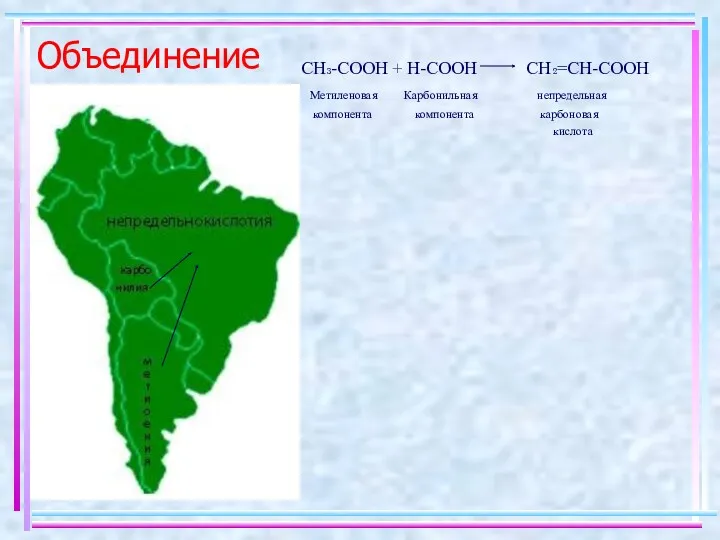
- 19. Объединение CH₃-COOH + H-COOH CH₂=CH-COOH Метиленовая Карбонильная непредельная компонента компонента карбоновая кислота
- 20. Соревнования по армрестлингу
- 21. «Соленый» дуэт R-COOH Na R-COONa
- 22. Каста аминокислот NH2 – CH2 – COOH + НNH – CH2 – COOH → NH2 –
- 23. Детский сад «Аминчик» HNO2 RNH2 R2NH R3N
- 25. Скачать презентацию

![Купание в бассейне HgSO₄ O Н−C≡C−H + H2O ⎯→ [HC=CH₂] ⎯→ CH3−C ⏐ H :OH](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/504028/slide-9.jpg)





![Спирты [O]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/504028/slide-16.jpg)




 Переустройство и перепланировка жилого помещения
Переустройство и перепланировка жилого помещения Планетарные и дифференциальные механизмы
Планетарные и дифференциальные механизмы Концевые меры длины. Гладкие калибры. План изучения инструментов. Назначение инструмента
Концевые меры длины. Гладкие калибры. План изучения инструментов. Назначение инструмента Исследовательский проект Тайны старинной книги
Исследовательский проект Тайны старинной книги Живопись рококо. Мастера галантного жанра (А.Ватто, Ф.Буше, О.Фрагонар)
Живопись рококо. Мастера галантного жанра (А.Ватто, Ф.Буше, О.Фрагонар) Развитие дизайна и его значение в жизни современного общества
Развитие дизайна и его значение в жизни современного общества Делимость произведения
Делимость произведения Трудовые ресурсы России
Трудовые ресурсы России Векторы в пространстве. Компланарные векторы
Векторы в пространстве. Компланарные векторы Демонстрационная лабораторная работа. Микроскопическое строение эпителиальной и соединительной ткани
Демонстрационная лабораторная работа. Микроскопическое строение эпителиальной и соединительной ткани Биология – наука о живых организмах
Биология – наука о живых организмах Измерение информации
Измерение информации Эмбриология. Сердечно-сосудистая система плода
Эмбриология. Сердечно-сосудистая система плода Права и обязанности несовершеннолетних
Права и обязанности несовершеннолетних Принцип действия и режимы работы электрических машин переменного тока
Принцип действия и режимы работы электрических машин переменного тока Медичне страхування, форми і особливості
Медичне страхування, форми і особливості Достижения и основные направления современной селекции и биотехнологии
Достижения и основные направления современной селекции и биотехнологии Алюминий – металл будущего
Алюминий – металл будущего Русский музей
Русский музей Учет основных средств
Учет основных средств Шаблон для презентации Правила дорожного движения
Шаблон для презентации Правила дорожного движения Сельский зеленый туризм в Италии
Сельский зеленый туризм в Италии Город Ладога
Город Ладога Агрегаты для обработки почвы
Агрегаты для обработки почвы Трагедия Хатыни
Трагедия Хатыни Маленькие герои - большой войны
Маленькие герои - большой войны Синхронные генераторы
Синхронные генераторы Презентация ко Дню Победы
Презентация ко Дню Победы