Слайд 2

Нитриды. Классификация
солеобразные
нитриды щелочных и щелочноземельных металлов
легко гидролизуются водой
ковалентные
нитриды Si, C, P
и др.
алмазоподобные
нитриды элементов IIIa (13) группы
изоэлектронны алмазу
металлоподобные (нитриды внедрения)
нитриды переходных металлов
высокие температуры плавления, твердые, химически инертные, часто – проводники и полупроводники, имеют переменный состав
Слайд 3

Нитриды. Получение
Нитриды металлов
Прямая реакция металла с азотом
Реакция металла с аммиаком
Разложение амидов
Взаимодействие
аммиака с оксидами и галогенидами
Восстановление оксидов и галогенидов в присутствии азота
Термическая диссоциация соединений, содержащих металл и азот
Нитриды неметаллов
Мягкое окисление цианид-ионов ионами Cu2+
Окисление цианидов кислородом или хлором
Взаимодействие с жидким аммиаком
Слайд 4

Слайд 5
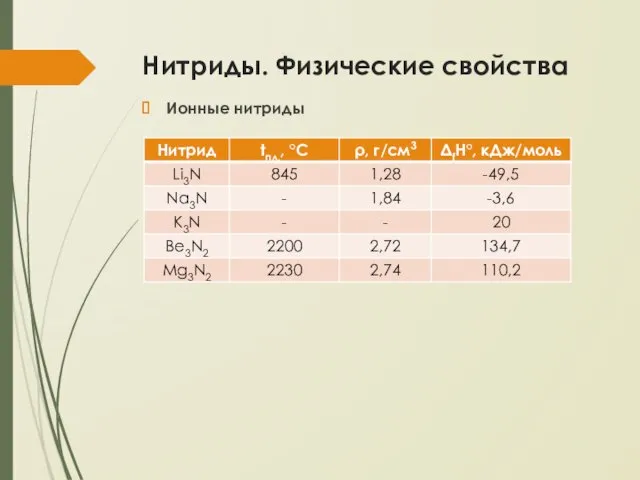
Нитриды. Физические свойства
Ионные нитриды
Слайд 6
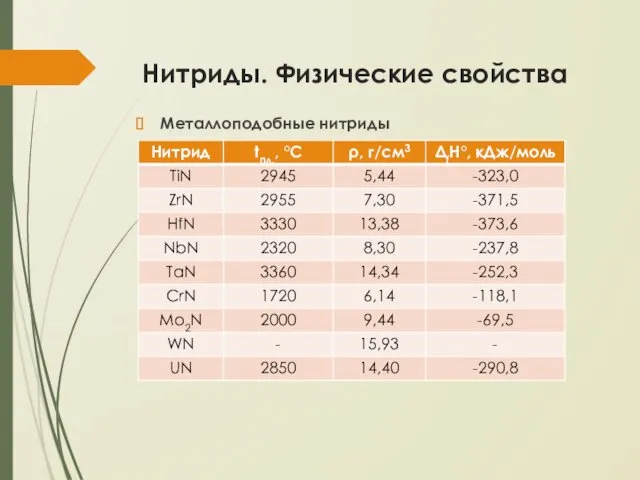
Нитриды. Физические свойства
Металлоподобные нитриды
Слайд 7

Нитриды. Химические свойства
Гидролиз
Взаимодействие с кислотами
Окисление при нагревании на воздухе
Металлоподобные нитриды разлагаются
с образованием низших нитридов
Слайд 8

Слайд 9

Литература
Гринвуд Н., Эрншо А. Химия элементов. Том 1, М.: Бином, 2008
Самсонов
Г. В. Нитриды, Киев: Наукова думка, 1969
Слайд 10
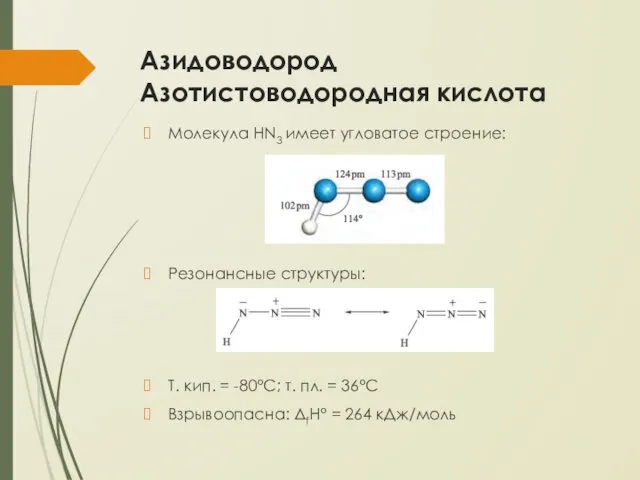
Азидоводород Азотистоводородная кислота
Молекула HN3 имеет угловатое строение:
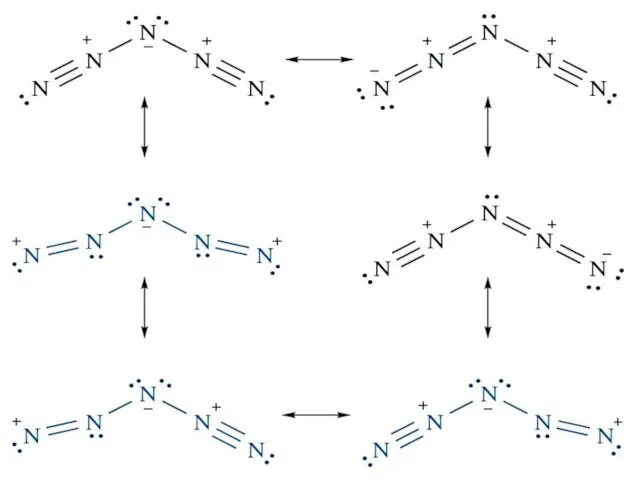
Резонансные структуры:
Т. кип. = -80°С;
т. пл. = 36°С
Взрывоопасна: ΔfH° = 264 кДж/моль
Слайд 11

Азидоводород. Получение
Из азидов щелочных металлов
Взаимодействие гидразина с азотистой кислотой
Нагревание амидов ЩМ
в токе оксида азота (I)
Слайд 12

Азидоводород.
Химические свойства
В растворе медленно разлагается
Взрывается при нагревании
Окислительные свойства, связанные с
ионом [N3]-
Взаимодействие с металлами и их соединениями
Реакции комплексообразования
Слайд 13
Слайд 14
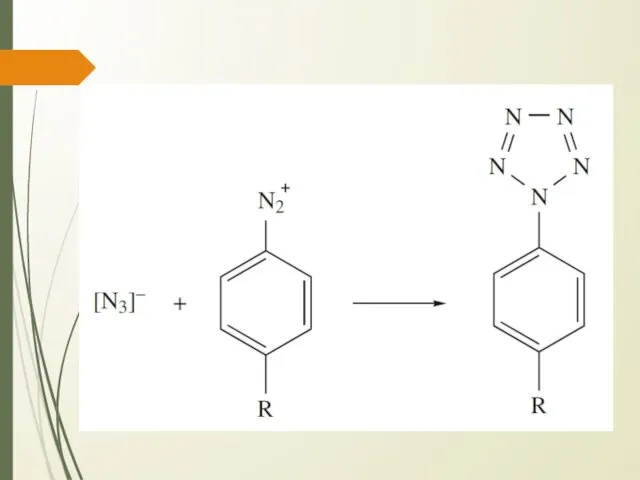
Слайд 15

Слайд 16

Литература
Гринвуд Н., Эрншо А. Химия элементов. Том 1, М.: Бином, 2008
Housecroft
C. E., Sharpe A. G. Inorganic Chemistry, 2-nd ed, Edinburg: Pearson Education Limited, 2005
Patnaik P. Handbook of inorganic chemicals, NY: McGraw-Hill, 2002
Слайд 17

Гидразин и его гомологи
Гидразин – N2H4 – дымящая бесцветная жидкость с
резким запахом аммиака
Триазан – N3H5 – нестабильно, существует в виде солей
Тетразан – N4H6 – ярко-желтое твердое вещество
Слайд 18
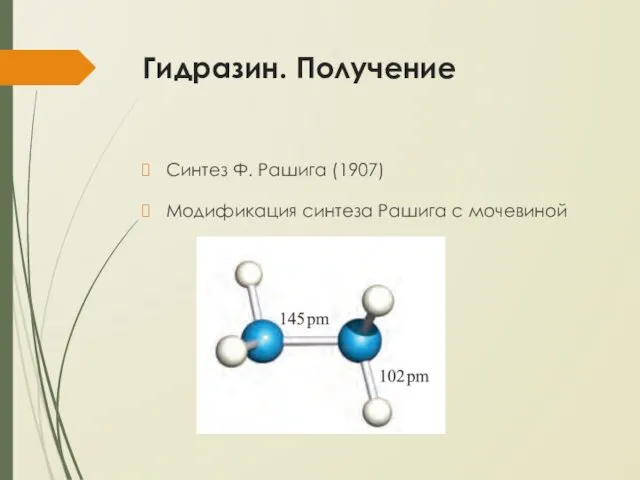
Гидразин. Получение
Синтез Ф. Рашига (1907)
Модификация синтеза Рашига с мочевиной
Слайд 19

Гидразин. Физические свойства
0
100
0,99701
0,8903
1,3330
78,39
5,7·10-8
-285,85
-237,19
70,1
Слайд 20

Гидразин. Химические свойства
Горение на воздухе
Окисление галогенами, кислородом и пероксидом водорода
Окисление иодатами
(количественное определение)
Основные свойства
Слайд 21
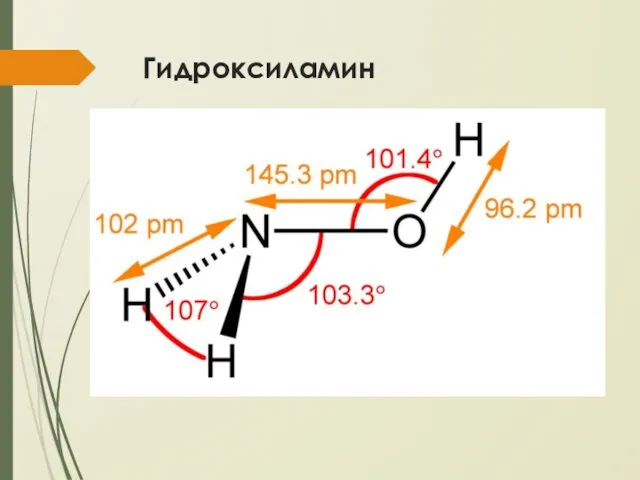
Гидроксиламин
NH2OH – бесцветное термически неустойчивое гигроскопичное соединение с т. пл. 32,05°С
Слабое
основание К = 6,6·10-9
Получается восстановлением нитрита аммония сернистым газом при 0°С
В лаборатории получают восстановлением азотистой кислоты бисульфитом
При температуре выше комнатной может бурно разлагаться с образованием смеси N2, NH3, N2O, H2O
Слайд 22
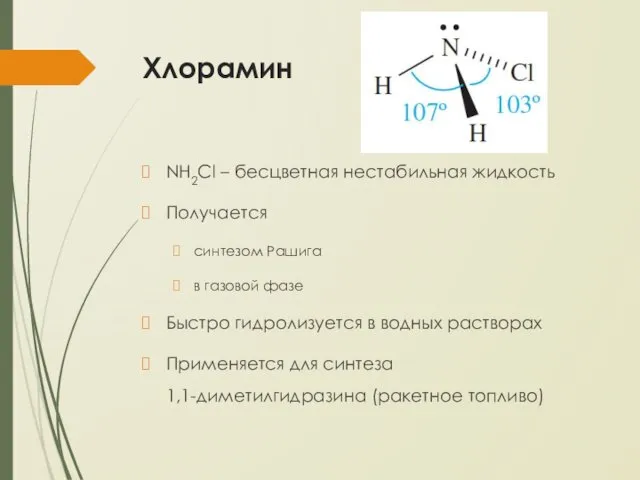
Хлорамин
NH2Cl – бесцветная нестабильная жидкость
Получается
синтезом Рашига
в газовой фазе
Быстро гидролизуется в
водных растворах
Применяется для синтеза 1,1-диметилгидразина (ракетное топливо)
Слайд 23
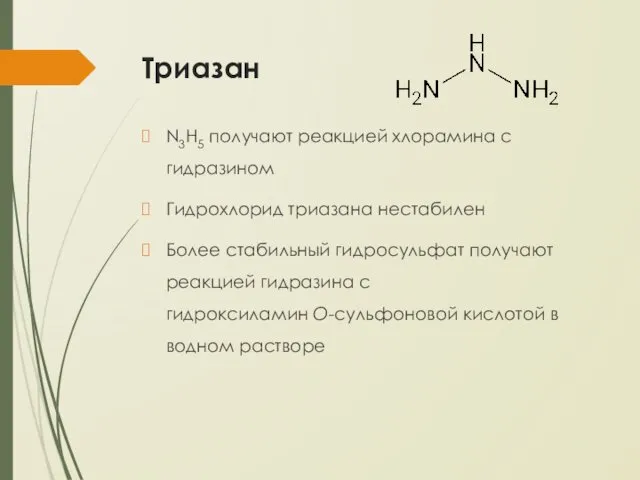
Триазан
N3H5 получают реакцией хлорамина с гидразином
Гидрохлорид триазана нестабилен
Более стабильный гидросульфат получают
реакцией гидразина с гидроксиламин О-сульфоновой кислотой в водном растворе
Слайд 24
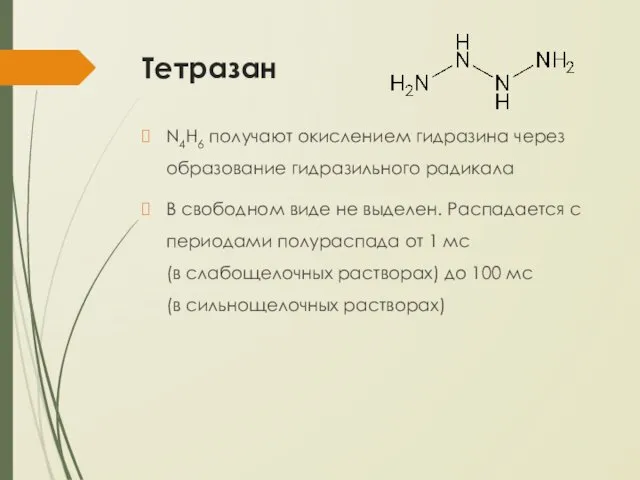
Тетразан
N4H6 получают окислением гидразина через образование гидразильного радикала
В свободном виде не
выделен. Распадается с периодами полураспада от 1 мс (в слабощелочных растворах) до 100 мс (в сильнощелочных растворах)
Слайд 25
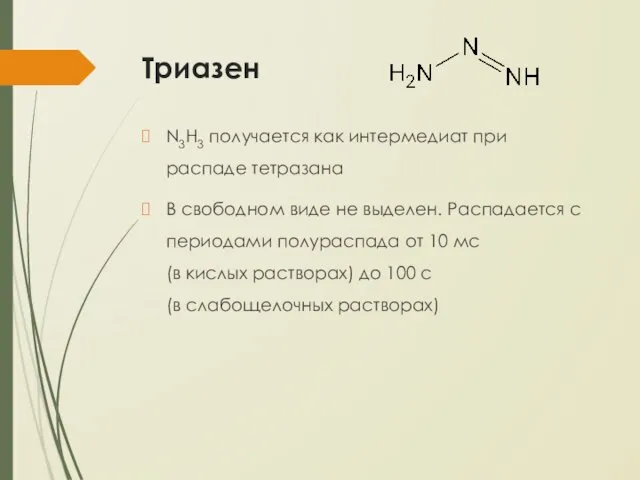
Триазен
N3H3 получается как интермедиат при распаде тетразана
В свободном виде не выделен.
Распадается с периодами полураспада от 10 мс (в кислых растворах) до 100 с (в слабощелочных растворах)
Слайд 26

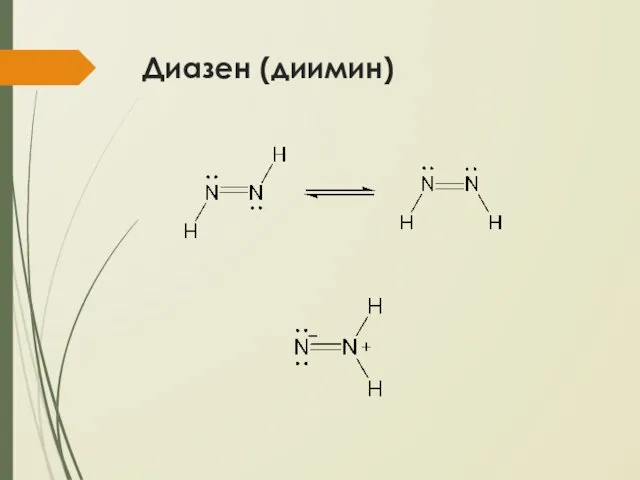
Диазен (диимин)
N2H2 – нестабильное твердое вещество светло-желтого цвета
Получают дегидрированием гидразина
Лабораторный синтез
- из производных гидразина
Хранится в жидком аммиаке при температуре жидкого азота (-196°С)
Разлагается с образованием азота и гидразина
Слайд 27
Слайд 28

Литература
Гринвуд Н., Эрншо А. Химия элементов. Том 1, М.: Бином, 2008
Housecroft
C. E., Sharpe A. G. Inorganic Chemistry, 2-nd ed, Edinburg: Pearson Education Limited, 2005
Wiberg E., Wiberg N. Inorganic Chemistry, Academic Press, 2001
Слайд 29

Кислоты
Азотистая
Азотная
Азотноватистая H2N2O2
Азотноватая H2N2O3
Пероксоазотная кислота HNO4
Ортоазотная кислота {H3NO4}
Слайд 30
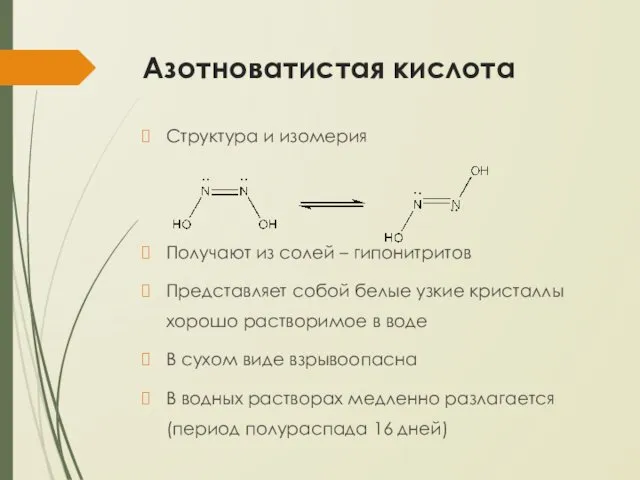
Азотноватистая кислота
Структура и изомерия
Получают из солей – гипонитритов
Представляет собой белые узкие
кристаллы хорошо растворимое в воде
В сухом виде взрывоопасна
В водных растворах медленно разлагается (период полураспада 16 дней)
Слайд 31

Азотноватая кислота
Получают из соли Анджели
Относится к кислотам средней силы
Образует нерастворимые соли
(оксогипонитриты) со ЩЗМ и тяжелыми металлами
Легко окисляется кислородом воздуха
Разлагается при хранении (катализатор – нитриты)
Слайд 32

Ортоазотная кислота
Не получена ни в каком виде
Известны ее соли – ортонитраты
Ортонитраты
синтезируют из нитратов
Во влажном воздухе быстро гидролизуются
Слайд 33

Литература
Гринвуд Н., Эрншо А. Химия элементов. Том 1, М.: Бином, 2008
Wiberg
E., Wiberg N. Inorganic Chemistry, Academic Press, 2001
































 Алексе́й Гаври́лович Венециа́нов
Алексе́й Гаври́лович Венециа́нов Фотокросс. Путешествие зеленых по Европе
Фотокросс. Путешествие зеленых по Европе Национальный центр образовательной статистики и оценки PISA-2012: читательская грамотность
Национальный центр образовательной статистики и оценки PISA-2012: читательская грамотность Глобальные проблемы человечества
Глобальные проблемы человечества Презентация Оснащение логопедического уголка в группах детского сада
Презентация Оснащение логопедического уголка в группах детского сада Цветное настроение
Цветное настроение Колыбельная песня – первая песня в жизни человека
Колыбельная песня – первая песня в жизни человека Власть в городе территориальном и архитектурном измерении
Власть в городе территориальном и архитектурном измерении История русского театра
История русского театра Профессиональный тип личности
Профессиональный тип личности Молодежный форум. Барановичи – молодежная столица Республики Беларусь
Молодежный форум. Барановичи – молодежная столица Республики Беларусь Малые государства древнего Востока
Малые государства древнего Востока Портфолио для аттестации
Портфолио для аттестации Полевые методы изучения горных пород и их взаимоотношений
Полевые методы изучения горных пород и их взаимоотношений Классы неорганических соединений
Классы неорганических соединений Игры по ознакомлению детей младшего дошкольного возраста с предметными миром
Игры по ознакомлению детей младшего дошкольного возраста с предметными миром Реконструкция и реставрация исторического дворца методом торкретирования
Реконструкция и реставрация исторического дворца методом торкретирования Путешествие по Тулате
Путешествие по Тулате Кто хочет стать миллионером
Кто хочет стать миллионером Презентация Портфолио
Презентация Портфолио Святая Пасха
Святая Пасха Презентация к уроку Высотная поясность
Презентация к уроку Высотная поясность Конфликт и его причины
Конфликт и его причины Эпидемическое вирусное заболевание краснуха
Эпидемическое вирусное заболевание краснуха Год Российской истории в школе
Год Российской истории в школе Презентация к логопедическому занятию в старшей группе Звук Б
Презентация к логопедическому занятию в старшей группе Звук Б Программа Капельки по музыкальному развитию (вокал)
Программа Капельки по музыкальному развитию (вокал) Биржевая торговля. Понятие организованного рынка
Биржевая торговля. Понятие организованного рынка