Содержание
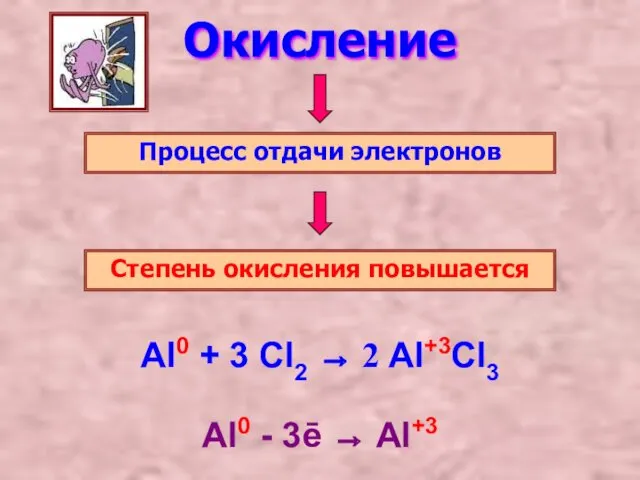
- 2. Окисление Процесс отдачи электронов Степень окисления повышается Al0 - 3ē → Al+3 Al0 + 3 Cl2
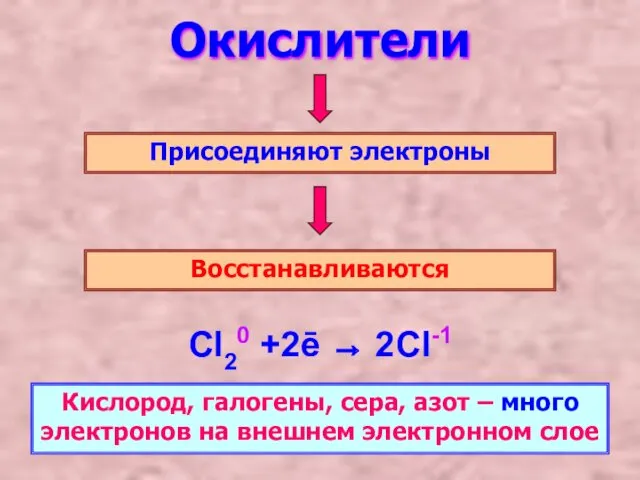
- 3. Окислители Присоединяют электроны Восстанавливаются Cl20 +2ē → 2Cl-1 Кислород, галогены, сера, азот – много электронов на
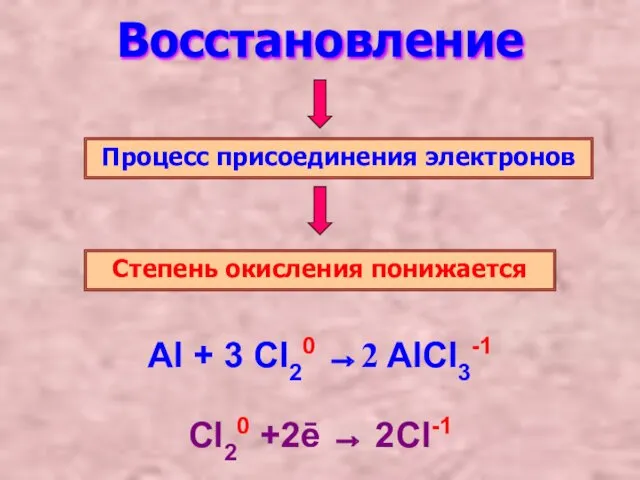
- 4. Восстановление Процесс присоединения электронов Степень окисления понижается Al + 3 Cl20 →2 AlCl3-1 Cl20 +2ē →
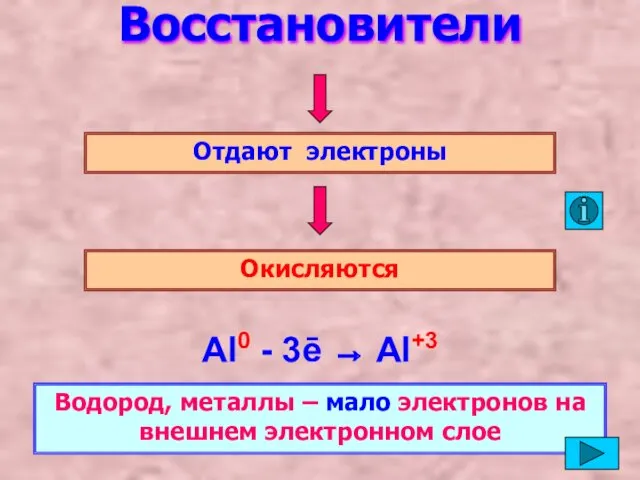
- 5. Восстановители Отдают электроны Окисляются Al0 - 3ē → Al+3 Водород, металлы – мало электронов на внешнем
- 7. ОВР – окислительно-восстановительные реакции Реакции в которых происходит изменение степени окисления Zn0 + 2H+1 Cl →
- 8. Окислитель восстанавливается, его степень окисления уменьшается Восстановитель окисляется, его степень окисления увеличивается 2 Na0 + Cl2
- 9. Положительный Восстановился
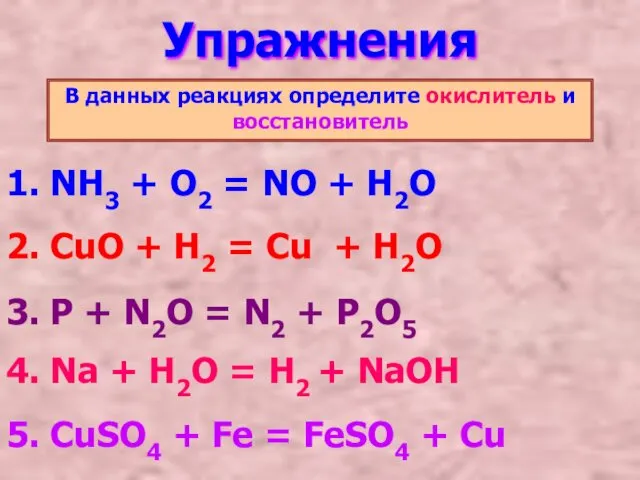
- 10. Упражнения В данных реакциях определите окислитель и восстановитель 1. NH3 + O2 = NO + H2O
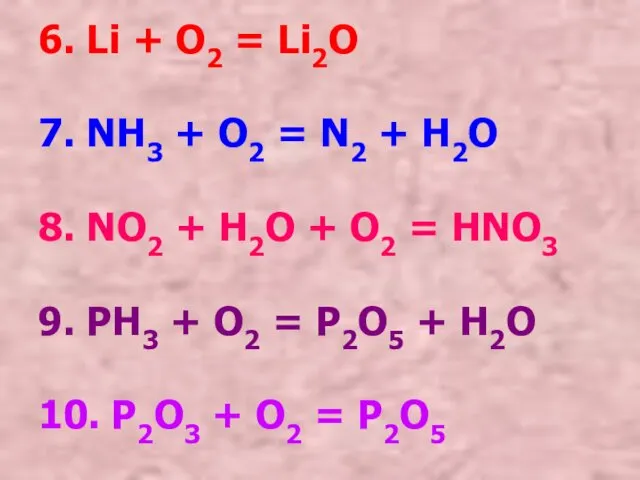
- 11. 6. Li + O2 = Li2O 7. NH3 + O2 = N2 + H2O 8. NO2
- 13. Скачать презентацию


 Мир растений. Лекарственные растения
Мир растений. Лекарственные растения Пости централізації, кросовий монтаж і технічне обслуговування станційних пристроїв
Пости централізації, кросовий монтаж і технічне обслуговування станційних пристроїв Салық – мемлекеттік бюджетке заңды және жеке тұлғалардан белгілі бір мөлшерде түсетін міндетті
Салық – мемлекеттік бюджетке заңды және жеке тұлғалардан белгілі бір мөлшерде түсетін міндетті Технология ручной дуговой сварки неплавящимся электродом в защитном газе углеродистых сталей, цветных металлов и их сплавов
Технология ручной дуговой сварки неплавящимся электродом в защитном газе углеродистых сталей, цветных металлов и их сплавов Презентация:Использования ИКТ для формирования открытого информационного пространства ДОУ
Презентация:Использования ИКТ для формирования открытого информационного пространства ДОУ Залог успешной работы– это благоприятный психологический климат в классе
Залог успешной работы– это благоприятный психологический климат в классе ФГОС как система обязательных требований.
ФГОС как система обязательных требований. Внутрипартийная борьба в 20-е годы ХХ века в России
Внутрипартийная борьба в 20-е годы ХХ века в России Использование проектной технологии в обучении географии
Использование проектной технологии в обучении географии Праздник праздников, торжество из торжеств
Праздник праздников, торжество из торжеств Автоматизация звука [Р] в середине слова (стечение согласных)
Автоматизация звука [Р] в середине слова (стечение согласных) Бесполое размножение организмов
Бесполое размножение организмов Контрастность изображения
Контрастность изображения Анализ деятельности МОУДОД ЦДТ Созвездие (презентация)
Анализ деятельности МОУДОД ЦДТ Созвездие (презентация) Признаки делимости на 2, 5, 10
Признаки делимости на 2, 5, 10 Город сквозь времена и страны
Город сквозь времена и страны Эхокардиография
Эхокардиография презентация
презентация Запись на программу персонифицированного дополнительного образования
Запись на программу персонифицированного дополнительного образования Проведение дезинфекции в образовательной организации
Проведение дезинфекции в образовательной организации ОБЖ в условиях лета
ОБЖ в условиях лета Презентация Развитие речи Вашего малыша
Презентация Развитие речи Вашего малыша Электронное портфолио педагога-организатора
Электронное портфолио педагога-организатора Использование деятельностного подхода в ОД при формировании ОБЖ
Использование деятельностного подхода в ОД при формировании ОБЖ Тұздау, ашыту және маринадтау әдістері
Тұздау, ашыту және маринадтау әдістері Графика системы matlab. (Лекция 2)
Графика системы matlab. (Лекция 2) diplom (3)
diplom (3) ООПТ Ульяновской области
ООПТ Ульяновской области