- Главная
- Без категории
- оксиды

Содержание
- 2. Оксиды – это сложные вещества, состоящие из двух элементов, один из которых кислород.
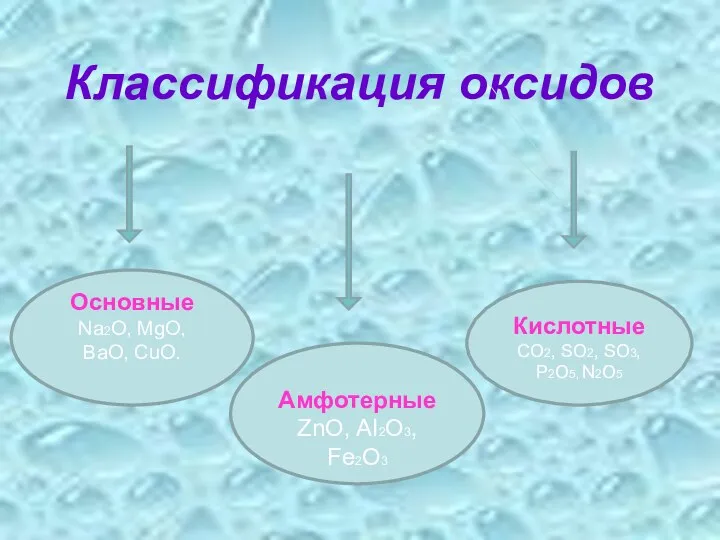
- 3. Классификация оксидов Амфотерные ZnO, AI2О3, Fe2О3 Кислотные CO2, SО2, SО3, P2О5, N2О5 Основные Na2O, MgО, BaO,
- 4. Типичные реакции оксидов Основной оксид + вода = основание CaО + H2O = Ca(ОH)2 Li2О +
- 5. ПРОВЕРЬ СЕБЯ 1.Формула кислотного оксида - это: а) NaOH в) CuCL2 б) HCL г) SO3 2.
- 7. Скачать презентацию
Слайд 2
Оксиды – это сложные вещества, состоящие из двух элементов, один из
Оксиды – это сложные вещества, состоящие из двух элементов, один из
которых кислород.
Слайд 3
Классификация оксидов
Амфотерные
ZnO, AI2О3,
Fe2О3
Кислотные
CO2, SО2, SО3,
P2О5, N2О5
Основные
Na2O, MgО,
BaO, CuО.
Классификация оксидов
Амфотерные
ZnO, AI2О3,
Fe2О3
Кислотные
CO2, SО2, SО3,
P2О5, N2О5
Основные
Na2O, MgО,
BaO, CuО.
Слайд 4
Типичные реакции оксидов
Основной оксид + вода = основание
CaО + H2O
Типичные реакции оксидов
Основной оксид + вода = основание
CaО + H2O
= Ca(ОH)2
Li2О + H2O = 2LiОH
Кислота + основной оксид = соль + вода
CuO + 2 HCL = CuCL2 + H2O
CuO + 2H+ = H2O + Cu2+
Основной оксид + кислотный оксид = соль
CaО + CО2 = CaCO3
3CaО + P2О5 = Ca3(PO4)2
Кислотный оксид + вода = кислота
CО2 + Н2О = Н2СО3
P2О5 + 3Н2О = 2Н3РО4
Кислотный оксид + основание = соль + вода
СО2 + 2NaОH = Na2CО3 + H2О
P2О5 + 6NaОH = 2Na3РО4 + 3H2О
Li2О + H2O = 2LiОH
Кислота + основной оксид = соль + вода
CuO + 2 HCL = CuCL2 + H2O
CuO + 2H+ = H2O + Cu2+
Основной оксид + кислотный оксид = соль
CaО + CО2 = CaCO3
3CaО + P2О5 = Ca3(PO4)2
Кислотный оксид + вода = кислота
CО2 + Н2О = Н2СО3
P2О5 + 3Н2О = 2Н3РО4
Кислотный оксид + основание = соль + вода
СО2 + 2NaОH = Na2CО3 + H2О
P2О5 + 6NaОH = 2Na3РО4 + 3H2О
Слайд 5
ПРОВЕРЬ СЕБЯ
1.Формула кислотного оксида - это:
а) NaOH в) CuCL2
б)
ПРОВЕРЬ СЕБЯ
1.Формула кислотного оксида - это:
а) NaOH в) CuCL2
б)
HCL г) SO3
2. Лакмус в растворе, полученном при взаимодействии оксида серы (IV) с водой:
а) синий в) фиолетовый
б) красный г) малиновый
3. Оксид углерода ( IV) взаимодействует с:
а) оксид магния в) оксид фосфора
б) оксид углерода г) сера
4. Оксид кремния (IV) не взаимодействует с :
а) алюминием в) водой
б) железом г) цинком
5. Формула основного оксида – это:
а) CO2 в) Р2О5
б) ВаО г) N2О5
6. Пара веществ не взаимодействующих друг с другом:
а) H2SO4 u SiO2 в) СаО u СO2
б) CO2 u Na2O г) Са(ОН)2 u CO2
2. Лакмус в растворе, полученном при взаимодействии оксида серы (IV) с водой:
а) синий в) фиолетовый
б) красный г) малиновый
3. Оксид углерода ( IV) взаимодействует с:
а) оксид магния в) оксид фосфора
б) оксид углерода г) сера
4. Оксид кремния (IV) не взаимодействует с :
а) алюминием в) водой
б) железом г) цинком
5. Формула основного оксида – это:
а) CO2 в) Р2О5
б) ВаО г) N2О5
6. Пара веществ не взаимодействующих друг с другом:
а) H2SO4 u SiO2 в) СаО u СO2
б) CO2 u Na2O г) Са(ОН)2 u CO2



 Культы. Как распознать
Культы. Как распознать Трудности адаптации пятиклассников.
Трудности адаптации пятиклассников. Глобальные проблемы человечества и пути их решения. Экологическая проблема
Глобальные проблемы человечества и пути их решения. Экологическая проблема Великобритания: культура и искусство. Элективный курс. 9-й класс.
Великобритания: культура и искусство. Элективный курс. 9-й класс. Особенности политического развития в мире
Особенности политического развития в мире Родительское собрание (1 класс)Трудности обучения письму и чтению в начальной школе.
Родительское собрание (1 класс)Трудности обучения письму и чтению в начальной школе. Химические свойства металлов
Химические свойства металлов о.ю
о.ю Слова с суффиксом -ость. Сопоставление пар слов с противоположным значением.
Слова с суффиксом -ость. Сопоставление пар слов с противоположным значением. Фруктовая и овощная батарейка
Фруктовая и овощная батарейка Притча Задача учителя
Притча Задача учителя Эмоции и чувства человека и животных
Эмоции и чувства человека и животных олимпиада по олимпийским играм
олимпиада по олимпийским играм Угольная промышленность России
Угольная промышленность России Варгашинский район на карте Курганской области
Варгашинский район на карте Курганской области Покрытосеменные, или цветковые растения. (Часть 2)
Покрытосеменные, или цветковые растения. (Часть 2) Федеральный стандарт оценки ФСО-9. Оценка для целей залога
Федеральный стандарт оценки ФСО-9. Оценка для целей залога Электронное портфолио
Электронное портфолио Социальная проблема - игромания
Социальная проблема - игромания Образование первых государств
Образование первых государств Давлат умумий ўрта таълим муассасалари ўқувчиларини замонавий ягона мактаб формаси билан таъминлаш
Давлат умумий ўрта таълим муассасалари ўқувчиларини замонавий ягона мактаб формаси билан таъминлаш Родительское собрание Учим детей мыслить
Родительское собрание Учим детей мыслить 2_5325665765213361055
2_5325665765213361055 Сальвадор Дали
Сальвадор Дали Arany nagykőrösi ballada korszaka
Arany nagykőrösi ballada korszaka Строительные машины для земляных работ
Строительные машины для земляных работ Высказывания со словами есть, существует, некоторые.
Высказывания со словами есть, существует, некоторые. Psychophysik Hören
Psychophysik Hören