Олефиновые углеводороды как сырье для органического синтеза. Реакции олефинов. Способы производства олефинов. Лекция 4 презентация
Содержание
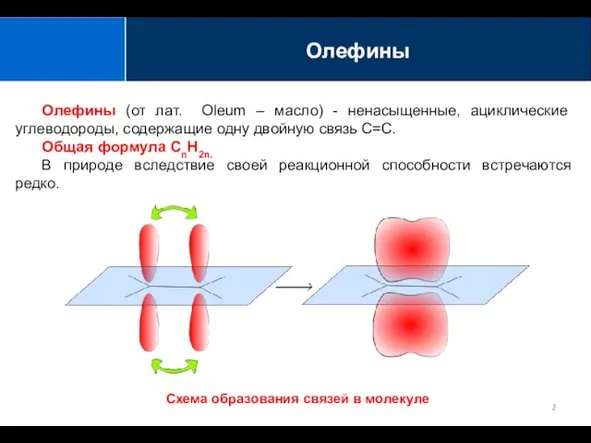
- 2. Олефины (от лат. Oleum – масло) - ненасыщенные, ациклические углеводороды, содержащие одну двойную связь С=С. Общая
- 3. Низшие олефины (C2-C5) С2-С4 – газы, С5Н10 - жидкость Этилен С2Н4 сжижается при низких температурах и
- 4. УГНТУ
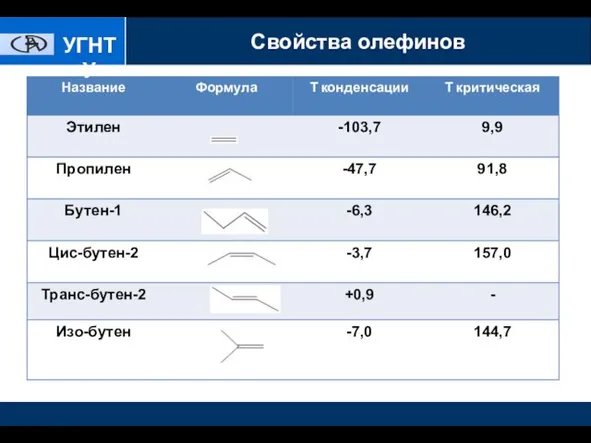
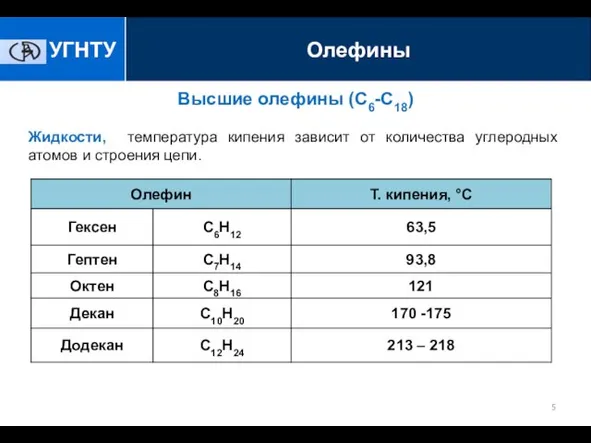
- 5. Высшие олефины (С6-С18) Жидкости, температура кипения зависит от количества углеродных атомов и строения цепи.
- 6. Из олефинов по масштабам потребления: Этилен > пропилен > бутилен УГНТУ
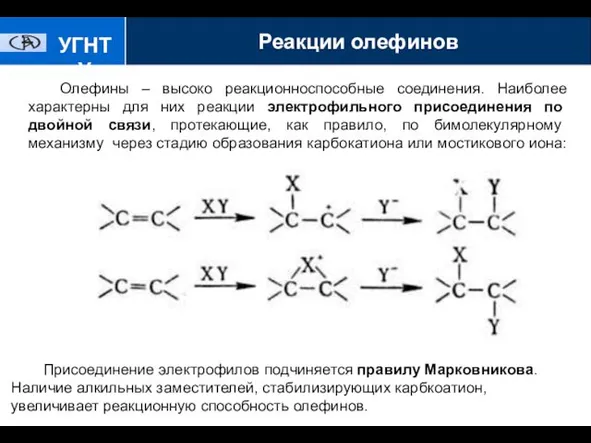
- 7. УГНТУ Олефины – высоко реакционноспособные соединения. Наиболее характерны для них реакции электрофильного присоединения по двойной связи,
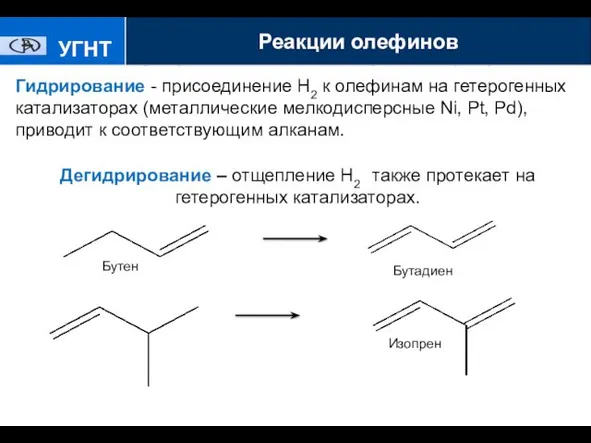
- 8. Хлорирование и гидрохлорир УГНТУ Гидрирование - присоединение Н2 к олефинам на гетерогенных катализаторах (металлические мелкодисперсные Ni,
- 9. Изопрен наиболее часто встречающийся углеводород находящийся в теле человека. Оценочная скорость производства изопрена в теле человека
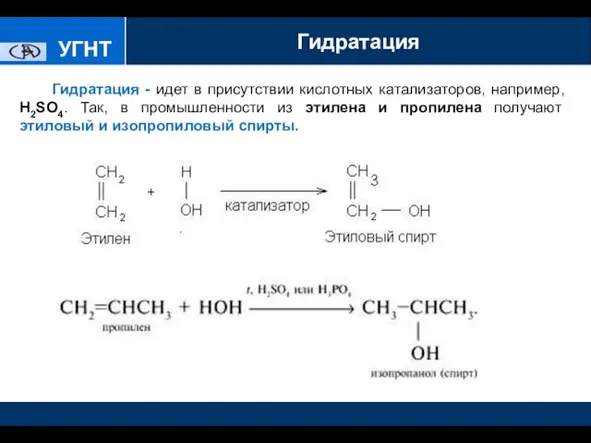
- 10. УГНТУ Гидратация - идет в присутствии кислотных катализаторов, например, H2SO4. Так, в промышленности из этилена и
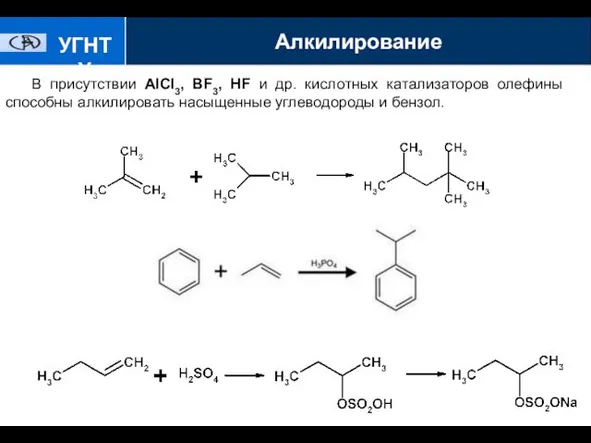
- 11. Алкилирование УГНТУ В присутствии АlСl3, BF3, HF и др. кислотных катализаторов олефины способны алкилировать насыщенные углеводороды
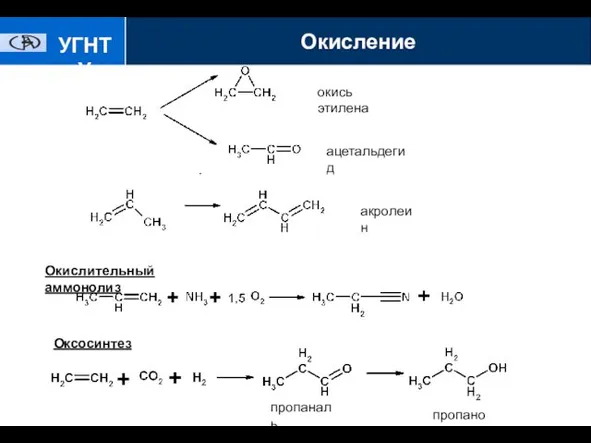
- 12. УГНТУ окись этилена ацетальдегид акролеин Окислительный аммонолиз Оксосинтез пропаналь пропанол
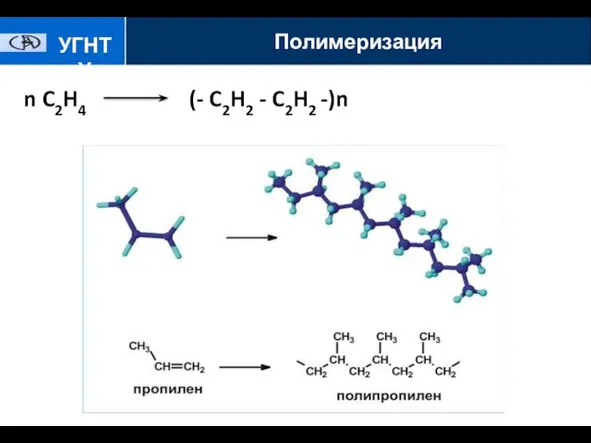
- 13. n C2H4 (- C2H2 - C2H2 -)n УГНТУ
- 14. Главным методом получения олефинов в промышленности являются процессы расщепления нефтяных фракций или углеводородных газов. Эти процессы
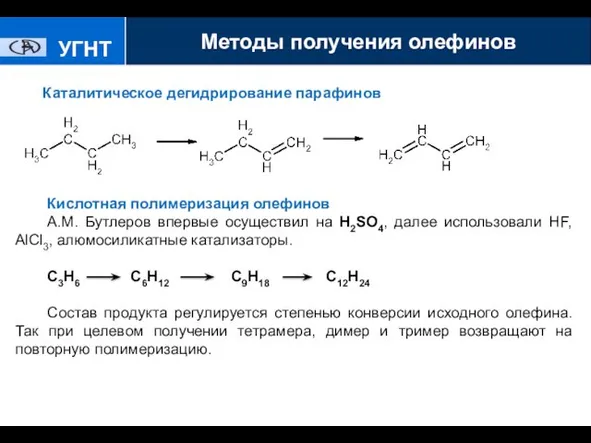
- 15. УГНТУ Каталитическое дегидрирование парафинов Кислотная полимеризация олефинов А.М. Бутлеров впервые осуществил на Н2SO4, далее использовали HF,
- 16. Для оценки возможных превращений углеводородов при переработке важную роль играет их термодинамическая стабильность. Термодинамическая стабильность углеводородов
- 17. Т Парафины может происходить лишь алкилирование. Т = 530 0С и выше расщепление практически необратимо. Высшие
- 18. Наиболее важная реакция - расщепление по углеродным связям. В результате образуется смесь газообразных и жидких насыщенных
- 19. Циклические углеводороды, присутствующие в нефтепродуктах, при тех же условиях отщепляют боковые цепи, а нафтеновые кольца, кроме
- 20. С повышением температуры расщепление идет более глубоко, но дополняется реакциями дегидрирования и циклизации. Дегидрирование также протекает
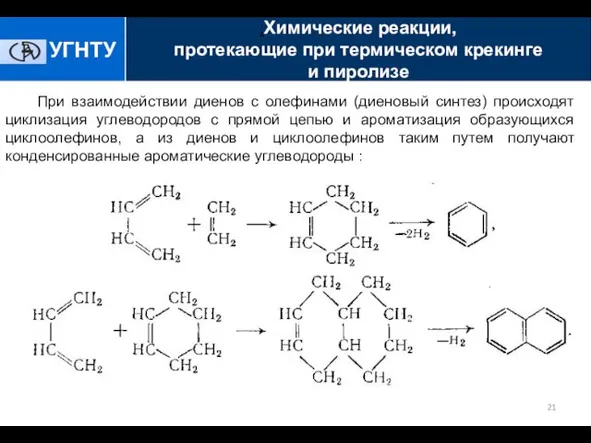
- 21. При взаимодействии диенов с олефинами (диеновый синтез) происходят циклизация углеводородов с прямой цепью и ароматизация образующихся
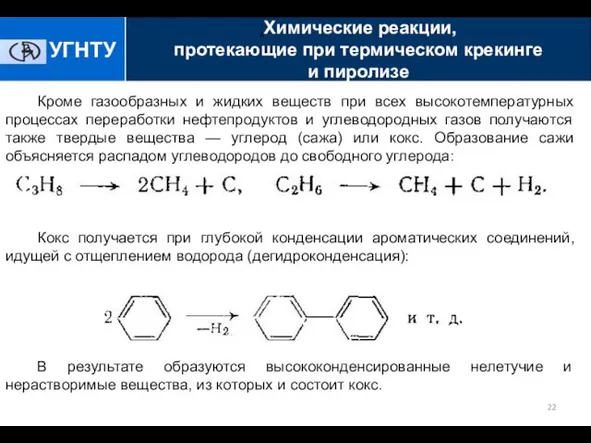
- 22. Кроме газообразных и жидких веществ при всех высокотемпературных процессах переработки нефтепродуктов и углеводородных газов получаются также
- 23. Относительный выход жидких продуктов (бензин и крекинг-остаток или смола пиролиза), газа (крекинг-газ или газ пиролиза) и
- 24. Каталитический крекинг приобрел преимущество перед термическим для производства моторных топлив. Причина – более высокие октановые числа,
- 25. В отличие от свободных радикалов ионы карбония легко изомеризуются. Вследствие этого бензин каталитического крекинга содержит много
- 26. УГНТУ Получение ЭС Пиролиз Процесс термического пиролиза углеводородного сырья остаётся основным способом получения низших олефинов —
- 27. УГНТУ Получение ЭС Пиролиз В промышленных условиях пиролиз углеводородов осуществляют при температурах 800—900°C и давлениях, близких
- 28. УГНТУ Пиролиз Для снижения скоростей вторичных реакций пиролиза используют разбавление сырья пиролиза водяным паром. В результате
- 30. Скачать презентацию














 Асептика и антисептика 222
Асептика и антисептика 222 Ограждение на перегоне пассажирского поезда. Сигналы ограждения на железнодорожном транспорте
Ограждение на перегоне пассажирского поезда. Сигналы ограждения на железнодорожном транспорте Кружок Волшебная бумага
Кружок Волшебная бумага Микроконтроллеры. Модули АЦП и ЦАП
Микроконтроллеры. Модули АЦП и ЦАП Філософія стародавнього світу
Філософія стародавнього світу Обмен веществ и энергии. Метаболизм
Обмен веществ и энергии. Метаболизм Мотивы и мотивация в зарубежных теориях
Мотивы и мотивация в зарубежных теориях Классные часы
Классные часы Медсестринський процес при корості та педикульозі
Медсестринський процес при корості та педикульозі Классификация и свойства эмоций
Классификация и свойства эмоций Использование энергии воды
Использование энергии воды Основные производственные фонды и производственные мощности геологоразведочного предприятия
Основные производственные фонды и производственные мощности геологоразведочного предприятия Презентация Сердечко 14.02.22г
Презентация Сердечко 14.02.22г Выбор правильного питания
Выбор правильного питания Определение географического положения горной системы в контурных картах
Определение географического положения горной системы в контурных картах О ПОЖАРЕ
О ПОЖАРЕ Гражданская война в России: причины, участники
Гражданская война в России: причины, участники Этапы ухода за кожей
Этапы ухода за кожей Властивість бісектриси трикутника
Властивість бісектриси трикутника Природа лесов и лесное хозяйство зоны хвойно-широколиственных лесов (Тема 5)
Природа лесов и лесное хозяйство зоны хвойно-широколиственных лесов (Тема 5) Планы защиты и планы обеспечения непрерывной работы и восстановления подсистем автоматизированной системы
Планы защиты и планы обеспечения непрерывной работы и восстановления подсистем автоматизированной системы Туберкулезный хориоретинит
Туберкулезный хориоретинит Antibiotics affecting codon phase-dependent binding of aminoacyl-tRNA to the ribosome
Antibiotics affecting codon phase-dependent binding of aminoacyl-tRNA to the ribosome презентация Богородица
презентация Богородица Жиры. Тема 2.5
Жиры. Тема 2.5 Работы которые проводятся при ликвидации чрезвычайных ситуаций техногенного и природного характера
Работы которые проводятся при ликвидации чрезвычайных ситуаций техногенного и природного характера Презентация на тему: Натуральный каучук.
Презентация на тему: Натуральный каучук. Российская компания Art Lumiere. Производство и реализация декоративных элементов из гипсокартона KNAUF
Российская компания Art Lumiere. Производство и реализация декоративных элементов из гипсокартона KNAUF