Содержание
- 2. Повторим: 1. Что такое бинарные соединения? 2. Какие классы неорганических веществ вам известны? 3.Что такое оксиды?
- 3. Задание выберите из перечня веществ ФОРМУЛЫ ОКСИДОВ . Дайте им названия. СuO CO2 Na2O Cu(OH)2 N2
- 4. Тема урока: Основания Цель урока: познакомиться с новым классом веществ – основания изучить номенклатуру , классификацию
- 5. Что такое основания? Основания – сложные вещества, состоящие из атомов металла и одной или нескольких групп
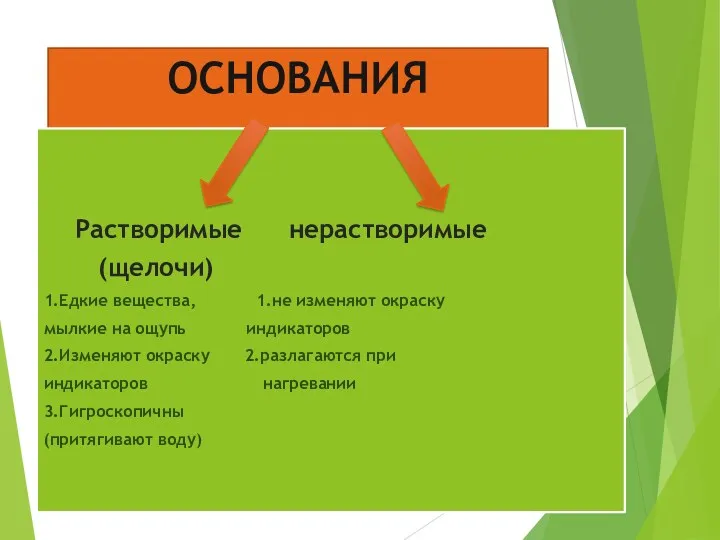
- 6. ОСНОВАНИЯ Растворимые нерастворимые (щелочи) 1.Едкие вещества, 1.не изменяют окраску мылкие на ощупь индикаторов 2.Изменяют окраску 2.разлагаются
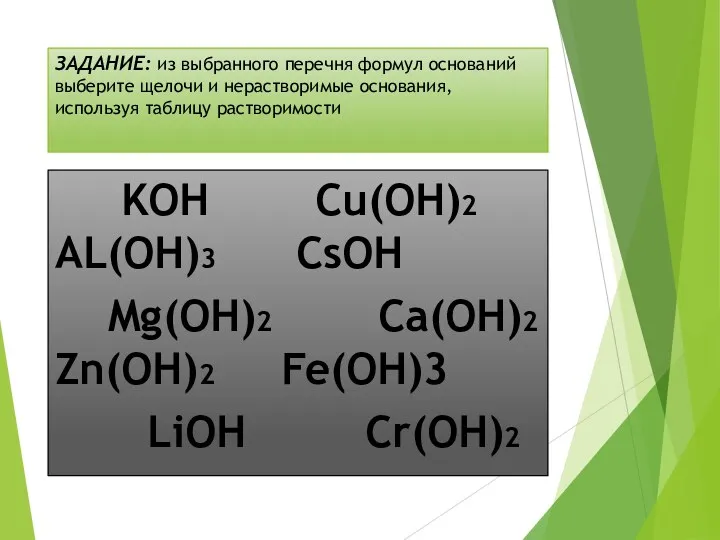
- 7. ЗАДАНИЕ: из выбранного перечня формул оснований выберите щелочи и нерастворимые основания, используя таблицу растворимости KOH Cu(OH)2
- 8. получение оснований 1) Активный металл + вода: 2Na + 2H2O = 2NaOH + H2 2) Оксид
- 9. действие индикаторов на щелочи в три пробирки с растворами гидроксида калия прилейте по каплям лакмус, метилоранж
- 10. химические свойства оснований взаимодействие с кислотами: NaOH+HCl=NaCl+H2O взаимодействие щелочей c кислотными оксидами: NaOH+CO2=Na2 CO3+H2O разложение при
- 11. Давайте повторим: В.1 Что такое основания? В.2 Как различаются основания по растворимости в воде? В.3 Как
- 12. Задание Составьте формулы гидроксидов, соответствующих оксидам K2O, BaO, Cr2O3. Дайте им названия.
- 13. Задание: закончить уравнения реакций: гидроксид бария + оксид серы (VI) = гидроксид бария + серная кислота
- 14. Домашнее задание : §31 упр.1,3-4.
- 16. Скачать презентацию











 Презентация ученицы 4 А класса Школьные годы чудесные
Презентация ученицы 4 А класса Школьные годы чудесные Космос глазами детей
Космос глазами детей Транспортная система в Токио
Транспортная система в Токио Безопасность жизнедеятельности
Безопасность жизнедеятельности Видеокурс Герои и антигерои XX века
Видеокурс Герои и антигерои XX века Оформление путевой документации и порядок списания горюче-смазочных материалов
Оформление путевой документации и порядок списания горюче-смазочных материалов Цели и задачи обучения математике в начальных классах
Цели и задачи обучения математике в начальных классах Акустический каротаж
Акустический каротаж Раннефеодальные государства и право Западной Европы
Раннефеодальные государства и право Западной Европы Урок толерантности (презентация)
Урок толерантности (презентация) Великий пост
Великий пост Челябинский институт развития профессионального образования. Итоги деятельности студенческого научного общества
Челябинский институт развития профессионального образования. Итоги деятельности студенческого научного общества Виды нарушения памяти
Виды нарушения памяти Внешняя политика России в начале XIX века
Внешняя политика России в начале XIX века презентация к уроку Кукольный театр
презентация к уроку Кукольный театр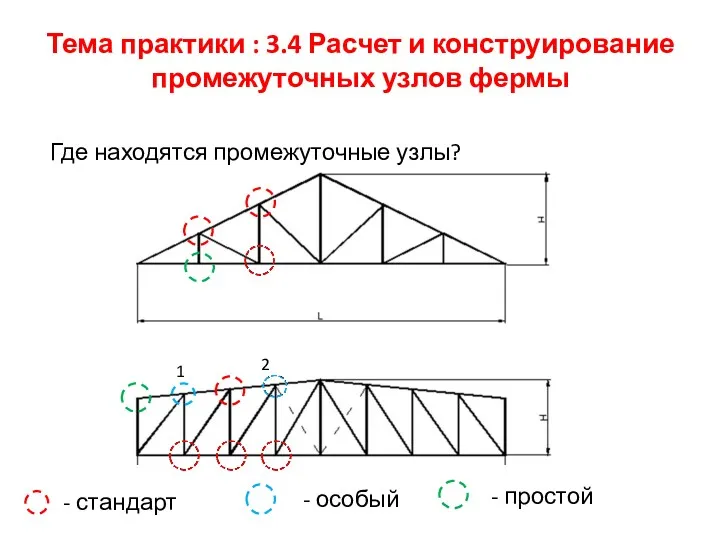 Расчет и конструирование промежуточных узлов фермы
Расчет и конструирование промежуточных узлов фермы Передовые технологии поставок алюминиевого металлопроката
Передовые технологии поставок алюминиевого металлопроката Пользовательский интерфейс
Пользовательский интерфейс Однополосные и широкополосные сигналы в системах радиосвязи. К лекции 4
Однополосные и широкополосные сигналы в системах радиосвязи. К лекции 4 Эмбриогенез человека
Эмбриогенез человека Судебно-медицинская экспертиза отравлений
Судебно-медицинская экспертиза отравлений Культурные памятники Центрального Чернозема
Культурные памятники Центрального Чернозема Презентация 3. Живопись Италии XVIIв. Караваджо
Презентация 3. Живопись Италии XVIIв. Караваджо Графика в Pascal
Графика в Pascal Имею право
Имею право Аппаратное и программное обеспечение сетей
Аппаратное и программное обеспечение сетей Беременность и роды при резус-несовместимости крови матери и плода
Беременность и роды при резус-несовместимости крови матери и плода Презентация по лексической теме День защитника Отечества
Презентация по лексической теме День защитника Отечества