Слайд 2
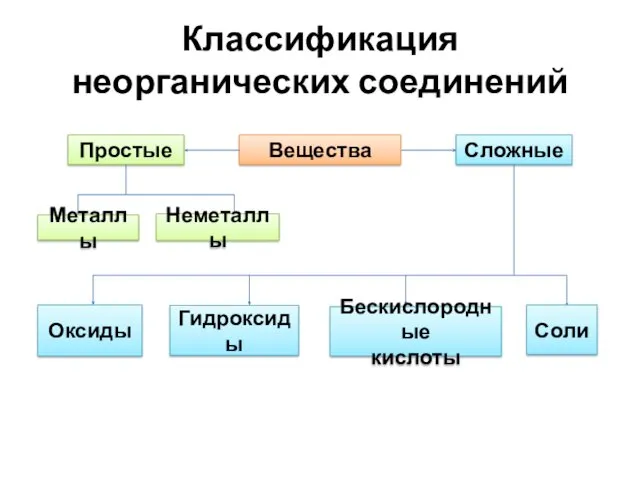
Классификация неорганических соединений
Вещества
Сложные
Простые
Металлы
Неметаллы
Оксиды
Гидроксиды
Соли
Бескислородные
кислоты
Слайд 3
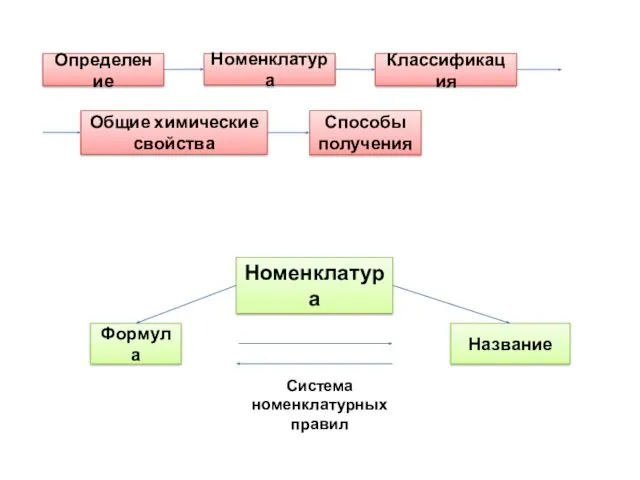
Определение
Номенклатура
Классификация
Общие химические свойства
Способы получения
Номенклатура
Формула
Название
Система номенклатурных
правил
Слайд 4
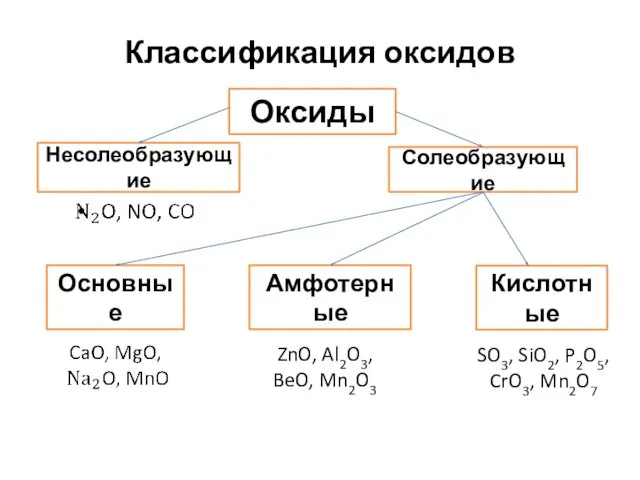
Классификация оксидов
Оксиды
Несолеобразующие
Солеобразующие
Кислотные
Амфотерные
Основные
ZnO, Al2O3,
BeO, Mn2O3
SO3, SiO2, P2O5, CrO3, Mn2O7
Слайд 5
Слайд 6

Химические свойства основных оксидов
Слайд 7

Химические свойства кислотных оксидов
Слайд 8

Химические свойства амфотерных оксидов
Слайд 9
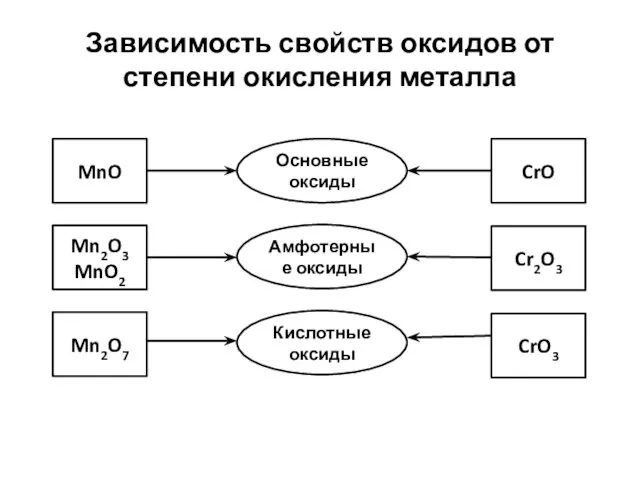
Зависимость свойств оксидов от степени окисления металла
Слайд 10

Способы получения оксидов
Слайд 11
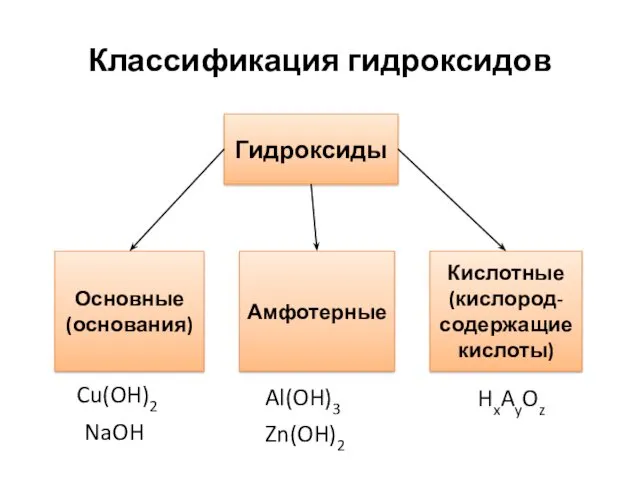
Классификация гидроксидов
Кислотные
(кислород-содержащие кислоты)
Основные
(основания)
Амфотерные
Гидроксиды
NaOH
Cu(OH)2
Zn(OH)2
Al(OH)3
HxAyOz
Слайд 12
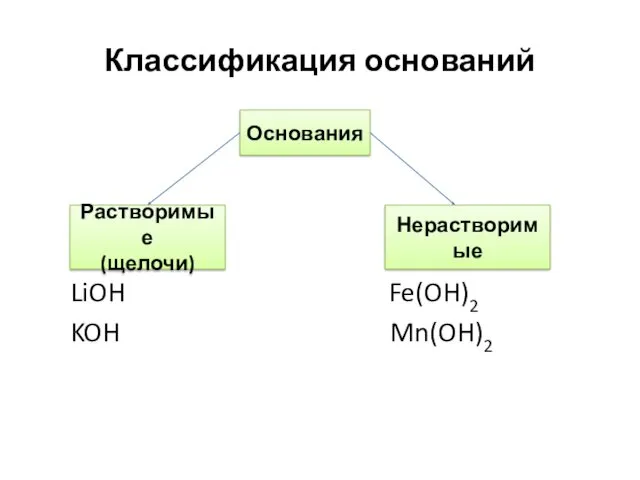
Классификация оснований
LiOH Fe(OH)2
KOH Mn(OH)2
Основания
Растворимые
(щелочи)
Нерастворимые
Слайд 13

Химические свойства оснований
Слайд 14

Слайд 15

Классификации кислот
По основности:
одноосновные HCl HNO3 HClO
многоосновные (двухосновные) H2SO4 H2CrO4
(трехосновные) H3РO4 H3AsO4
По наличию кислорода:
бескислородные HBr H2S
кислородсодержащие (оксокислоты) H2SeO3 HClO4
По силе:
сильные HMnO4 HI
слабые HF HCN H2CO3 H2SiO3
IV. По растворимости
Слайд 16

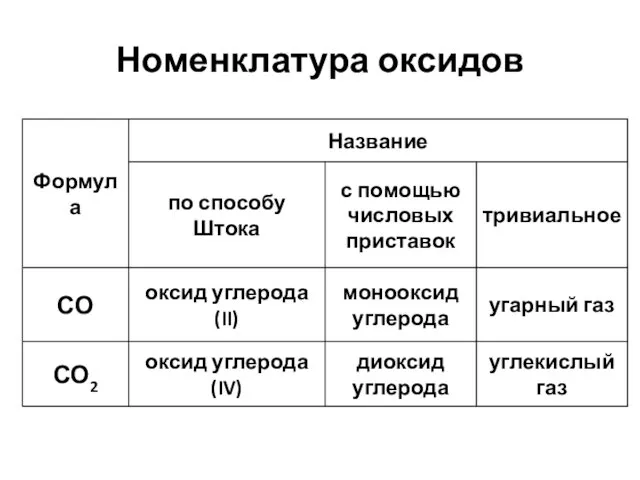
Номенклатура кислот
НА HxAyOz
HPO3 метафосфорная H4P2O7 дифосфорная
H3PO4 ортофосфорная H2S2O7 дисерная
Слайд 17

Химические свойства кислот
Слайд 18

Слайд 19

Свойства амфотерных гидроксидов
Слайд 20
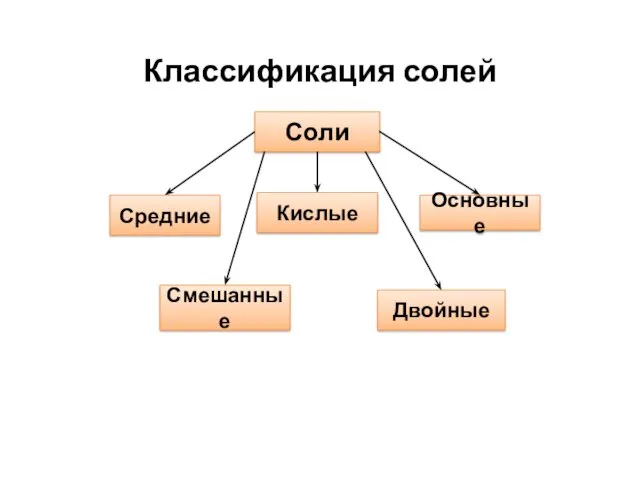
Классификация солей
Соли
Средние
Основные
Кислые
Смешанные
Двойные
Слайд 21

Средние соли
H2SO4 + 2NaOH = Na2SO4 + 2H2O
FeSO4 – сульфат
железа (II)
NH4NO3 – нитрат аммония
UO2SO4 – сульфат уранила
NONO3 – нитрат нитрозила
Na2S – сульфид натрия
CrCl3 – хлорид хрома (III)
Слайд 22
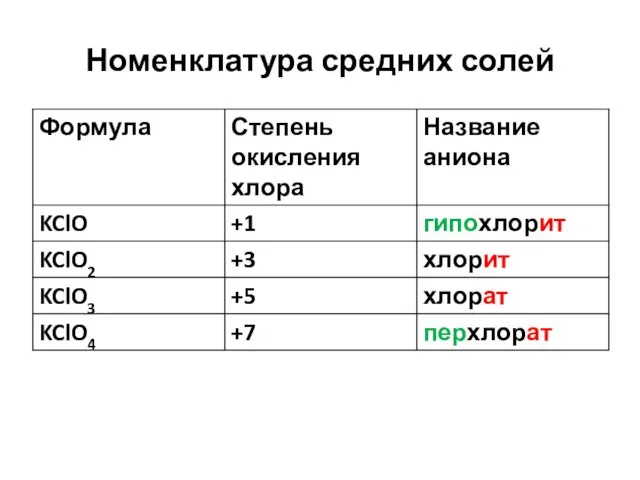
Номенклатура средних солей
Слайд 23

Кислые соли
H2SO4 + NaOH = NaHSO4 + H2O
Ba(HSO3)2 – гидросульфит бария
Ca(H2PO4)2
– дигидроортофосфат кальция
NaHS – гидросульфид натрия
Основные соли
Fe(OH)3 + 2HCl = (FeOH)Cl2 + 2H2O
(CuOH)2CO3 – гидроксокарбонат меди(II)
Al(OH)Cl2 – гидроксохлорид алюминия
Слайд 24

Двойные соли
KCr(SO4)2 – сульфат хрома(III)-калия
NaNH4Cl2 – хлорид аммония-натрия
Смешанные соли
Ca5(PO4)3F –
фторид-ортофосфат кальция
Слайд 25

Слайд 26

Слайд 27

Слайд 28




























 Пошаговая инструкция по заполнению заявления о выдаче повторного свидетельства о рождении
Пошаговая инструкция по заполнению заявления о выдаче повторного свидетельства о рождении Сын есімнің сөйлемдегі қызметі
Сын есімнің сөйлемдегі қызметі Маркировка кабелей
Маркировка кабелей Сигналы светофора
Сигналы светофора Jeopardy. Ad main topic here
Jeopardy. Ad main topic here опыт работы презентация
опыт работы презентация Основные положения законодательства об охране окружающей среды
Основные положения законодательства об охране окружающей среды Методика изучения и обобщения передового педагогического опыта
Методика изучения и обобщения передового педагогического опыта Английские надписи на одежде и их влияние на культуру современных подростков
Английские надписи на одежде и их влияние на культуру современных подростков Сварка чугуна
Сварка чугуна Внеклассное занятие Если добрый ты...
Внеклассное занятие Если добрый ты... Портрет выпускника начальной школы по ФГОС
Портрет выпускника начальной школы по ФГОС Духовные искания Пьера Безухова
Духовные искания Пьера Безухова Отчет о создании развивающей среды.
Отчет о создании развивающей среды. Из опыта работы учителя математики Никифоровой З.З
Из опыта работы учителя математики Никифоровой З.З Орфография. Слитное, раздельное, дефисное написание. Написание не с разными частями речи
Орфография. Слитное, раздельное, дефисное написание. Написание не с разными частями речи Динамические структуры данных
Динамические структуры данных Инструкция по проведению Вводного тренинга ЭТП
Инструкция по проведению Вводного тренинга ЭТП География черной металлургии
География черной металлургии
 Организация исследовательское деятельности в учебном процессе. Из опыта работы учителя географии
Организация исследовательское деятельности в учебном процессе. Из опыта работы учителя географии Ликвидация дефектных участков на морских нефте- и газопроводах
Ликвидация дефектных участков на морских нефте- и газопроводах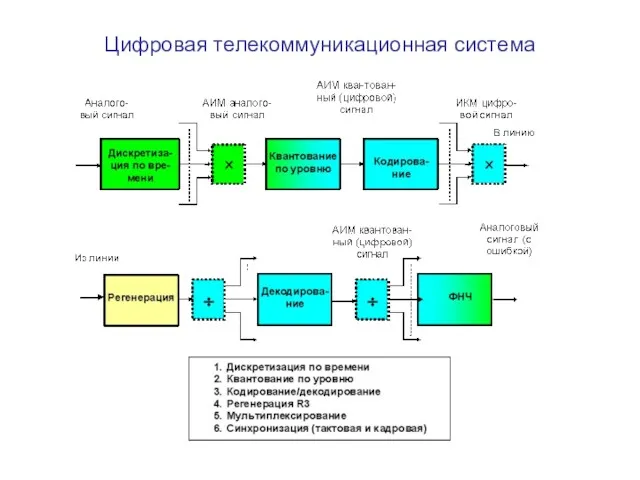 Цифровая телекоммуникационная система
Цифровая телекоммуникационная система Культура и духовная жизнь общества
Культура и духовная жизнь общества Причины и клинические синдромы перинатального поражения нервной системы в периоде новорожденности
Причины и клинические синдромы перинатального поражения нервной системы в периоде новорожденности Экологические болезни
Экологические болезни Выпускники
Выпускники Household items furniture
Household items furniture