Содержание
- 2. Термодинамический процесс Изменение состояния термодинамической системы во времени называется термодинамическим процессом. Так, при перемещении поршня в
- 3. Термодинамический процесс Система, выведенная из состояния равновесия, и предоставленная при постоянных параметрах окружающей среды самой себе,
- 4. Равновесный термодинамический процесс Термодинамический процесс называется равновесным, если все параметры системы при его протекании меняются достаточно
- 5. Равновесный процесс состоит из непрерывного ряда последовательных состояний равновесия, поэтому в каждой его точке состояние термодинамической
- 6. Неравновесные термодинамические процессы Процессы, не удовлетворяющие условию , протекают с нарушением равновесия, т. е. являются неравновесными.
- 7. 2. Внутренняя энергия и работа расширения и сжатия рабочего тела
- 8. Основы термодинамики Внутренняя энергия идеального газа -это кинетическая энергия хаотического (теплового) движения молекул. Среднее значение энергии
- 9. Внутреняя энергия – функция состояния, зависит от температуры. Температура – мера интенсивности теплового движения молекул. Изменение
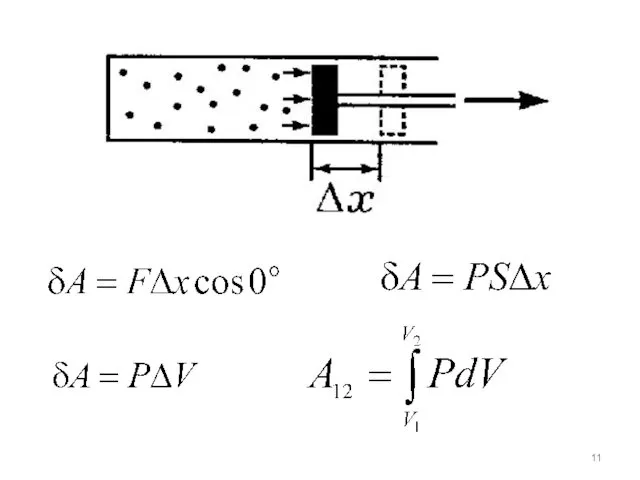
- 10. Внутренняя энергия изменяется путём совершения работы и путём теплообмена. Работа – это процесс изменения внутренней энергии
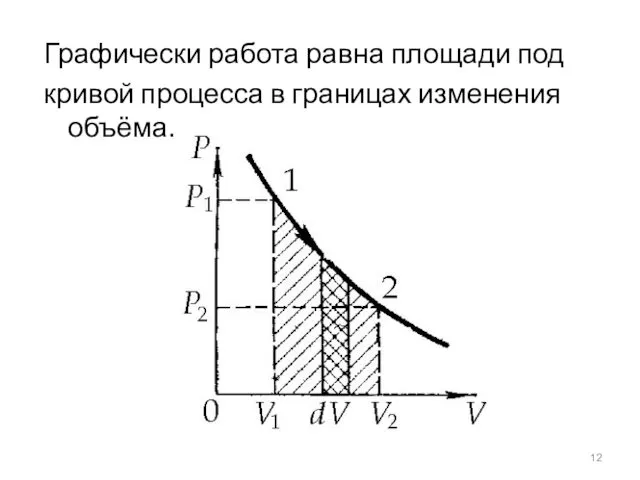
- 12. Графически работа равна площади под кривой процесса в границах изменения объёма.
- 13. Приращение внутренней энергии в процессе чистого теплообмена называется количеством теплоты или просто – теплотой (Q). Теплота
- 14. 3. Первый закон термодинамики. Энтальпия газа
- 15. Первое начало термодинамики Количество теплоты, которое система получает в процессе теплообмена идет на изменение внутренней энергии
- 16. В более общем случае: и – это количественные характеристики процесса изменения энергии – элементарные теплота и
- 17. Энтальпия В термодинамике важную роль играет сумма внутренней энергии системы U и произведения давления системы р
- 18. Энтальпия Величина , называемая удельной энтальпией (h = H/M), представляет собой энтальпию системы, содержащей 1 кг
- 19. Энтальпия Если давление системы сохраняется неизменным, т. е. осуществляется изобарный процесс (dp=0), то и т. е.
- 20. 4. Процессы изменения состояния идеального газа
- 21. Применение 1 закона термодинамики к изопроцессам Изотермический. dT = 0), (dU = 0). РV = const.
- 22. Изохорный процесс. Р/Т = const. =0 Изобарный процесс (P = const)
- 23. Адиабатическим называется процесс, протекающий без теплообмена с окружающей средой
- 24. Адиабатный процесс. – показатель адиабаты.
- 25. Уравнение адиабатического процесса в переменных Т и V :
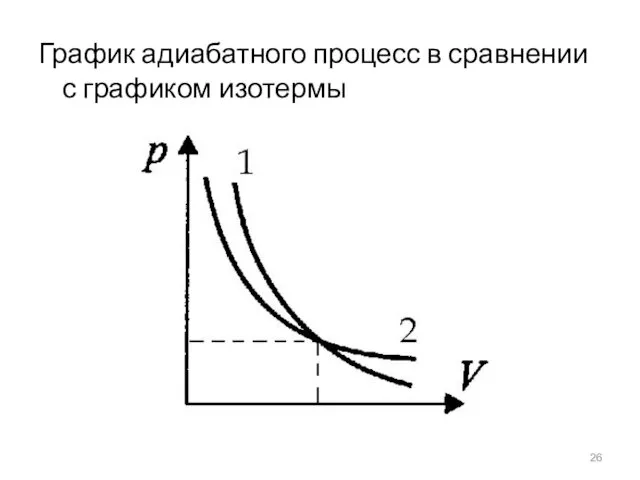
- 26. График адиабатного процесс в сравнении с графиком изотермы
- 27. Работа при адиабатном процессе
- 28. Политропный процесс Все процессы – частный случай политропного. Изохорный – Изобарный – Изотермический – Адиабатный -
- 30. Скачать презентацию
























 Коклюш. Паракоклюш
Коклюш. Паракоклюш Трехкомпонентные системы
Трехкомпонентные системы Выражение и его значение. Порядок выполнения действий. Равенства и неравенства
Выражение и его значение. Порядок выполнения действий. Равенства и неравенства Крымская весна. Лекция 13
Крымская весна. Лекция 13 Что изучают в курсе География материков и океанов?
Что изучают в курсе География материков и океанов? Моделирование и конструирование одежды промышленного производства
Моделирование и конструирование одежды промышленного производства А. И. Куприн Куст сирени
А. И. Куприн Куст сирени The indefinite article (a/an) - неопределенный артикль
The indefinite article (a/an) - неопределенный артикль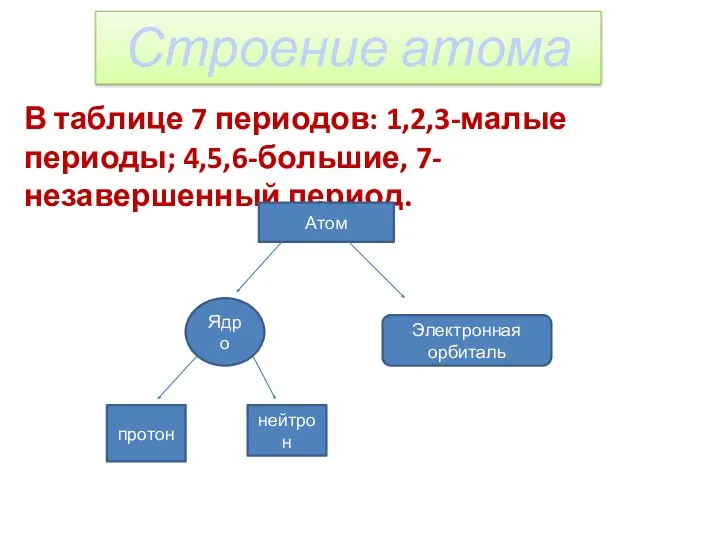 Строение атома
Строение атома Современные проблемы сохранения КОТР Журавлиная родина: новые реалии XXI века
Современные проблемы сохранения КОТР Журавлиная родина: новые реалии XXI века Основные виды PR-мероприятий
Основные виды PR-мероприятий Прочность бетона
Прочность бетона Аппликация кораблик. Поэтапное изготовление
Аппликация кораблик. Поэтапное изготовление Мониторинг народная игротерапия
Мониторинг народная игротерапия Профессиональная этика педагога. Закон Об образовании РФ, ФГОСы, ПСП и ФОСы
Профессиональная этика педагога. Закон Об образовании РФ, ФГОСы, ПСП и ФОСы Абсолютные и относительные величины
Абсолютные и относительные величины Музыкальный фотоальбом Времена года-зима.
Музыкальный фотоальбом Времена года-зима. Возможности и варианты активизации инновационных процессов НГК РФ в условиях санкций
Возможности и варианты активизации инновационных процессов НГК РФ в условиях санкций Компьютерная презентация Путешествие в Африку
Компьютерная презентация Путешествие в Африку Японская национальная валюта йена
Японская национальная валюта йена Исследование функции. Построение графиков
Исследование функции. Построение графиков Русское национальное блюдо Ватрушки
Русское национальное блюдо Ватрушки Живой Журнал: инструкция по эксплуатации
Живой Журнал: инструкция по эксплуатации دیمر کارکرد عملکرد
دیمر کارکرد عملکرد Лесной пожар
Лесной пожар Внутренняя энергия и энтальпия
Внутренняя энергия и энтальпия Современные теории психопатологии личности
Современные теории психопатологии личности Презентация совместной деятельности педагога с детьми и детей с родителями Фестиваль пасхальных посиделок
Презентация совместной деятельности педагога с детьми и детей с родителями Фестиваль пасхальных посиделок