Слайд 2

Эквивалент
– это часть молекулы (атома) вещества, равноценная в химической реакции одному
атому или иону водорода или одному электрону.
Слайд 3

или
Эквивалентом вещества называется такое его количество, которое соединяется с 1 молем
атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Слайд 4

молярная масса эквивалента вещества
– это масса одного моль эквивалентов вещества, равноценная
в химической реакции массе 1 моль атомов или ионов водорода или количеству электронов 1 моль.
Слайд 5

или эквивалентной массой
называется масса 1 эквивалента вещества
Слайд 6

Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
1.Химические элементы.
Мэ =
М / n
Где Мэ – молярная масса эквивалента элемента,
М – молярная масса элемента,
n - валентность.
Слайд 7

Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
2.Кислоты и основания.
Мэ
= М / n
Где Мэ – молярная масса эквивалента вещества,
М – молярная масса вещества,
n – основность кислоты (количество Н) или кислотность (количество групп ОН) основания.
Слайд 8

Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
3.Соли и оксиды.
Мэ
= М / (N * n)
Где Мэ – молярная масса эквивалента вещества,
М – молярная масса вещества,
N – количество катионов в формуле,
n – формальный заряд катиона.
Слайд 9

Расчет молярной массы эквивалента вещества осуществляется по следующим правилам:
4.Окислители и восстановители.
Мэ
= М / n
Где Мэ – молярная масса эквивалента вещества,
М – молярная масса вещества,
n – количество электронов, присоединяемое одной молекулой окислителя или отдаваемое одной молекулой восстановителя.
Слайд 10

Молярная масса одного итого же вещества может рассчитываться по – разному,
в зависимости от его химических свойств.
Слайд 11

Для экспериментального определения молярной массы эквивалента вещества необходимо найти массу данного
вещества, равноценную в химической реакции молярной массе эквивалента другого известного вещества
Слайд 12

Источник
Задачи и упражнения по общей химии: Учеб. Пособие для вузов/Под.ред. В.А.Рабиновича
и Х..Рубиной.- 24-е изд., испр.- Л.: Химия, 1986.-272 с.,ил.











 Звуковые волны
Звуковые волны Стандартты толық теледидар сигналдарын зерттеу
Стандартты толық теледидар сигналдарын зерттеу Информация – это сведения о предметах, процессах и явлениях окружающего нас мира
Информация – это сведения о предметах, процессах и явлениях окружающего нас мира Деловой этикет
Деловой этикет Презентация к театрализованной постановке Без привычек вредных жить на свете здорово!
Презентация к театрализованной постановке Без привычек вредных жить на свете здорово!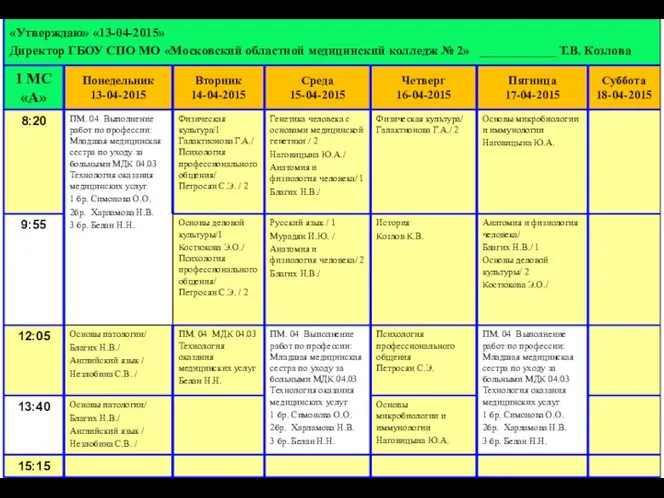 Расписание MOMK2
Расписание MOMK2 Что изучает история
Что изучает история Формирование доброжелательных отношений среди дошкольников
Формирование доброжелательных отношений среди дошкольников NIR Systems
NIR Systems Собака - друг человека - презентация
Собака - друг человека - презентация Безусловное принятие
Безусловное принятие Согласие да лад для общего дела клад
Согласие да лад для общего дела клад Учитель математики
Учитель математики Радуга, федеральная аптечная сеть
Радуга, федеральная аптечная сеть Гидродинамические аварии
Гидродинамические аварии Проектирование транспортной системы в машиностроительном производстве
Проектирование транспортной системы в машиностроительном производстве Вводное занятие по геометрии для учащихся 7 класса
Вводное занятие по геометрии для учащихся 7 класса Методы и приборы оценки ровности дорожных покрытий
Методы и приборы оценки ровности дорожных покрытий Приёмы сжатия (компрессии) текста
Приёмы сжатия (компрессии) текста Презентация Инструментарий педагога для развития IT-компетенций
Презентация Инструментарий педагога для развития IT-компетенций Книжная выставка. Избирательное право. Избирательный процесс
Книжная выставка. Избирательное право. Избирательный процесс Электроосветительные приборы
Электроосветительные приборы Родительское собрание Ваш ребенок - третьеклассник (с презентацией)
Родительское собрание Ваш ребенок - третьеклассник (с презентацией) Низковольтное оборудование. Стабилизаторы напряжения Since 2000. Преобразователи напряжения
Низковольтное оборудование. Стабилизаторы напряжения Since 2000. Преобразователи напряжения Поняття креативності в психології та педагогіці
Поняття креативності в психології та педагогіці Магнитные взаимодействия
Магнитные взаимодействия Преступления и девиантное поведение
Преступления и девиантное поведение Роберт Миңнулин иҗатында туган як образы (презентация)
Роберт Миңнулин иҗатында туган як образы (презентация)