Содержание
- 2. Распределите эти формулы по классам в таблицу MgO, NaOH, H2S, N2 O5, Zn(OH)2, K2O, HCI, SiO2,
- 3. Тема: Кислоты “Просто знать – еще не все, знания нужно уметь использовать”. (Иоганн Гете)
- 4. Что должны узнать на уроке: какие бывают кислоты, какая формула кислоты, как их классифицируют, как составляют
- 5. СТАНЦИЯ ИНФОРМАЦИОННАЯ Кислоты вокруг нас
- 6. Кислоты в дождевой воде Углекислый газ при растворении дает раствор слабой угольной кислоты Азотная кислота может
- 7. Природное озеро серной кислоты на п-ове Камчатка
- 8. Кислоты в животном мире Тропический паук педипальпида стреляет во врагов струйкой жидкости, содержащей 84% уксусной кислоты.
- 9. Кислоты в растительном мире Мухоморы в качестве ядовитых токсинов «используют» иботеновую кислоту. Это вещество так ядовито,
- 10. Кислоты в организме человека Если ты проглотил аскорбинку, Твой организм получил витаминку. Она закрывает болезням врата
- 11. Кислоты в нашей пище Жуйте лимон, если горло болит, Сок чудотворный вас исцелит.
- 12. Яблоко ешь, кислый вкус – красота . В яблоке – яблочная кислота. .
- 13. Думаю, что не приукрашу, Если хвалить буду я простоквашу. Есть в ней молочная кислота – Молодость
- 14. Яблочный уксус по ложке пейте, Вы обязательно похудеете. Уксус столовый на кухне хранится – Для консервации
- 15. Лучше не жуйте косточки вишни, Косточки сливы – это лишнее. Будет вам плохо – диагноз такой:
- 16. Вывод Кислоты разные нужны, Кислоты всякие важны! Они и в пище и в траве, В белке,
- 17. Что произойдет, если к сахару добавить концентрированную серную кислоту? СТАНЦИЯ ЭКСПЕРИМЕНТАЛЬНАЯ
- 18. Концентрированная серная кислота обугливает органические вещества. Правила техники безопасности: Внимание! Работать с кислотами необходимо аккуратно, так
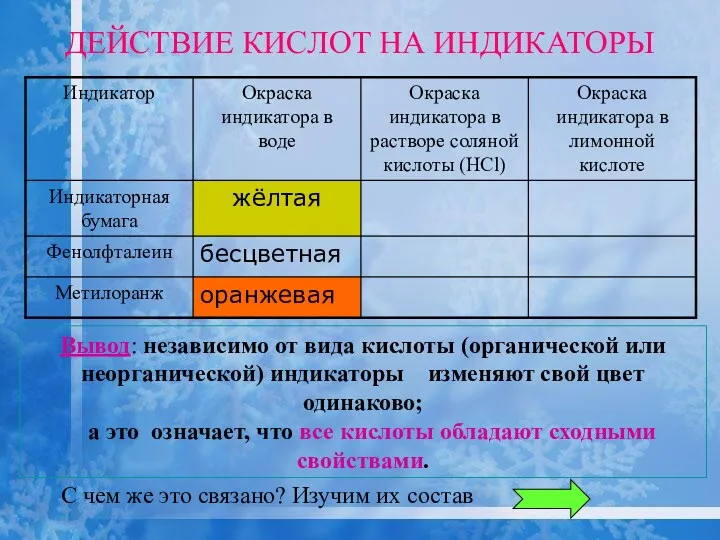
- 19. ДЕЙСТВИЕ КИСЛОТ НА ИНДИКАТОРЫ Вывод: независимо от вида кислоты (органической или неорганической) индикаторы изменяют свой цвет
- 20. СТАНЦИЯ ТЕОРЕТИЧЕСКАЯ
- 21. Прочитайте формулы кислот. HCl, H2SO4, H3PO4 Кислоты – это сложные вещества, состоящие из ионов водорода и
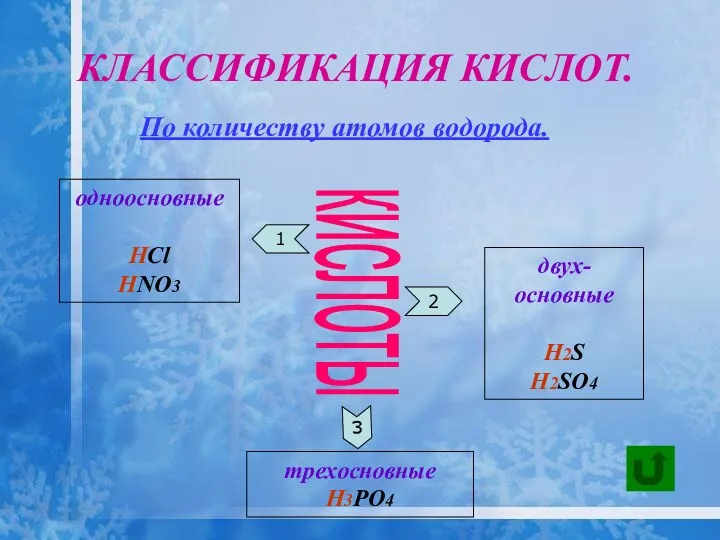
- 22. КЛАССИФИКАЦИЯ КИСЛОТ. кислоты 2 1 3 одноосновные HCl HNO3 двух- основные H2S H2SO4 трехосновные H3PO4 По
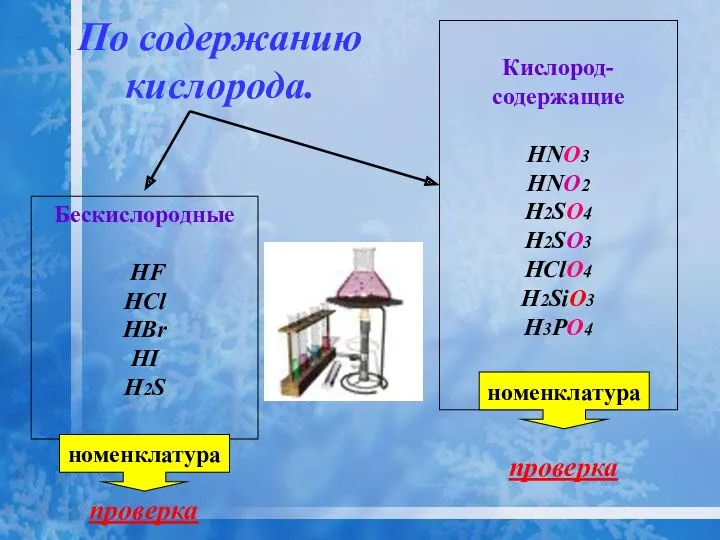
- 23. По содержанию кислорода. Бескислородные HF HCl HBr HI H2S Кислород- содержащие HNO3 HNO2 H2SO4 H2SO3 HClO4
- 24. НОМЕНКЛАТУРА КИСЛОТ Бескислородные кислоты: К названию кислотообразующего элемента добавляют гласную «о» и слова «водородная кислота» HCl
- 25. Кислородсодержащие кислоты: К русскому названию кислотообразующего элемента добавляют суффикс: Если элемент проявляет высшую С.О.(равную № группы)
- 28. Выполнение задания Выясните и запишите, на каком признаке основывается каждая из классификаций 1 вариант Кислоты: H3PO4,
- 29. ОРГАНИЧЕСКИЕ – ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ, ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ. По происхождению кислоты бывают
- 30. НЕОРГАНИЧЕСКИЕ- СЕРНАЯ, СОЛЯНАЯ, ПЛАВИКОВАЯ, ФОСФОРНАЯ, АЗОТНАЯ.
- 31. КИСЛОТЫ ПРИМЕНЯЮТСЯ В МЕДИЦИНЕ. Аскорбиновая, фолиевая, ацетил- салициловая и другие
- 32. КИСЛОТЫ ПРИМЕНЯЮТСЯ В КУЛИНАРИИ . Уксусная и лимонная кислоты.
- 33. Задание: в каждой строчке удалите формулу вещества, которое принадлежит к другому классу Игра «Третий лишний» CO2
- 35. Скачать презентацию





























 Yuhan. Global map
Yuhan. Global map Презентация к выступлению учащихся 4 классов ГБОУ СОШ №394 на районном конкурсе Безопасное колесо.
Презентация к выступлению учащихся 4 классов ГБОУ СОШ №394 на районном конкурсе Безопасное колесо. Стромалық-қантамырлық дистрофиялар дәнекер тінде зат ал-масуының бүзылуымен, осыган байланысты агзалар
Стромалық-қантамырлық дистрофиялар дәнекер тінде зат ал-масуының бүзылуымен, осыган байланысты агзалар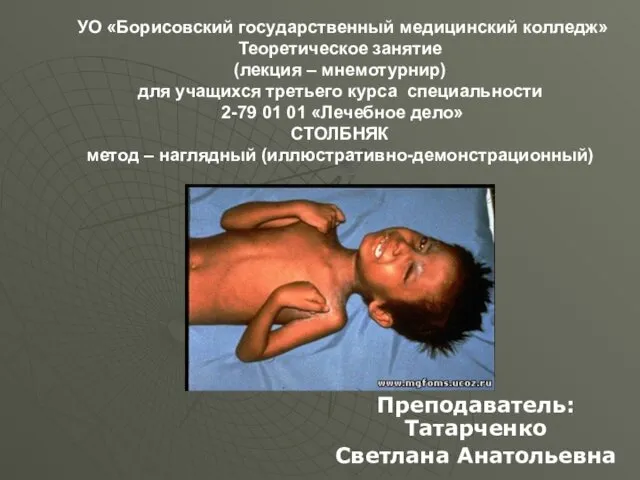 Столбняк. Источник инфекции
Столбняк. Источник инфекции Презентация Наш любимый детский сад
Презентация Наш любимый детский сад Системная склеродермия
Системная склеродермия Kursovaya_rabota_8
Kursovaya_rabota_8 Судебный прецедент как источник права
Судебный прецедент как источник права Подразделение по связям с общественностью и рекламе в структуре предприятия
Подразделение по связям с общественностью и рекламе в структуре предприятия Техническое обслуживание и ремонт коробки передач автомобиля Камаз-5320
Техническое обслуживание и ремонт коробки передач автомобиля Камаз-5320 Публичные выступления. Ораторское искусство
Публичные выступления. Ораторское искусство презентация по пожарной безопасности
презентация по пожарной безопасности Неравенство треугольника. Урок 46
Неравенство треугольника. Урок 46 Развитие исследовательской деятельности на уроках географии.
Развитие исследовательской деятельности на уроках географии.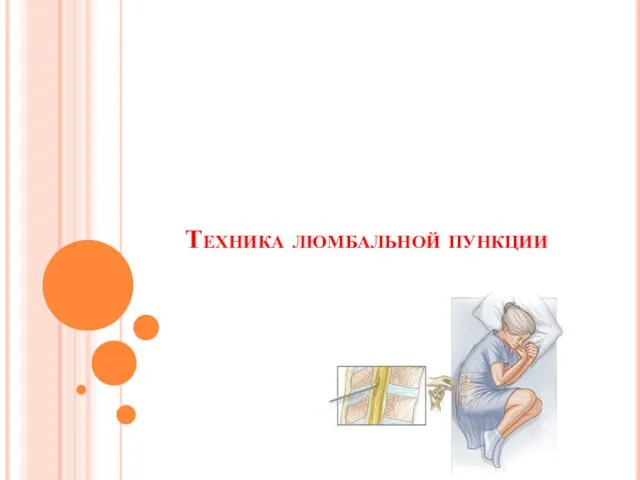 Техника люмбальной пункции
Техника люмбальной пункции Мережа SDH. Технологія SDH
Мережа SDH. Технологія SDH Корсаковский синдром
Корсаковский синдром Поздравительная открытка к 23 февраля
Поздравительная открытка к 23 февраля Презентация Складывание фигурок оригами на основе базовой формы Воздушный змей Диск
Презентация Складывание фигурок оригами на основе базовой формы Воздушный змей Диск Сюжетно-ролевая игра как средство нравственного воспитания старших дошкольников
Сюжетно-ролевая игра как средство нравственного воспитания старших дошкольников Образовательный портал, как средство повышения эффективности образовательного процесса
Образовательный портал, как средство повышения эффективности образовательного процесса Rozliczenie w handlu zagranicznym ( cz.1)
Rozliczenie w handlu zagranicznym ( cz.1) Строки в языке С++
Строки в языке С++ Metode numerice in mecanica solidului deformabil
Metode numerice in mecanica solidului deformabil Технология машиностроения. Изготовление валов
Технология машиностроения. Изготовление валов Флаги, переходы, макрокоманды условий, циклы, битовые операции, стек, подпрограммы, сдвиги в MASM
Флаги, переходы, макрокоманды условий, циклы, битовые операции, стек, подпрограммы, сдвиги в MASM Основы PHP
Основы PHP Александр Невский - князь покрытый воинской славой
Александр Невский - князь покрытый воинской славой