Содержание
- 2. Типы химических реакций на примере свойств воды. Na + HOH = NaOH + H2 2Na +
- 3. 4P + 5O2 = 2P2O5 P2O5 + 3H2O = 2H3PO4 реакция соединения
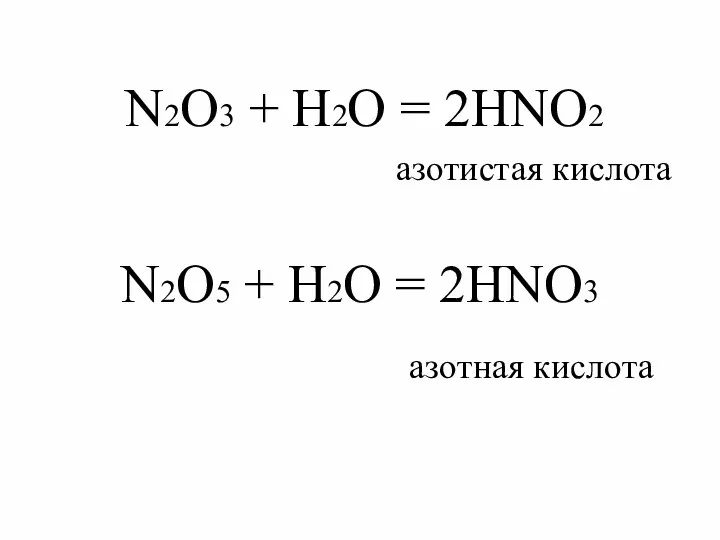
- 4. N2O3 + H2O = 2HNO2 азотистая кислота N2O5 + H2O = 2HNO3 азотная кислота
- 5. SiO2 + H2O = CaO + H2O = Ca(OH)2 реакция соединения
- 6. CuO + H2O = Fe2O3 + H2O = Вода реагирует с оксидами металлов и оксидами неметаллов
- 7. 2H2O = 2H2 + O2 реакция разложения
- 8. CaC2 +2HOH = C2H2 +Ca(OH)2 реакция обмена Al2S3+ 6HOH = 2Al(OH)3+ 3H2S реакция обмена
- 9. Гидролиз - обменное взаимодействие веществ с водой, приводящее к их разложению.
- 10. Закончите уравнения реакций, укажите их тип. Расставьте коэффициенты: K + H2O = BaO + H2O =
- 11. 2K + 2H2O = 2KOH + H2 реакция замещения BaO + H2O = Ba(OH)2 реакция соединения
- 12. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: S SO2 H2SO3 S + O2
- 13. Ba BaO Ba(OH)2 BaCl2 2Ba+ O2=2BaO BaO+ H2O=Ba(OH)2 Ba + 2H2O =Ba(OH)2 + H2 Ba(OH)2 +2HCl
- 15. Скачать презентацию










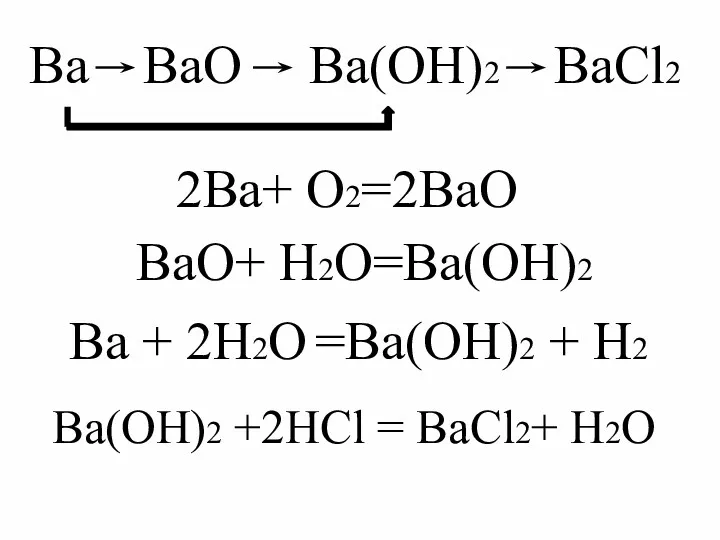
 Портфолио педагога- Биккиняевой Рамили Абдрякиповны
Портфолио педагога- Биккиняевой Рамили Абдрякиповны Основы безопасности жизнедеятельности в сети интернет. Безопасная работа для рук и спины
Основы безопасности жизнедеятельности в сети интернет. Безопасная работа для рук и спины Искусство японской каллиграфии
Искусство японской каллиграфии Диплом_Петров
Диплом_Петров Умножение одночленов. Возведение одночлена в степень
Умножение одночленов. Возведение одночлена в степень Средства музыкальной выразительности
Средства музыкальной выразительности Хлеб всему голова
Хлеб всему голова Хвала Христу
Хвала Христу ВКР: Изготовление бюгельного протеза на нижнюю челюсть с кламмерной фиксацией
ВКР: Изготовление бюгельного протеза на нижнюю челюсть с кламмерной фиксацией Животноводство. Окружающий мир. (3 класс)
Животноводство. Окружающий мир. (3 класс) Знатоки математики
Знатоки математики Коррекция агрессивного поведения
Коррекция агрессивного поведения Озон в перерабатывающих производствах
Озон в перерабатывающих производствах Выставка поделок на тему Зимушка-зима
Выставка поделок на тему Зимушка-зима Александр Бенуа. Грани таланта
Александр Бенуа. Грани таланта Творческий отчет по самообразрванию на тему: Развитие творческих способностей учащихся на уроках литературного чтения
Творческий отчет по самообразрванию на тему: Развитие творческих способностей учащихся на уроках литературного чтения UNIFICAZIONE
UNIFICAZIONE Интеллектуальная игра Что такое хорошо и что такое плохо для учеников 2-го класса
Интеллектуальная игра Что такое хорошо и что такое плохо для учеников 2-го класса Из чего состоят роботы?
Из чего состоят роботы? Контрольная работа по технологии, 6 класс
Контрольная работа по технологии, 6 класс Общие понятия о Биомедицине. Разграничение и взаимосвязь медицинской практики и исследования
Общие понятия о Биомедицине. Разграничение и взаимосвязь медицинской практики и исследования Построение автоматической воронки продаж
Построение автоматической воронки продаж Презентация Права ребенка Диск
Презентация Права ребенка Диск Рассказ Федора Абрамова О чем плачут лошади
Рассказ Федора Абрамова О чем плачут лошади Цветовые контрасты
Цветовые контрасты Государственные финансы
Государственные финансы День Святого Валентина
День Святого Валентина Keeping healthy
Keeping healthy