Содержание
- 2. План изучения темы: Глюкоза в природе. Биологические функции. Физические свойства. Строение глюкозы. Химические свойства. Получение. Применение.
- 3. Глюкоза Виноградный сахар
- 4. Обнаружение глюкозы в различных продуктах t0 Исследуемое + реактив → осадок вещество Фелинга желтого цвета I
- 5. Физические свойства глюкозы Бесцветное кристаллическое вещество; Хорошо растворяется в воде; Сладкое на вкус.
- 6. Молекулярная формула C6Н12О6
- 7. Глюкоза – многоатомный спирт ? Лабораторный опыт: Взаимодействие с гидроксидом меди (II) Глюкоза + NaOH +
- 8. Глюкоза – альдегид ? Лабораторный опыт: Взаимодействие с аммиачным раствором оксида серебра. t0 AgNO3 + NH4OH
- 9. Глюкоза – многоатомный спирт ? Лабораторный опыт: Взаимодействие с гидроксидом меди (II) t0 Глюкоза + NaOH
- 10. Глюкоза – карбоновая кислота? Лабораторный опыт: Изменение окраски индикаторов Глюкоза + лакмус → раствор красного цвета
- 11. А.А. Колли – русский химик, профессор Московского университета 1 моль глюкозы + 5 моль СН3СООН ???
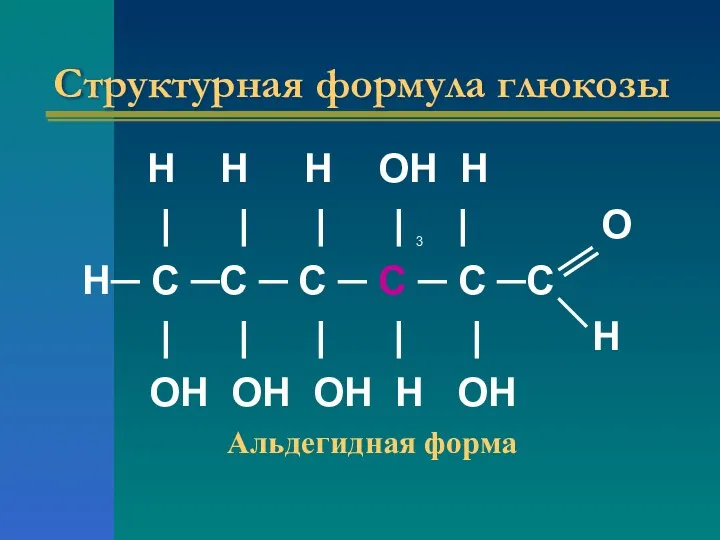
- 12. Структурная формула глюкозы Н Н Н ОН Н | | | | 3 | О Н─
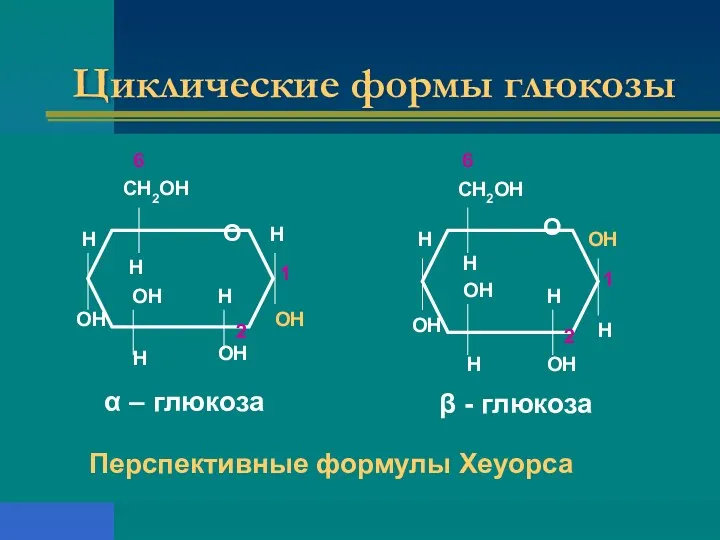
- 13. Циклические формы глюкозы СН2ОН Н Н ОН ОН Н Н ОН Н ОН О СН2ОН Н
- 14. Таутомерия α – глюкоза альдегидная форма 37% 0,0026% 63% Таутомерия (динамическая изомерия) существование изомерных форм, находящихся
- 15. Химические свойства глюкозы
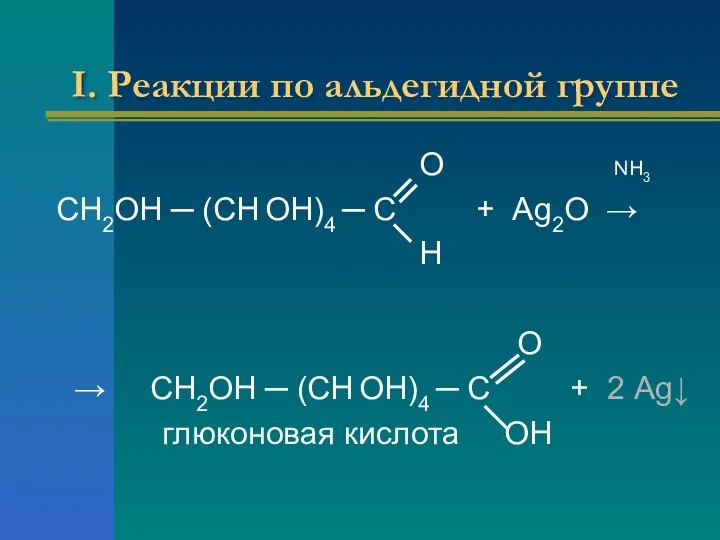
- 16. I. Реакции по альдегидной группе О NH3 СН2ОН ─ (СН ОН)4 ─ С + Аg2О →
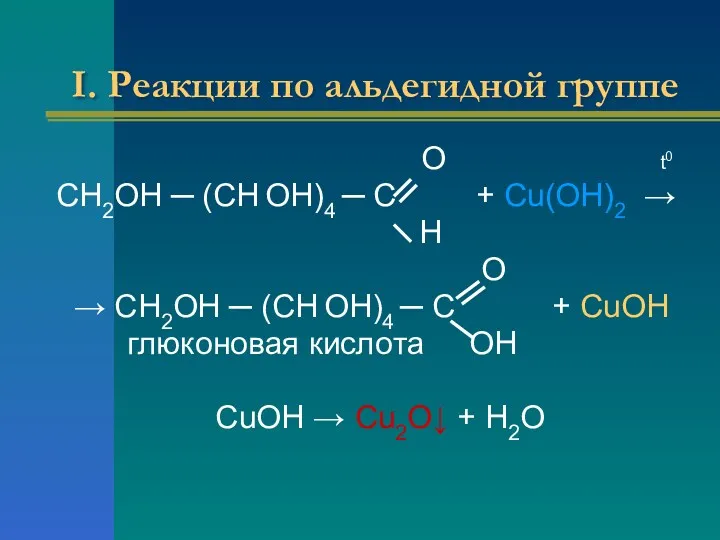
- 17. I. Реакции по альдегидной группе О t0 СН2ОН ─ (СН ОН)4 ─ С + Cu(OH)2 →
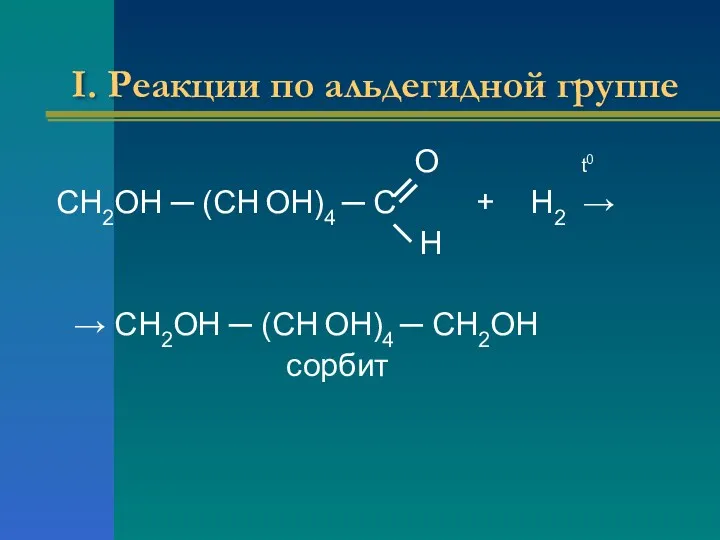
- 18. I. Реакции по альдегидной группе О t0 СН2ОН ─ (СН ОН)4 ─ С + H2 →
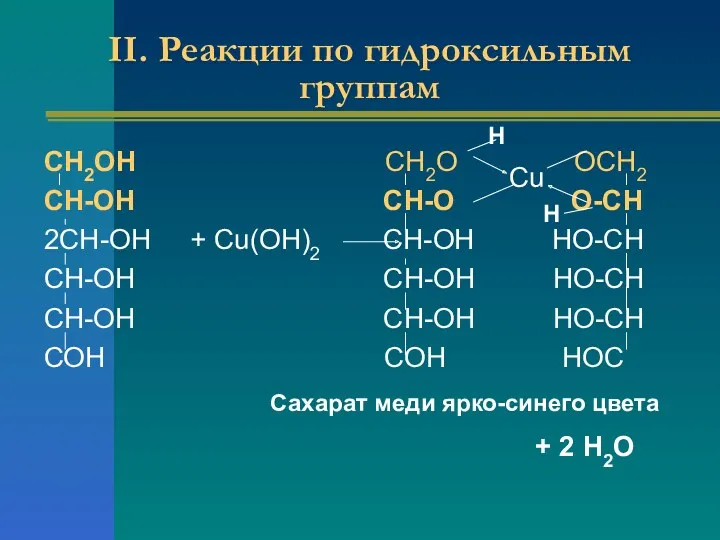
- 19. II. Реакции по гидроксильным группам СН2ОН CН2О ОCН2 СН-ОН СН-О О-СН 2СН-ОН + Cu(OH)2 СН-ОН НО-СН
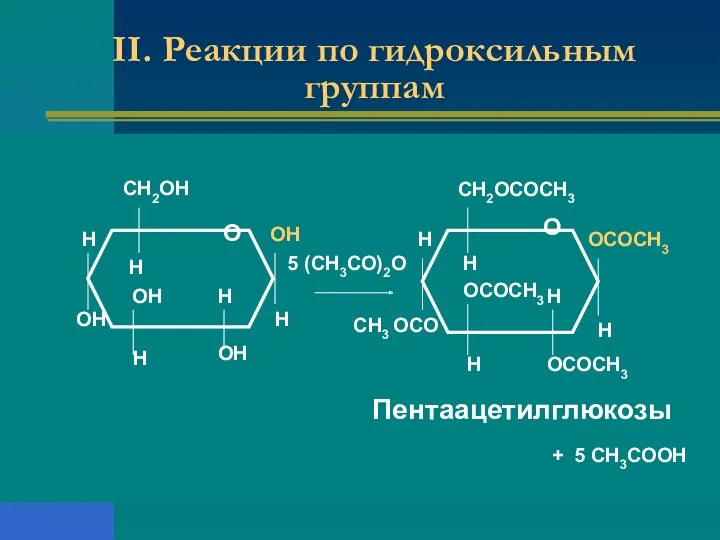
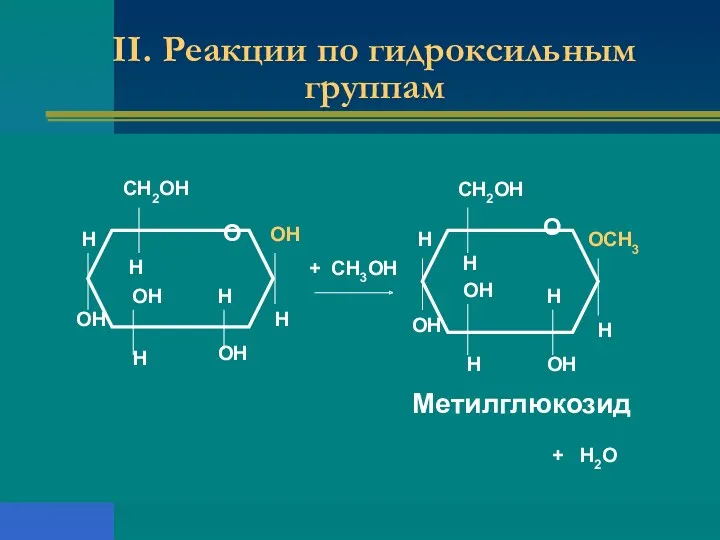
- 20. II. Реакции по гидроксильным группам СН2ОН Н Н ОН ОН Н Н ОН ОН Н О
- 21. II. Реакции по гидроксильным группам СН2ОН Н Н ОН ОН Н Н ОН ОН Н О
- 22. Специфические свойства глюкозы-реакции брожения Спиртовое С6Н12О6 → 2 С2Н5ОН + 2 СО2↑ Молочнокислое С6Н12О6 → 2
- 24. Скачать презентацию













 Табиғаттағы уран
Табиғаттағы уран Учет расходов по займам и кредитам
Учет расходов по займам и кредитам мини проект Семья
мини проект Семья Культурно-зрелищные здания
Культурно-зрелищные здания Мотель как новый тип гостиничного предприятия
Мотель как новый тип гостиничного предприятия Российское законодательство. Юридическая ответственность: понятие, принципы, признаки, виды
Российское законодательство. Юридическая ответственность: понятие, принципы, признаки, виды Теневая экономика в России
Теневая экономика в России Детский травматизм. Особенности травм у детей
Детский травматизм. Особенности травм у детей Линейное уравнение с одной переменной (урок 2)
Линейное уравнение с одной переменной (урок 2) Возведение зданий с металлическим каркасом
Возведение зданий с металлическим каркасом Система универсально-сборной технологической оснастки (УСП) станков
Система универсально-сборной технологической оснастки (УСП) станков Государственная поддержка сельскохозяйственных товаропроизводителей
Государственная поддержка сельскохозяйственных товаропроизводителей Родительское собрание. Итоги 1 четверти
Родительское собрание. Итоги 1 четверти Гострі респіраторні вірусні унфекціїї у дітей. Діагностика. Ускладнення. Терапія
Гострі респіраторні вірусні унфекціїї у дітей. Діагностика. Ускладнення. Терапія Особенности функциональной межполушарной асимметрии
Особенности функциональной межполушарной асимметрии Обмен углеводов-3
Обмен углеводов-3 Средства, влияющие на свертывание крови
Средства, влияющие на свертывание крови Технология и организация производства работ при ремонте и реконструкции зданий и сооружений Гродно
Технология и организация производства работ при ремонте и реконструкции зданий и сооружений Гродно Использование игровых технологий при обучение в дошкольном возрасте правилам дорожного движения.
Использование игровых технологий при обучение в дошкольном возрасте правилам дорожного движения. Механическая энергия. Закон сохранения
Механическая энергия. Закон сохранения Медикэр және Медикейд бағдарламалары
Медикэр және Медикейд бағдарламалары Личностно – ориентированное обучение школьников на уроках географии путем активизации познавательной деятельности
Личностно – ориентированное обучение школьников на уроках географии путем активизации познавательной деятельности Ладыгина Ольга. Практика
Ладыгина Ольга. Практика Урок Выразительные средства в музыке
Урок Выразительные средства в музыке Познавай бумагу!
Познавай бумагу! Текстовый и символьный типы данных Паскаль
Текстовый и символьный типы данных Паскаль Основные стратегии осмысления природы человека в классической философии
Основные стратегии осмысления природы человека в классической философии Комплекс артикуляционной гимнастики для постановки звука Л
Комплекс артикуляционной гимнастики для постановки звука Л