Содержание
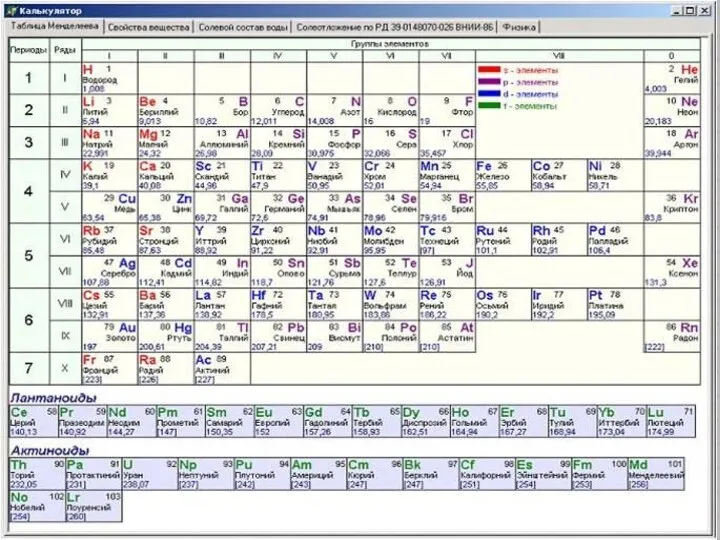
- 3. Be, Mg, Ca, Sr, Ba, Ra Щелочноземельные (радиоактивен) 1. На внешнем энергетическом уровне – 2 электрона
- 4. ФИЗИЧЕСКИЕ СВОЙСТВА Легкие Серебристо-белые (Sr – золотистый оттенок) Be и Mg – защитная оксидная пленка
- 5. ФИЗИЧЕСКИЕ СВОЙСТВА бериллий магний Кальций (приложение) стронций
- 6. ХИМИЧЕСКИЕ СВОЙСТВА 1. Взаимодействие с неметаллами: а) + O2 (горение) – приложение б ) + Cl2
- 7. 2. Со сложными веществами а) с водой (кроме Be – защищен оксидной пленкой. Mg – реагирует
- 8. СОЕДИНЕНИЯ МЕТАЛЛОВ II А ГРУППЫ Оксиды: BeO – амфотерный, другие – основные (BeO – амфотерный, другие
- 9. Гидроксиды - щелочи (кроме Be(OH)2 и Mg(OH)2) Получение: 1. Взаимодействие оксида с водой (приложение) CaO +
- 10. Соли: CaCO3 – мел, мрамор, известняк, кальцит
- 11. Мел
- 12. Мрамор
- 13. Известняк
- 14. кальцит
- 15. CaSO4 * 2H2O - гипс
- 17. Скачать презентацию













 Соединённое Королевство Великобритании и Северной Ирландии
Соединённое Королевство Великобритании и Северной Ирландии Музеи г. Перми
Музеи г. Перми Австрийская экономическая школа: общий анализ
Австрийская экономическая школа: общий анализ Презентация кабинета учителя - логопеда
Презентация кабинета учителя - логопеда Endured a heart break recently. Figure out how to move on and get over it successfully
Endured a heart break recently. Figure out how to move on and get over it successfully Атеросклероз
Атеросклероз Герои России и СССР
Герои России и СССР Преимущества и недостатки систем охлаждения ПК
Преимущества и недостатки систем охлаждения ПК Составление маркетингового плана
Составление маркетингового плана Русский язык на 8 февраля
Русский язык на 8 февраля Конструктивные особенности высокопроизводительных современных ЭВМ
Конструктивные особенности высокопроизводительных современных ЭВМ Презентация Мой любимый город Старый Оскол
Презентация Мой любимый город Старый Оскол Задания №13 и №16 (призма)
Задания №13 и №16 (призма) Коэффициенты рентабельности
Коэффициенты рентабельности Отчет по неделе игры и игрушки (старшая группа)
Отчет по неделе игры и игрушки (старшая группа) философия
философия Хохлома. Узоры
Хохлома. Узоры Профессиональная деятельность = активность
Профессиональная деятельность = активность Индивидуальный проект. Плазма-четвертое состояние вещества
Индивидуальный проект. Плазма-четвертое состояние вещества Мастер-карандаш (для дошкольников)
Мастер-карандаш (для дошкольников) Содержание и ремонт цементобетонных покрытий
Содержание и ремонт цементобетонных покрытий Sisteme VLSI reconfigurabile. Operatorii definiţi în limbajul Verilog
Sisteme VLSI reconfigurabile. Operatorii definiţi în limbajul Verilog Метаболизм лекарственных препаратов
Метаболизм лекарственных препаратов Арифметические операции в двоичной системе счисления
Арифметические операции в двоичной системе счисления Виртуальная экскурсия на Никольский завод хрусталя
Виртуальная экскурсия на Никольский завод хрусталя Профессиональные стандарты в лесной отрасли
Профессиональные стандарты в лесной отрасли Магистратура онтолингвистика май 2022
Магистратура онтолингвистика май 2022 Мои школьные будни (ಠ_ಠ)
Мои школьные будни (ಠ_ಠ)