Слайд 2

Слайд 3

ВОДОРОД
В П Р И Р О Д Е
H
1
1 ,
Слайд 4

Земная кора
(массовая доля)
1 %
99 %
Слайд 5

В составе атмосферного воздуха присутствие водорода менее 0,0001 %
Слайд 6

Слайд 7

Слайд 8

Слайд 9

Каменный уголь
Горные породы
и минералы
Слайд 10

На долю
водорода
приходится
50 % массы
Солнца и других
звезд
Слайд 11

Слайд 12

Общая характеристика водорода
Слайд 13

Слайд 14

Получение водорода.
В лаборатории:
Взаимодействие цинка с соляной кислотой:
Zn+2H Cl=ZnCl2+ H2
хлорид
цинка
Взаимодействие калия с водой:
2К+2H2O=2KOH+H2
гидроксид
калия
3.Взаимодействие алюминия с водным раствором щелочи
2Al+ 2 NaOH + 6 H2O= 2 Na[Al(OH) 4]+3H2
Слайд 15

В промышленности:
1.Разложение воды электрическим током:
2H2O=2H2+O2
2. Крекинг метана
CH4 = C + 2H2
3.
Каталитическая паровая конверсия метана
CH4 + O2 = СO2 + 2H2
Слайд 16

Слайд 17

Слайд 18

Способы собирания водорода:
Собирание водорода методом вытеснения воды;
Слайд 19

Собирание водорода методом вытеснения воздуха.
Слайд 20

Физические свойства водорода



















 Начальный период евангельской истории: События, предшествующие рождеству Христа Спасителя (Лекция 3)
Начальный период евангельской истории: События, предшествующие рождеству Христа Спасителя (Лекция 3) Элементная база современных электронных устройств
Элементная база современных электронных устройств Проектная деятельность учащихся.Из опыта работы.
Проектная деятельность учащихся.Из опыта работы. Аналого-цифровые и цифроаналоговые преобразователи
Аналого-цифровые и цифроаналоговые преобразователи Презентация к классному часу в 3 классе по теме Моя малая Родина - Шаховская
Презентация к классному часу в 3 классе по теме Моя малая Родина - Шаховская 3 сыйныфның рус төркемендә бәйлек сүзләр темасы буенча үткәрелгән видео дәрес
3 сыйныфның рус төркемендә бәйлек сүзләр темасы буенча үткәрелгән видео дәрес Общие положения об обязательствах
Общие положения об обязательствах Списание машин
Списание машин Рациональное питание
Рациональное питание Презентация Притча о друге
Презентация Притча о друге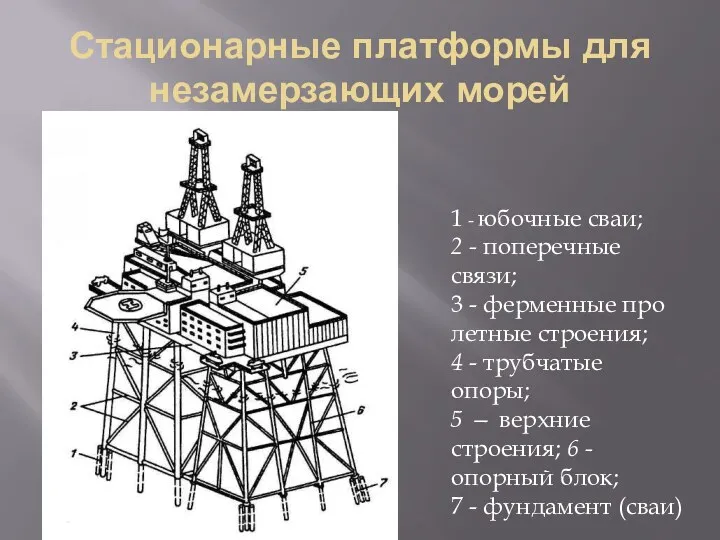 Стационарные платформы для незамерзающих морей
Стационарные платформы для незамерзающих морей Презентация к проекту Технология
Презентация к проекту Технология The modal verbs can, could and would
The modal verbs can, could and would Захист прав використання нематеріальних активів
Захист прав використання нематеріальних активів особенности работы с семьями воспитанников в условиях лекотеки
особенности работы с семьями воспитанников в условиях лекотеки Мастер класс по теме Магия пластилина
Мастер класс по теме Магия пластилина Стиль модерн
Стиль модерн Топливно-энергетический комплекс мира.
Топливно-энергетический комплекс мира. Ультразвуковые методы исследования белков
Ультразвуковые методы исследования белков Презентация проекта ЭкоСелфи
Презентация проекта ЭкоСелфи 23 февраля
23 февраля Проектирование промежуточной станции
Проектирование промежуточной станции Порядок прохождения военной службы офицерским составом. Тема №6
Порядок прохождения военной службы офицерским составом. Тема №6 Лимфопролиферативные заболевания
Лимфопролиферативные заболевания Стратегический анализ. Стратегический маркетинг. Стратегическое управление логистикой
Стратегический анализ. Стратегический маркетинг. Стратегическое управление логистикой Учителю химии
Учителю химии Модели. Моделирование
Модели. Моделирование Транспортная и инфраструктурная система - Краснодар
Транспортная и инфраструктурная система - Краснодар