Содержание
- 2. Актуальность: Антитела животного происхождения (сыворотки, моноклональные антитела) обладают недостатком: низкая степень афинности и авидности этих антител
- 3. В-лимфоциты являются основным клеточным функционером гуморального иммунитета. Для осуществления этой функции В-лимфоциты имеют на своей поверхности
- 4. Рецепторы В-лимфоцитов: CD21 – рецептор для С3 компонента комплемента; CD23 – низкоаффинный рецептор для IgE; CD40
- 5. Антитела – белки, вырабатывающийся В-лимфоцитами в ответ на внедрение в организм антигена. Антитела содержат 4 цепи:
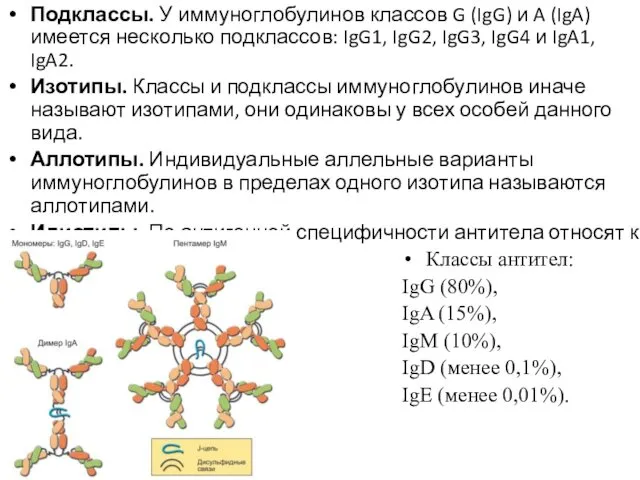
- 6. Классы антител: IgG (80%), IgA (15%), IgM (10%), IgD (менее 0,1%), IgE (менее 0,01%). Подклассы. У
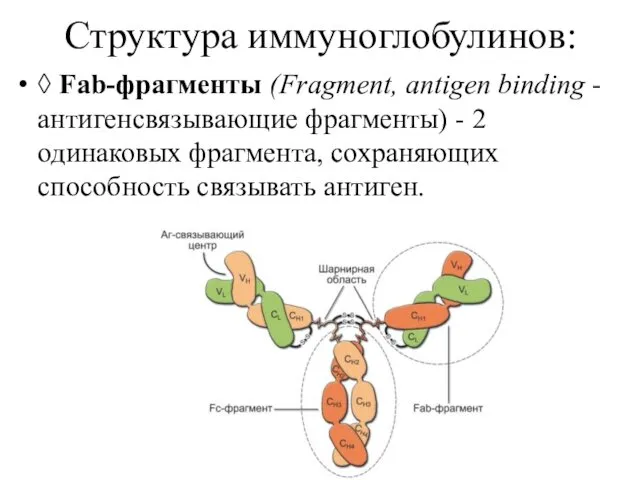
- 7. Структура иммуноглобулинов: ◊ Fab-фрагменты (Fragment, antigen binding - антигенсвязывающие фрагменты) - 2 одинаковых фрагмента, сохраняющих способность
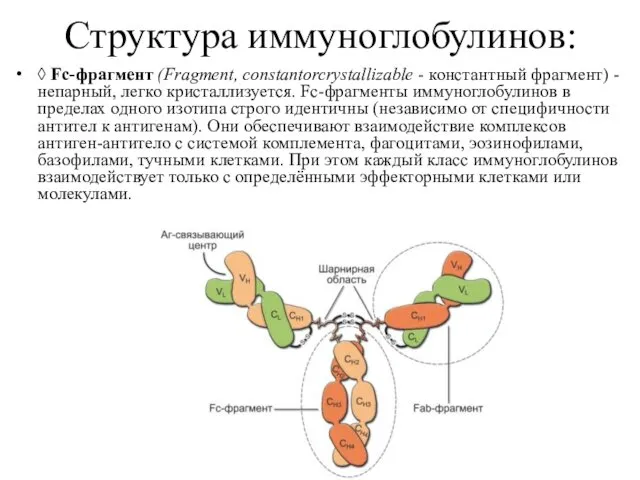
- 8. Структура иммуноглобулинов: ◊ Fc-фрагмент (Fragment, constantorcrystallizable - константный фрагмент) - непарный, легко кристаллизуется. Fc-фрагменты иммуноглобулинов в
- 9. Производство антител. Антитела практически невозможно синтезировать без использования живых систем, т.к. они имеют очень сложное строение.
- 10. Путем изменения генетических конструкций, кодирующих антитело, можно влиять на такие его характеристики, как способ действия, селективность
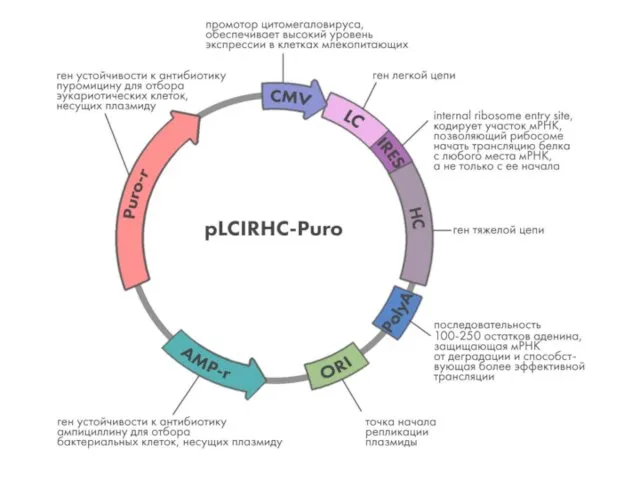
- 11. Генная инженерия антител Сейчас существуют программы, позволяющие оптимизировать нуклеотидную последовательность генно-инженерных конструкций для продукции антител in
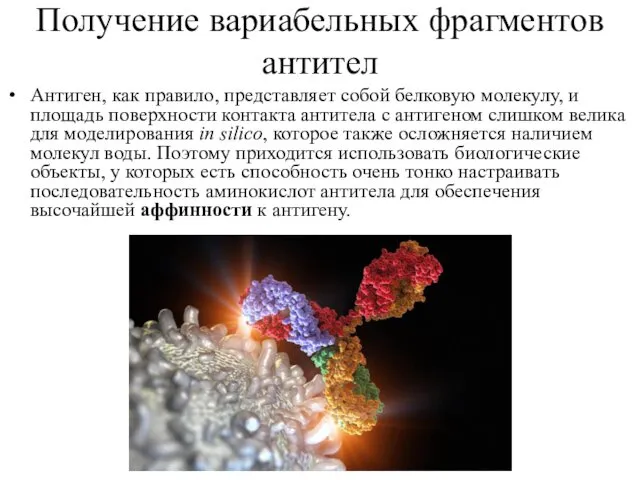
- 13. Получение вариабельных фрагментов антител Антиген, как правило, представляет собой белковую молекулу, и площадь поверхности контакта антитела
- 14. Дисплейные методы получения антител. За использование метода фагового дисплея в отборе пептидов и антител была присуждена
- 15. Получение антитела дисплейным методом in vitro схематически подражает эволюционному процессу формирования антител в организме : Сперва
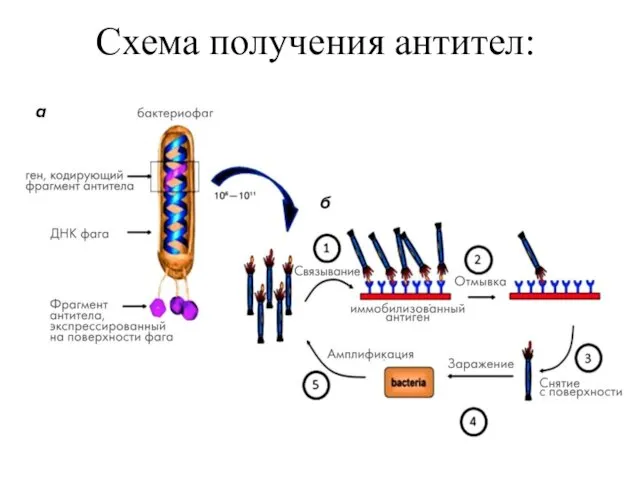
- 16. Схема получения антител:
- 17. 1. Целевые белки или последовательности ДНК помещаются в ячейки микротитрационного планшета. 2. Различные генетические последовательности, вставленные
- 18. Выводы: При помощи современных технологий можно прибегнуть к созданию антител без иммунизации крупных животных. В настоящее
- 20. Скачать презентацию







 Демо версия 2009 ЕГЭ по химии
Демо версия 2009 ЕГЭ по химии Цветная металлургия мира
Цветная металлургия мира Русь у ХІ-ХІІІ століттях. Період усобиць, роздробленості та занепаду
Русь у ХІ-ХІІІ століттях. Період усобиць, роздробленості та занепаду Психологические основы творчества. Решение педагогических ситуаций
Психологические основы творчества. Решение педагогических ситуаций Родительское собрание Мир подростка
Родительское собрание Мир подростка ВИКТОРИНА ДЛЯ НАСТОЯЩИХ И БУДУЩИХ УЧИТЕЛЕЙ
ВИКТОРИНА ДЛЯ НАСТОЯЩИХ И БУДУЩИХ УЧИТЕЛЕЙ Технология написания сочинения по заданному тексту. ЕГЭ 2020
Технология написания сочинения по заданному тексту. ЕГЭ 2020 Реформы управления Петра I
Реформы управления Петра I Звук [Ч]. Буква Ч
Звук [Ч]. Буква Ч День защитника Отечества Диск
День защитника Отечества Диск Параметры Excel
Параметры Excel ПАЛЬЦЕХОД - логопособие своими руками.
ПАЛЬЦЕХОД - логопособие своими руками. Пилюлялар дәрілік түр ретінде. Пилюлялар дайындау үшін қолданылатын көмекші заттар
Пилюлялар дәрілік түр ретінде. Пилюлялар дайындау үшін қолданылатын көмекші заттар Air conditioning system (HD)
Air conditioning system (HD) Показательные уравнения. 10 класс
Показательные уравнения. 10 класс Подготовка природных газов к переработке
Подготовка природных газов к переработке Методы диагностики ИБС в амбулаторных условиях
Методы диагностики ИБС в амбулаторных условиях Комбинаторика. Перестановки. Размещение. Сочетание
Комбинаторика. Перестановки. Размещение. Сочетание Глобализация, её проявления и последствия
Глобализация, её проявления и последствия Топографическая анатомия и оперативная хирургия органов таза и забрюшинного пространства
Топографическая анатомия и оперативная хирургия органов таза и забрюшинного пространства Международные организации.
Международные организации. Желудок и поджелудочная железа. Очищение
Желудок и поджелудочная железа. Очищение Қытай. Мемлекеттегі темір жол көлігі және оның ерекшеліктері
Қытай. Мемлекеттегі темір жол көлігі және оның ерекшеліктері Смысловые типы текста
Смысловые типы текста Класс Насекомые. Внешнее строение насекомых. Внутреннее строение майского жука
Класс Насекомые. Внешнее строение насекомых. Внутреннее строение майского жука Презентация Педагогическая этика воспитателя
Презентация Педагогическая этика воспитателя Критерии подобия. Подобие течений неоднородных жидкостей в пористой среде при линейном законе сопротивления
Критерии подобия. Подобие течений неоднородных жидкостей в пористой среде при линейном законе сопротивления Легализация (отмывание) денежных средств. Современное состояние и предупреждение
Легализация (отмывание) денежных средств. Современное состояние и предупреждение